Электрофорез новорожденным: Электрофорез | Детский медицинский центр «ЧудоДети»
Физиотерапия для детей, онлайн-запись на консультацию к специалисту – сеть клиник МЕДСИ
Физиотерапия для лечения детей предлагает большое количество разнообразных по лечебному действию процедур, которые могут быть назначены ребенку с первых дней жизни для повышения защитных сил, лечения и профилактики заболеваний, правильного развития систем организма. При этом методика проведения и техника физиотерапевтических процедур для детей существенно отличаются от применяемых для взрослых. Это различие определяется возрастными анатомо-морфологическими особенностями.
Физиотерапевтические процедуры для новорожденных длятся не более 5 минут, поскольку развитие нервной системы малышей еще не завершено, ей свойственна быстрая истощаемость ответных реакций.
Для профилактики и лечения рахита у детей раннего возраста эффективно местное УФ-облучение (лицо, кисти, стопы).
Наиболее часто физиотерапевтическое лечение детей применяют при таких заболеваниях:
- При болезнях кожи и пупка у новорожденных (омфалите, опрелости, пиодермии)
- Для лечения флегмоны новорожденных
- Для лечения острого гематогенного остеомиелита
- При последствиях родовой травмы
- Для профилактики и лечения рахита
Для лечения аллергических реакций могут быть применены:
- Переменное магнитное поле
- Теплые лекарственные ванны
- Дарсонвализация
- Ультразвук
- Общие УФ-облучения
- Электрофорез
Эффективна физиотерапия при лечении и реабилитации заболеваний опорно-двигательного аппарата:
- Сколиотическая болезнь
- Врожденная косолапость
- Врожденный вывих бедра
- Остеохондропатии
- Травмы
- Ювенильный ревматоидный артрит и др.

Здесь применяют:
- УВЧ-терапию
- УФ-эритему
- Лекарственный электрофорез
- Амплипульстерапию
- Электростимуляцию
- Массаж
Восстановительное лечение заболеваний нервной системы (последствий нейроинфекций, детских церебральных параличей, периферических нервов, черепно-мозговых травм, нейромышечной дистрофии и т. д.) проводят в основном методами физиотерапии: УВЧ-терапией, амплипульстерапией, электростимуляцией, лекарственным электрофорезом, массажем, УФ-облучениями, ЛФК. При наличии невротических реакций, неврозов (тиков, заикания, энуреза и др.) хороший эффект получают от применения лекарственного электрофореза, эндоназальной гальванизации, общих УФ-облучений.
Широко используют физиотерапевтические методы при лечениия ЛОР-заболеваний (тонзиллитов, отитов, риносинуситов и др.):
- УФ-облучение
- Ингаляции
- Электрическое поле УВ
- Лекарственный электрофорез
- Ультрафонофорез
Физиотерапевтические процедуры могут быть назначены и при профилактике болезней сердечно-сосудистой системы:
- Миокардита
- Ревматизма
- Кардиопатии
- Аритмий
- Пороков сердца
-
Артериальной гипертензии и т.

Для чего делать электрофорез ребенку
Количество детей, имеющих врожденные или приобретенные заболевания, увеличивается с каждым годом. Наряду с современными фармакологическими препаратами актуальность не утратили и физпроцедуры. Электрофорез не назначают детям при любых заболеваниях, а его способы различаются в зависимости от показаний.
Содержание:
Особенности электрофореза у детей
При назначении лечения зачастую выбор педиатров падает на вспомогательную терапию – электрофорез(или ионофорез). Он безопасен, имеет минимальные риски побочных эффектов, позволяет вводить небольшие дозы лекарств в место с патологическими изменениями. Процедура безболезненна для маленького пациента, ткани при введении лекарства не повреждаются.
Популярность вызвана тем, что ток способен оказывать положительное воздействие на организм человека:
-
расширяет сосуды;
-
расслабляет мышцы;
-
снимает воспаление;
-
стимулирует иммунитет;
-
регулирует гормональный фон.

Проведение электрофореза у детей и взрослых различается потому что:
-
Детская кожа тоненькая и незрелая, имеет меньше клеточных слоев.
-
Кожный покров детей быстрее всасывает вещества, обладает низкой сопротивляемостью току.
-
До четырех месяцев у младенцев не развиты потовые железы, терморегуляция недостаточно развита.
-
Эпидермис у детей обладает высокой способностью к регенерации.
В связи с перечисленными факторами лечение электрофорезом нужно проводить под контролем медицинского персонала и родителей, соблюдая меры предосторожности.
У детей младшего возраста процедура не должна превышать 7-8 минут. Детям более старшего возраста длительность увеличивается до 15-20 минут.
Показания для назначения электрофореза детям
Физпроцедуры занимают особое место в комплексном лечении разных болезней у детей. Их назначают при простудных заболеваниях, неврологических патологиях, болезнях костно-мышечной системы. Основные показания включают:
Их назначают при простудных заболеваниях, неврологических патологиях, болезнях костно-мышечной системы. Основные показания включают:
-
Поражения центральной нервной системы (в результате гипоксии, ишемии, ДЦП).
-
Черепно-мозговые травмы, инфекции головного мозга, их последствия.
-
Астенический синдром.
-
Заболевания ЛОР-органов и полости рта.
-
Болезни органов дыхания (пневмония, бронхит).
-
Нарушения работы желудочно-кишечного тракта.
-
Патологии мочевыделительной системы.
-
Заболевания опорно-двигательного аппарата (гипо- или гипертонус мышц, дисплазия тазобедренных суставов).
-
Родовые травмы спины или головы, патологии шейного отдела позвоночника.

-
Поражения периферических нервов (нейропатии, невриты).
-
Воспалительные процессы внутренних органов с бактериальным поражением.
Назначает электрофорез только врач (педиатр, травматолог-ортопед, невролог или уролог). Специалист подбирает нужную дозировку лекарства, силу тока, количество процедур, выявляет противопоказания. Плюсом физиотерапии является то, что при введении лекарств отсутствует системное воздействие на организм, препарат действует локально в очаге поражения.
Варианты проведения процедуры у детей
Большая часть методов подходит как взрослым, так и маленьким пациентам. Рассмотрим методики, наиболее подходящие детям.
-
Гальванический воротник по Щербаку. Назначается детям старше двух лет для лечения неврозов, нарушения сна, травм головы. Используется два электрода: первый размещают в области шеи, второй – на пояснице.
 Силу тока и длительность процедуры увеличивают постепенно. Курс лечения – 10-12 процедур.
Силу тока и длительность процедуры увеличивают постепенно. Курс лечения – 10-12 процедур.
-
Методика Вермеля. Такой электрофорез назначается новорожденным детям при родовой травме, неврологических проблемах. Используют два электрода: первый размещают между лопатками, второй – на живот или бедра. Продолжительность воздействия составляет не более 10 минут, количество процедур – 10.
-
Внутритканевой электрофорез. Назначается при острых патологиях и сопутствующей аллергии на лекарства. Эффективен при пневмонии на ранней стадии. Представляет собой одновременное внутривенное введение лекарства и гальванизацию грудной клетки. Благодаря этому антибиотик действует именно в бронхолегочной системе.
-
Метод по Бургиньону. Показан при неврологических внутричерепных заболеваниях (вегетососудистой дистонии, ишемическом или травматическом поражении нервной системы).

-
Назальный электрофорез. Назначается для лечения заболеваний ЛОР-органов. Электроды вводятся в носовые ходы, а также на область шеи сзади. При проведении используют новокаин и кальций, предварительно промывают нос физраствором. Подходит более старшим детям, так как электроды проблематично вводить в нос новорожденным и дошкольникам. Длительность сеанса – 15-20 минут.
-
Метод по Левину. Назначаетсяприповышенном тонусе мышц, например, при ДЦП и иных поражениях головного мозга. Электроды закрепляют на пальцах конечностей. Используют одновременно с новокаином и адреналином.
-
Способ Келлата-Змановского. Назначается при заикании, спастической дизартрии. Электроды размещаются на голове по бокам, процедура длится недолго: 5-15 минут в зависимости от тяжести симптомов и назначения невролога.
 Курс терапии включает 10 сеансов.
Курс терапии включает 10 сеансов.
-
При патологиях суставов. Новорожденным назначается при дисплазии тазобедренных суставов. Хороший эффект достигается при одновременной магнитотерапии.
Как делают электрофорез
Механизм действия следующий: на тело, прокладку и электрод наносят лекарственное вещество. Его ионы приводятся в движение электрическим током. Через потовые протоки по кровотоку лекарство поступает к нужным органам и тканям. Эффект от терапии зависит от концентрации вещества, силы тока, длительности процедуры, специфики кожного покрова пациента.
При проведении процедуры детям устанавливаются минимальные параметры. Чтобы избежать испуга и боязни, маленьких детей важно правильно настроить на лечение, объяснить, что не будет больно, но возможны слабые пощипывания. Первую процедуру с целью знакомства проводят на минимальных показателях или даже без включения аппарата.
Грудничкам сеанс проводят через час после кормления или за 45 минут до него.
Перед началом терапии и после нее медсестра обязана провести осмотр кожи. Повреждений, покраснений и ожогов быть не должно. После воздействия тока область накладывания электродов желательно смазать кремом или специальным маслом.
Противопоказания
Несмотря на отсутствие болевых ощущений, манипуляция имеет противопоказания:
-
Повреждения кожного покрова на местах наложения пластин.
-
Кожные заболевания (пятна, высыпания, покраснения).
-
Патологии сердца, наличие кардиостимулятора.
-
Повышенная температура тела.
-
Бронхиальная астма в стадии обострения.
-
Выявленная аллергия на назначенный препарат.

-
Инфекционно-воспалительный процесс в острой фазе.
Имеющиеся опухолевые поражения выступают абсолютным препятствием к назначению ионофореза.
Электрофорез активно применяется в педиатрической практике: при лечении неврологических патологий, ортопедических проблемах, ЛОР-заболеваниях. Метод отличается доступностью, эффективностью, безопасностью, позволяет обеспечить доступ лекарства к патологическому очагу. Контролировать ход процедуры должен врач-физиотерапевт, а при наличии противопоказаний подбирается альтернативный метод физлечения.
Детская поликлиника в Кургане — «Центр здоровья ребёнка»
Современный медицинский центр «Здоровье ребёнка» открылся в стенах нашей клиники в 2014 году. Здесь ведут прием узкопрофильные специалисты, врачи-педиатры, детские хирурги, ортопеды, аллергологи, иммунологи, логопеды, неврологи, специалисты в области детской эндокринологии, кардиологии, а также гастроэнтеролог, физиотерапевт. Проводятся лечебно-диагностические и профилактические процедуры: массаж, УЗИ, МРТ. Физиотерапевтический кабинет работает даже с грудничками, проводятся такие физиопроцедуры, как: парафинотерапия, лазерная терапия, тубусный кварц, электрофорез, небулайзер, амплипульс, светолечение и другие.
Проводятся лечебно-диагностические и профилактические процедуры: массаж, УЗИ, МРТ. Физиотерапевтический кабинет работает даже с грудничками, проводятся такие физиопроцедуры, как: парафинотерапия, лазерная терапия, тубусный кварц, электрофорез, небулайзер, амплипульс, светолечение и другие.
Более подробную информацию узнайте в центре или по телефону.
Если вам нужна справка в детский сад, школу, другое учебное заведение, а также справка в бассейн, пионерлагерь, санаторно-курортная карта, то вы также можете оформить документы быстро и без проблем.
Детская поликлиника в Кургане
К здоровью детей важно относиться с особой тщательностью и трепетом. Ведь именно в детском возрасте закладывается здоровье человека на всю жизнь, формируется организм. Если ребенок заболел — необходим особый, чуткий и внимательный подход высококвалифицированных специалистов. Важно выявить причину заболевания, провести детальное, максимально полное обследование, на основании которого назначить правильное, наиболее подходящее лечение.
Мы предоставляем амбулаторно-поликлинические услуги по многим направлениям, проводим диагностику и лечебные процедуры в одном месте, что очень удобно для вас и вашего ребенка.
- Врачи всех специализаций в одной клинике — вы вправе рассчитывать на компетентную помощь высококлассных специалистов.
- Лечение детей любого возраста — мы работаем с пациентами от 0 до 18 лет.
- Современный диагностический центр — чтобы пройти тщательное обследование не нужно ехать в другую больницу.
- Проводится широкий спектр лечебно-оздоровительных мероприятий непосредственно в стенах центра, что также удобно для вас.
- Максимум комфорта для детей и родителей — вам не придется простаивать в очередях в ожидании приема. Сотрудники центра всегда доброжелательно и чутко относятся к посетителям, решают проблемы со здоровьем ребенка наилучшим для него образом, не вызывая стресса и страхов, что благоприятно сказывается на ранимой психике ребенка.
- Приятная обстановка — интерьер оформлен таким образом, чтобы вы чувствовали себя уютно, все кабинеты найти легко, для новорожденных есть пеленальные столики, а детей постарше — игровая зона.

Мы заботимся о сохранении здоровья детей с самого раннего возраста. Пройдите ежегодные профилактические осмотры у педиатров и узкопрофильных специалистов, чтобы убедиться в абсолютном здоровье малыша или своевременно выявить проблемы. Также наши специалисты дадут полезные рекомендации по уходу за детьми, правильному питанию, проведению оздоровительных процедур и гигиене.
Заботьтесь о здоровье детей правильно. Обеспечьте себе и ребенку максимум пользы и комфорта при обращении к врачам. Цените время. Приходите в наш центр «Здоровье ребенка».
Отделение патологии новорожденных и раннего возраста
В декабре 2006 года отделение патологии новорожденных было открыто после капитального ремонта, которое состоит из 19 палат « Мать и Дитя» , расположенных на 3-х постах. На первый и второй посты поступают дети непосредственно из роддомов. На этих постах выделено по 3 палаты для выхаживания недоношенных детей. На 3-ой пост принимаются новорожденные дети с участка. Каждая палата оборудована новой сантехникой с подачей горячей и холодной воды, пеленальным столом, баком с клеенчатым мешком для сбора грязного белья, бактерицидной лампой, детской кроваткой, кроватью для мамы. Все предметы имеют легко обрабатывающуюся поверхность.
На этих постах выделено по 3 палаты для выхаживания недоношенных детей. На 3-ой пост принимаются новорожденные дети с участка. Каждая палата оборудована новой сантехникой с подачей горячей и холодной воды, пеленальным столом, баком с клеенчатым мешком для сбора грязного белья, бактерицидной лампой, детской кроваткой, кроватью для мамы. Все предметы имеют легко обрабатывающуюся поверхность.
Отделение патологии новорожденных расположено на первом этаже и изолировано от других отделений. Принимаются дети с рождения до 1,5 мес. Отделение рассчитано на 15 коек, которое имеет межтерриториальное значение, оказывая медицинскую помощь новорожденным нашего города и района , а также новорожденным г. Гурьевска и Салаира, пос. Красный Брод и других городов области.
На сестринском посту находится все необходимое для ухода за ребенком: шкаф с медикаментами для неотложной помощи при экстренных ситуациях, лекарства, предназначенные для раздачи больным, средства для наружного применения, мединструментарий, необходимый для ухода за новорожденными ( стерильные пипетки, термометры, шпателя, пинцеты), биксы со стерильным материалом. На сестринском посту находится стол для хранения медицинской документации. Пост имеет подводку горячей и холодной воды, весы, электроотсос, ингалятор.
На сестринском посту находится стол для хранения медицинской документации. Пост имеет подводку горячей и холодной воды, весы, электроотсос, ингалятор.
В палатах для недоношенных детей размещены кювезы закрытого типа (всего 6 ) с двойными стенками, встроенными весами, кроме того имеются 5 кроваток-грелок, 2 пеленальных стола с подогревом «Аист». Каждый пост имеет централизованную подачу кислорода. Сейчас у нас появилась возможность использовать кислородные палатки, вместо ранее используемых носовых катетеров.
Недоношенные получают кислородотерапию в кювез. Также для недоношенных детей приобретена сенсорная панель * Beby sense * для выявления апное. Все палаты расположены на солнечную, южную сторону.
В отделении есть процедурный кабинет, оборудованный холодильником для хранения препаратов крови, ее заменителей и других медикаментов, шкафами для медикаментов, шкафами для инструментария и аппаратуры, системами для в/в вливаний, шприцев, столом для забора крови. Имеется передвижной столик для доставки всего необходимого в стерильных условиях в боксы, где проводятся все манипуляции. В процедурном кабинете имеется подводка горячей и холодной воды, бактерицидная лампа, электроотсос.
Из подсобных помещений есть комната для хранения чистого белья, отдельно от нее комната для сбора грязного белья, которое выносится сюда из боксов в клеенчатых мешках. Счет и сортировка белья проводятся в комнате с подводкой горячей и холодной воды для последующей обработки рук. Комната для сбора грязного белья оборудована большим ящиком и бактерицидной лампой. Сейчас у нас оборудована собственная прачечная, что облегчает работу отделения.
Среди других помещений на посту новорожденных имеются :
- ординаторская;
- кабинет старшей медсестры;
- кабинет кастелянши;
- санитарная комната для матерей, оборудованная душем;
- ванная комната;
- гладильная комната;
- комната для сан. обработки мед оборудования;
- холл для отдыха матерей.
Перевод детей на пост новорожденных осуществляется в основном на 6 – 7 день жизни ребенка по договоренности с зав. отделением. Для недоношенных детей заранее готовится кювез. При размещении детей в палатах устанавливается цикличность, а также обязательно учитываются нозология, сроки жизни. Дети с инфекционной патологией переводятся в отделение сразу после выявления заболевания. Дети в тяжелом и крайне тяжелом состоянии осматриваются врачом-реаниматологом нашей больницы в роддоме, и если необходим и возможен перевод, то он осуществляется врачом реаниматологом или неонатологом роддома. Все новорожденные дети, поступившие в детское реанимационное отделение ,ведутся совместно с неонатологом. Отказов в госпитализации нет.
Дети отделения патологии новорожденных обслуживаются общебольничным физиопроцедурным, R-кабинетом и др. диагностическими кабинетами, поэтому для приема новорожденных выделено специальное время с 8 до 9 часов утра. Такие процедуры как электрофорез, массаж, ингаляции лекарственных средств, парафинолечение осуществляются новорожденным непосредственно в палатах.
Влажная уборка боксов проводится 3 раза в сутки с дезрастворами, кварцевание боксов проводится 4 раза в сутки, согласно Приказу № 440.
В целях улучшения организации и качества оказания медицинской помощи новорожденным отделение работает по приказам:
- № 408 от 12.07.89 «О мерах по снижению заболеваемости вирусным гепатитом по Российской Федерации».
- № 545 от 10.05.2011г. «О профилактике профессионального заражения ВИЧ инфекцией»
- СанПин 2.1.3.2630-10 Санитарно-эпидемические требования к организациям, осуществляющим медицинскую деятельность
- МЗ ОСТ42-21-02-1985г., который определяет методы, средства, режим дезинфекции и стерилизации изделий медицинского назначения.
- №345 «Профилактика внутрибольничных инфекций в акушерских стационарах и родильных домах.»
- № 440 от 30.04.1983г. «О дополнительных мерах по совершенствованиюмедицинской помощи новорожденным детям»
Для соблюдения санитарно-противоэпидемического режима отделения пользуемся следующими дез.средствами:1% р-р Виркона, Лизоформином, Бианолом, Диабаком, Хлормиксом. Рабочие растворы готовятся согласно инструкции каждого дез.средства. Все инъекциии и манипуляции, связанные с уходом за новорожденными, проводятся в перчатках. Персонал отделения ежеквартально проходит медицинский осмотр, регулярно обследуется на бациллоносительство. Ежемесячно берутся смывы с инструментария, белья, твердого и мягкого инвентаря, рук персонала. Бактериологический контроль за работой в отделении осуществляет городская санэпидстанция согласно плана производственного контроля.
Дети поста новорожденных по показаниям осматриваются узкими специалистами. По выписке из стационара все дети передаются на участок.
Врач неонатолог , повседневно решаю следующие задачи:
- Обеспечивает контакт и преемственность с роддомом и участковым врачом.
- Осматривет больных поста новорожденных: оцениваю их общее состояние , интересуюсь аппетитом, сном, характером стула. Оценивает динамику клинических симптомов и синдромов, параклинических показателей, физическое развитие. Рассчитывает питание и объем инфузионной терапии для недоношенных и тяжелых больных каждые 3 дня, следит за весовой кривой. На основании анамнеза, клинических синдромов, параклиники, осмотра специалистами ставит диагноз и назначает рациональную терапию.
- В случаях гипотрофии III степени рассчитывает парентеральное питание.
- Своевременно информирует СЭС о выявлении инфекционного заболевания или подозрении на него, занимается комплексной профилактикой инфекционных заболеваний.
- Ведет истории болезни, в срок 3 – 5 дней выставляет и обосновывает клинический диагноз, при длительном пребывании ребенка в отделении отражает динамику в этапных эпикризахкаждые 10 дней.
- Оформляет выписные эпикризы с подробными рекомендациями.
- Следит за соблюдением санэпид. режима в отделении, особенно в периоды заболеваемости ОРВИ, не допуская распространения инфекции путем изоляции новорожденных на отдельный пост, применения профилактических мер среди персонала.
- Обучает матерей приемам массажа и гимнастики, дает рекомендации по уходу за новорожденным.
На 1 рабочий час приходится 2-3 ребенка.
Кадры: укомплектованность врачебными кадрами, средним мед персоналом, младшим мед персоналом — 100%.
В отделении патологии новорожденных 2,5 врачебных ставок ОМС.
- Заведующий отделением патологии новорожденных, врач — неонатолог первой категории – Чештанова Т. Н. общий стаж работы 16 лет. Занимает 1 ставку заведующей отделением + 0,5 ставки врача-неонатолога. Стаж работы врачем-неонатологом (по сертификату) 8 лет.
В ОПН – 2 круглосуточных медсестринских поста . В отделении выделена процедурная и старшая медсестры, занимающие по 1,0 ставки – физических лиц 10. Всего медсестры занимают 21,5 медсестринских ставки. Стаж работы медицинских сестер от 7 до 30 лет. Средний медсестринский персонал отделения опытный. Высшую категорию имеют 7 медсестер, 3 первую категорию. С целью повышения квалификации среднего медицинского персонала проводятся сестринские общебольничные и отделенческие конференции. Младший мед персонал занимает 7 ставок – физических лиц 4. Прочего персонала — 5 ставок.
III Национальный Конгресс с международным участием ЛАБРиН «Инфекции. Год с COVID-19.»
Завершился III Национальный Конгресс с международным участием ЛАБРиН «Инфекции. Год с COVID-19.», который проходил в ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России.
На Конгрессе в рамках научной программы были затронуты следующие темы:
- Проблемы инфекций репродуктивного тракта.
- Инфекции у беременных и новорожденных.
- COVID-19: беременность, новорожденные и проблемы репродуктивного здоровья.
- COVID-19: преаналитика, лабораторная диагностика и перспективные разработки.
- COVID-19 и оценка состояния гемостаза.
- COVID-19 и вакцинопрофилактика.
- Организация лабораторной службы в условиях COVID-19.
- COVID-19 и дезинфекция.
- COVID-19: инфекции, связанные с оказанием медицинской помощи (ИСМП) и антибиотикорезистентность.
- Консолидация специалистов всех отраслей экономики в противодействии биологических угроз.
Компания ООО «Эко-мед-с М» приняла участие в выставке в рамках III Национального Конгресса.
На стенде компании был представлен экспресс анализатор Cepheid GeneXpert® для молекулярной диагностики.
В основе технологии GeneXpert® лежит запатентованный одноразовый картридж компании Cepheid, который содержит все необходимые реагенты для проведения анализа. В этой замкнутой «Лаборатории в картридже» проводится экстракция, амплификация и детекция. Данный анализатор полностью совместим с информационными и лабораторными системами
и базами данных.
• POC- молекулярная диагностика
• Быстрый результат
• Простота использования
• Широкая панель тестов
• Гибкость конфигурации и высокого качества проб.
Так же, на стенде компании были представлены системы вакуумные с поршнем для исследований проб крови S-monovette®. Закрытая система взятия крови состоит из пластикового контейнера с поршнем и иглы S-Monovette® или иглы-бабочки Multifly®, которые предназначены для совместного использования и обеспечивают герметичность системы. Небьющийся пластик минимизирует риск заражения гемоконтактными инфекциями и обеспечивает безопасность медицинского персонала при работе с кровью пациентов. Правильное наполнение пробирок обеспечивает точное соотношение кровь/реагент. Возможность использования в качестве первичных пробирок в системах лабораторной автоматизации экономит время на подготовку к исследованию, отбор и маркировку пробы. Использование закрытых системы взятия крови является основным инструментом для обеспечения стандартизации процедуры взятия крови и высокого качества проб.
Информация о семейном скрининге новорожденных: признак
На этой странице:
Что такое черта?
Сообщение о признаке гемоглобина
Почему важно знать, есть ли у вас признак гемоглобина
Информационные бюллетени
Часто задаваемые вопросы
Дополнительная информация и ресурсы
Контактная информация о признаке гемоглобина
Что такое черта?
Признак — это когда у человека нормальный гемоглобин и ненормальный гемоглобин. Гемоглобин входит в состав красных кровяных телец, и его задача — переносить кислород по всему телу.Один из видов тестирования, проводимого при скрининге новорожденных, — это поиск группы заболеваний, называемых гемоглобинопатиями.
Гемоглобинопатии — это наследственные заболевания, влияющие на структуру гемоглобина. Возможно, вы знакомы с наиболее распространенной гемоглобинопатией — серповидно-клеточной анемией. Однако, в отличие от серповидно-клеточной анемии, ожидается, что человек с признаками здоров и может прожить всю жизнь, не зная, что у них есть признаки. Хотя серповидно-клеточный признак является наиболее распространенным признаком, существует также много других признаков (например, признак C, признак E или признак D).Когда какая-либо черта наследуется вместе с нормальным гемоглобином, ожидается, что человек будет здоровым.
Связь с особенностями гемоглобина
Если при скрининге новорожденного будет установлено, что у ребенка есть какая-либо черта, матери ребенка по почте будет отправлен пакет информации о конкретной характеристике ребенка.
Мы напрямую свяжемся с лечащим врачом или клиникой, указанной в карточке скрининга новорожденного, чтобы подтвердить, что они видели ребенка, и отправим им результаты обследования новорожденных.Это одна из причин, по которой больницам и родильным специалистам важно получить имя врача или поликлиники ребенка, чтобы результаты скрининга новорожденного могли быть незамедлительно отправлены им.
Родители малышей с особенностями должны:
- Обсудите с врачом ребенка результат, его следующие шаги и важность результата для них самих, их ребенка и их семьи.
- Убедитесь, что их ребенок повторно проверил признак, чтобы подтвердить результат.
- Сохраняйте записи результатов анализов и пакета информации из программы скрининга новорожденных для использования в будущем.
Почему важно знать, есть ли у вас гемоглобин
Гемоглобин передается по наследству от родителей, например, цвет волос или глаз. Если один из родителей имеет признак гемоглобина, существует 50% (1 из 2) шанс при каждой беременности иметь ребенка с этим признаком.
Если у обоих родителей есть гемоглобин, существует 25% (1 из 4) шанс при каждой беременности иметь ребенка с серьезной гемоглобиновой болезнью, такой как серповидноклеточная анемия.
При каждой беременности у этой пары есть 25% (1 из 4) шанс иметь ребенка с серповидно-клеточной анемией, 50% (2 из 4) шанс иметь ребенка с чертой серповидноклеточной анемии и 25% (1 в 4) шанс иметь ребенка без каких-либо черт или болезней.
Информационные бюллетени
Вы можете найти наши информационные бюллетени о характеристиках на веб-странице «Болезни крови: информация и ресурсы»:
Часто задаваемые вопросы
A: Самая важная причина узнать, есть ли у вас черта характера, — это планирование семьи.Люди с особенностями имеют более высокий риск иметь ребенка с гемоглобиновой болезнью, такой как серповидно-клеточная анемия. Кроме того, есть некоторые редкие проблемы со здоровьем, которые могут возникнуть у людей с особенностями, поэтому для врачей может быть важно ежегодно обсуждать статус черты со своими пациентами. Чтобы узнать о своем индивидуальном риске, поговорите со специалистом в области здравоохранения или генетическим консультантом.
A: Младенцев проверяют при рождении на множество различных нарушений гемоглобина, включая серповидно-клеточную анемию.То, как проводится это тестирование, показывает младенцев, у которых есть особенность, хотя это не то, что искали. Поскольку эта черта наследуется в семье, важно сообщить опекуну ребенка и врачу, что она была обнаружена.
A: Люди любой расы или этнической принадлежности могут иметь гемоглобин. Определенные типы гемоглобина чаще встречаются у людей определенных национальностей. Например, серповидно-клеточная анемия чаще всего встречается у лиц африканского происхождения к югу от Сахары, но также может быть обнаружена у людей из Южной Америки, Карибского бассейна, Центральной Америки, Италии, Греции, Турции, Саудовской Аравии и Индии.Другие черты, такие как гемоглобин Е, наиболее распространены у лиц юго-восточноазиатского происхождения. Признак гемоглобина D чаще всего встречается у людей восточно-индийского происхождения.
A: Единственный способ узнать, есть ли у вас гемоглобин, — это пройти анализ. Простой анализ крови, называемый электрофорезом гемоглобина, может определить, есть ли у вас гемоглобин.
Ответ: Миннесота проводит скрининг на серповидно-клеточную анемию с 1988 года.Тестирование также выявляет здоровых младенцев с серповидно-клеточными признаками и другими признаками гемоглобина. К сожалению, MDH требовалось уничтожить пятна крови и результаты анализов у всех людей, у которых были пятна крови, собранные до 1 августа 2014 года. Единственным исключением являются случаи, когда родитель дал письменное согласие на долгосрочное хранение и использование своего ребенка или ребенка. пятна крови и результаты анализов.Мы понимаем, что NCAA требует, чтобы студенты-спортсмены указали свой статус серповидно-клеточных признаков до участия в межвузовских соревнованиях по легкой атлетике.
Для студенческих спортсменов доступны следующие варианты:
- Обратитесь в медицинскую карту в больнице, где вы родились, и запросите копию результатов обследования новорожденного. Возможно, у них уже нет результатов тестов.
- Обратитесь в клинику, где вы получали медицинскую помощь в младенчестве, чтобы узнать, есть ли у них копии результатов. Возможно, у них нет результатов тестирования.
- Запишитесь на прием, чтобы сдать анализ крови (электрофорез гемоглобина) у вашего основного лечащего врача или в студенческую службу здравоохранения.
- Обсудите варианты отказа с отделом легкой атлетики вашего колледжа.
Мы надеемся, что эта информация окажется для вас полезной, и желаем вам больших успехов в учебе! Если у вас есть дополнительные вопросы о тестировании серповидно-клеточных признаков, вы можете поговорить с одним из наших генетических консультантов по телефону 651-201-3548 или написать нам по адресу [email protected]
Дополнительная информация и ресурсы
Вопросы? Позвоните нашим генетическим консультантам по телефону 651-201-3548 или напишите в службу здравоохранения[email protected]
Скрининг новорожденных на гемоглобинопатии с использованием технологии капиллярного электрофореза: Тестирование устройства Capillarys® Neonat Fast Hb
Серповидно-клеточная анемия (SCD) и большая бета-талассемия (TM) являются двумя наиболее распространенными формами тяжелой гемоглобинопатии. Скрининг новорожденных (НБС) был введен в нескольких странах в качестве инструмента для предотвращения заболеваемости этими заболеваниями [1], [2], [3], [4], [5], [6], [7]. Анализ проводится либо на свежей пуповинной крови [8], собранной во время родов, либо на образцах периферической крови, обычно собираемых в течение первой недели после рождения, в основном с пятки и обычно выявляемых и транспортируемых в высушенном состоянии на фильтровальной бумаге (карточка Гатри) [7 ].
Пуповинная кровь может быть идеальным материалом для НБС, поскольку она отражает ситуацию при рождении, но ее следует собирать осторожно, чтобы избежать заражения матери. Периферическая кровь, собранная вскоре после рождения, не загрязнена материнской кровью, но переключение гемоглобина плода / взрослого (Hb) может влиять на уровни фракций Hb при измерениях в последующие дни. Более того, при слишком длительном хранении в сухом состоянии образец может частично разрушиться.
Предварительный диагноз у новорожденных исторически основывался на разделении фракций гемоглобина [9] либо на щелочном электрофорезе, либо на изоэлектрическом фокусировании (ИЭФ) [10].Сегодня высокоэффективная жидкостная хроматография (ВЭЖХ) [11] является современным методом, в то время как капиллярный электрофорез (КЭ) [12] является возможной альтернативой высокопроизводительному скринингу. В обоих случаях это базовое разделение гемоглобина, которое остается самой простой и наиболее прямой информативной технологией для идентификации пациентов и носителей.
В соответствии с местным законодательством, некоторые лаборатории используют ИЭФ в качестве первого метода скрининга, за которым следует предполагаемое подтверждение с помощью ВЭЖХ. И наоборот, другие используют исключительно ВЭЖХ и подтверждают результаты конкретно на молекулярном уровне и семейным анализом.Среди других специализированных устройств Capillarys 2 (Sebia) оказался отличным методом для анализа гемоглобинопатии [13], но его использование ограничивалось только свежей кровью. В связи с растущей тенденцией к проведению национальных NBS на сухой крови, недавно была представлена модификация Capillarys 2 (Capillarys Neonat Fast Hb, Sebia), специально разработанная для высокопроизводительного анализа свежих и сухих образцов крови. Мы представляем тестирование и валидацию этого устройства и даем несколько советов по тонкой настройке диагностического потенциала.
Система Capillarys Neonat Fast Hb основана на той же технологии, что и система Capillarys 2, но адаптирована для автоматического и быстрого отделения сухой крови новорожденных. Система снабжена полуавтоматической системой подготовки проб со штрих-кодом и использует 8 параллельно работающих капилляров, что позволяет проводить одновременный анализ большего количества проб. Фракции гемоглобина непосредственно и специфически обнаруживаются на длине волны 415 нм. Время для прогона 8 образцов составляет 7 минут, и можно заранее загрузить до 24 штативов для образцов (192 образца).
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Скрининг новорожденных на гемоглобинопатии с использованием капиллярного электрофореза
- P. C. Giordano
Первый онлайн:
- 1 Цитаты
- 1,3 км Загрузки
Abstract
В этой главе описаны основные элементы, необходимые для понимания базовой лабораторной диагностики, состоящей из разделения и измерения фракций гемоглобина.Несмотря на то, что базовая диагностика хорошо зарекомендовала себя, для ее применения и интерпретации требуются некоторый фон и некоторый опыт. Методы последнего поколения, состоящие из автоматических систем, таких как высокоэффективная жидкостная хроматография и капиллярный электрофорез (КЭ), позволяют проводить высокопроизводительный анализ у взрослых и новорожденных. Скрининг новорожденных с использованием КЭ представлен в некоторых деталях, на примере системы Capillarysâ Neonat Hb (Себия, Франция), в качестве будущей альтернативы, с объяснением метода, интерпретации результатов, целей, последующих действий, преимуществ, и подводные камни.
Ключевые слова
Гемоглобин Гемоглобинопатии Талассемия Серповидноклеточная болезнь Диагностика Лечение Профилактика Электрофорез ХроматографияЭто предварительный просмотр содержимого подписки,
войдите в систему, чтобы проверить доступ.
Примечания
Благодарности
Автор благодарит Элени Мантику за ее умелый вклад и заявляет об отсутствии конфликта интересов с производителями.
Ссылки
1.
Банн А.Ф., Забудьте Б.Г., Ранни Х.М. (1977) Гемоглобины человека. W.B. Saunders, Philadelphia
Google Scholar2.
van den Berg HM et al (1999) Hb Nijkerk: новая мутация в кодонах 138/139 гена бета-глобина, вызывающая тяжелую гемолитическую анемию у голландской девочки. Гемоглобин 23: 135–144
PubMedCrossRefGoogle Scholar3.
Weatherall DJ, Clegg JB (2001) Синдромы талассемии, 4-е изд. Wiley-Blackwell, Oxford
CrossRefGoogle Scholar4.
Harteveld CL et al (2003) Новая делеция дельтабета-талассемии 112 kb (epsilonGgammaAgamma) в голландской семье. Br J Haematol 122: 855–858
PubMedCrossRefGoogle Scholar5.
Harteveld CL et al (2008) Сегментарные дупликации с участием кластера генов альфа-глобина вызывают промежуточные фенотипы бета-талассемии у пациентов с гетерозиготной бета-талассемией. Клетки крови Mol Dis 40: 312–316
PubMedCrossRefGoogle Scholar6.
Sharma V et al (2009) Число генов альфа-глобина: важный модификатор HbE / бета-талассемии.Гематология 14: 297–300
PubMedCrossRefGoogle Scholar7.
Giardine B et al (2007) База данных HbVar вариантов гемоглобина человека и мутаций талассемии: обновление 2007 г. Hum Mutat 28: 206
PubMedCrossRefGoogle Scholar8.
Amato A et al (2009) Стратегии профилактики тяжелых гемоглобинопатий в эндемичных и неэндемичных иммиграционных странах: пример Latium. Prenat Diagn 29: 1171–1174
PubMedCrossRefGoogle Scholar9.
Giordano PC (2009) Начало неонатального скрининга на гемоглобинопатии в Нидерландах. J Clin Pathol 62: 18–21
PubMedCrossRefGoogle Scholar10.
Gulbis B et al (2009) Скрининг неонатальной гемоглобинопатии в Бельгии. J Clin Pathol 62: 49–52
PubMedCrossRefGoogle Scholar11.
Streetly A et al (2009) Внедрение универсального скрининга новорожденных на серповидно-клеточную анемию и другие клинически значимые гемоглобинопатии в Англии: результаты скрининга за 2005–2007 годы.J Clin Pathol 62: 26–30
PubMedCrossRefGoogle Scholar12.
Dickerhoff R, Genzel-Boroviczeny O, Kohne E (2009) Скрининг гемоглобинопатии и гемоглобинопатии новорожденных в Германии. J Clin Pathol 62:34
PubMedCrossRefGoogle Scholar13.
Michlitsch J et al (2009) Скрининг новорожденных на гемоглобинопатии в Калифорнии. Pediatr Blood Cancer 52: 486–490
PubMedCrossRefGoogle Scholar14.
Nasserullah Z et al (2003) Региональный опыт скрининга новорожденных на серповидно-клеточную анемию, другие гемоглобинопатии и дефицит G6PD.Ann Saudi Med 23: 354–357
PubMedGoogle Scholar15.
Giordano PC (2009) Проспективная и ретроспективная первичная профилактика гемоглобинопатий в полиэтнических обществах. Clin Biochem 42: 1757–1766
PubMedCrossRefGoogle Scholar16.
Van Delft P et al (2009) Оценка пяти специализированных автоматических устройств для диагностики гемоглобинопатии в многонациональных популяциях. Int J Lab Hematol 31: 484–495
PubMedCrossRefGoogle Scholar17.
Mosca A et al (2009) Роль тестирования гемоглобина A (2) в диагностике талассемии и родственных гемоглобинопатий. J Clin Pathol 62: 13–17
PubMedCrossRefGoogle Scholar18.
Gilman JG, Huisman TH, Abels J (1984) Голландская бета-0-талассемия: делеция ДНК размером 10 килобаз, связанная со значительным образованием гамма-цепи. Br J Haematol 56: 339–348
PubMedCrossRefGoogle Scholar19.
Mantikou E et al (2009) Краткий обзор методов скрининга новорожденных на гемоглобинопатии и предварительные результаты отбора носителей бета-талассемии при рождении путем количественной оценки HbA дробная часть.Clin Biochem 42: 1780–1785
PubMedCrossRefGoogle Scholar20.
Rugless MJ et al (2006) Hb Bart’s в пуповинной крови: точный индикатор альфа-талассемии. Гемоглобин 30: 57–62
PubMedCrossRefGoogle Scholar
Информация об авторских правах
© Springer Science + Business Media, LLC 2013
Авторы и аффилированные лица
- 1. Кафедра человеческой и клинической генетики Медицинский центр Лейденского университета Лейден, Нидерланды
Выполнимость и приемлемость скрининга детей раннего возраста на серповидно-клеточную анемию в Лагосе, Нигерия — пилотное исследование
Abstract
В Нигерии ежегодно рождается около 1 50000 детей с серповидно-клеточной анемией (ВСС), и, по оценкам, эта цифра увеличится на 100% к 2050 году без эффективных и устойчивых стратегий контроля.Несмотря на высокую распространенность, скрининг новорожденных на ВСС, позволяющий раннее профилактическое лечение, обучение родителей / опекунов и всестороннее лечение, пока недоступен. В этом исследовании изучалась стратегия скрининга детей раннего возраста во время первого и второго визитов иммунизации, определялась распространенность, осуществимость и приемлемость скрининга детей раннего возраста на ВСС и оценка диагностического теста HemoTypeSC по сравнению с высокоэффективной жидкостной хроматографией (ВЭЖХ). ) Золотой стандарт.Поперечное исследование было проведено в двух выбранных центрах первичной медико-санитарной помощи в районе местного самоуправления Сомолу (LGA) в Лагосе, Нигерия. Двести девяносто одна пара мать-младенец, пришедшая на первое или второе посещение иммунизации, была последовательно включена в исследование после письменного информированного согласия. Генотип гемоглобина в парах мать-младенец определяли с помощью набора для экспресс-тестов HemoTypeSC. Подтверждение генотипа гемоглобина у младенцев проводили с помощью ВЭЖХ. Данные были проанализированы с помощью SPSS версии 22.Также были рассчитаны валидность и прогностическая ценность экспресс-теста HemotypeSC. Скрининг младенцев на ВСС был приемлемым для 86% матерей, обратившихся в клиники иммунизации. Распространенность ВСС среди младенцев составила 0,8%. Младенцы с диагнозом ВСС были немедленно зарегистрированы в педиатрической клинике ВСС для лечения конкретного заболевания. Тест HemoTypeSC имел 100% чувствительность и специфичность для серповидно-клеточной анемии в раннем младенчестве по сравнению с ВЭЖХ. Это исследование подтверждает, что для матерей возможно и приемлемо реализовать программу скрининга ВСС в раннем младенчестве в штате Лагос.Исследование также демонстрирует полезность экспресс-тестирования HemotypeSC для облегчения и снижения стоимости скрининга младенцев на ВСС.
Образец цитирования: Олуволе Е.О., Адейемо Т.А., Осаньин Г.Е., Одукоя О.О., Канки П.Дж., Афолаби Б.Б. (2020) Возможность и приемлемость скрининга детей раннего возраста на серповидно-клеточную анемию в Лагосе, Нигерия — пилотное исследование. PLoS ONE 15 (12): e0242861. https://doi.org/10.1371/journal.pone.0242861
Редактор: Амбруаз Вонкам, Кейптаунский университет, ЮЖНАЯ АФРИКА
Поступила: 21 августа 2020 г .; Дата принятия: 11 ноября 2020 г .; Опубликовано: 3 декабря 2020 г.
Авторские права: © 2020 Oluwole et al.Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Все соответствующие данные находятся в рукописи и ее файлах с вспомогательной информацией.
Финансирование: EO Это исследование было поддержано Международным центром Фогарти Национальных институтов здравоохранения под номером гранта D43TW010134.Авторы несут полную ответственность за содержание, которое не обязательно отражает официальную точку зрения Национальных институтов здравоохранения. Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Авторы заявили, что никаких конкурирующих интересов не существует.
Введение
Серповидно-клеточная анемия (ВСС) — аутосомно-рецессивная генетически передающаяся гемоглобинопатия, ответственная за значительную заболеваемость и смертность [1, 2].Заболевание поражает эритроциты и характеризуется хронической гемолитической анемией с несколькими клиническими последствиями [3, 4]. Документально подтверждено, что 50–90% детей, рожденных с ВСС, не достигают пятилетнего возраста из-за отсутствия диагностики и комплексной помощи [5, 6]. Ожидается, что бремя ВСС в Африке к югу от Сахары увеличится до 88% случаев в мире к 2050 году, но, несмотря на высокую распространенность, программы скрининга новорожденных не являются широко доступными [7–9].
В 2006 г. Всемирная организация здравоохранения (ВОЗ) признала ВСС заболеванием, имеющим сильные глобальные последствия и имеющим огромное значение для общественного здравоохранения в Африке, при котором необходимо уделять больше внимания повышению общей выживаемости детей [10].Около 465 000 детей рождаются ежегодно со значительными нарушениями гемоглобина (Hb), из которых 401 000 являются SCD во всем мире [7].
В Нигерии распространенность серповидно-клеточной анемии составляет около 23,7%, в то время как частота серповидно-клеточной анемии составляет около 20 на 1000 рождений, в результате чего ежегодно рождается около 1 50000 детей с ВСС. Этот показатель относится к Нигерии, стране с самым большим бременем ВСС в мире, где поражено около 2,69–5% населения [11, 12]. Также предлагается увеличить этот показатель на 100% к 2050 году без эффективных и устойчивых стратегий борьбы [5, 7].
В настоящее время в Нигерии нет национальной политики неонатального скрининга для диагностики и лечения ВСС, большинство людей с ВСС выявляются, когда у них появляются симптомы, а диагноз подтверждается качественным электрофорезом, который чаще всего доступен в учебных больницах и обычно очень высок. дорого [13]. Разрушительные осложнения ВСС и отсутствие комплексной медицинской помощи в значительной степени способствуют заболеваемости и смертности людей с ВСС. Однако в странах с высоким уровнем доходов, где существует инфраструктура для всеобщего скрининга новорожденных, раннего вмешательства и комплексного ухода, смертность и заболеваемость ВСС снизились в течение первых 20 лет жизни, при этом глобальное бремя болезней составляет менее 1% и более 90%. новорожденных с ВСС доживают до взрослого возраста [5, 14, 15].
Ранний скрининг младенцев на ВСС позволяет в раннем возрасте начать профилактическое лечение, обучить родителей / опекунов и обеспечить комплексное лечение, ведущее к снижению смертности [11]. Были продемонстрированы доказательства множественных преимуществ универсального скрининга новорожденных на ВСС в регионах с высокой распространенностью [9, 16]. На Ямайке скрининг новорожденных на ВСС привел к улучшению результатов у пораженных детей, в то время как в Бразилии скрининг новорожденных на ВСС привел к тому, что к концу 2000 года в 36 муниципалитетах было обследовано около 300 000 детей [17, 18].
Скоординированный скрининг новорожденных на ВСС не проводился в Нигерии [11]. Некоторые из проблем, связанных с запуском программы для новорожденных в стране, включают: Текущий метод диагностики — это лабораторный электрофорез гемоглобина, изоэлектрическое фокусирование, высокоэффективная жидкостная хроматография (ВЭЖХ), масс-спектрометрия и молекулярные методы. Все это требует больших денег, специально обученного персонала и постоянного источника энергии, которые не всегда доступны. Кроме того, еще одной важной проблемой диагностики ВСС в Нигерии является использование электрофореза щелочного гемоглобина, который является наиболее распространенным методом диагностики с большим количеством ошибочных диагнозов генотипов гемоглобина (Hb) [19, 20].Следовательно, существует потребность в недорогих, надежных и простых в использовании устройствах для оказания медицинской помощи (POCT) с высокой чувствительностью и специфичностью при обнаружении генотипов Hb.
HemoTypeSC ™ (Silver Lake Research Corp., США) — это набор для тестирования на месте (POCT), предназначенный для диагностики in vitro медицинскими работниками для определения присутствия гемоглобина A, S и C в цельной крови. Он основан на конкурентном иммуноанализе с боковым потоком, включающем моноклональные антитела для определения присутствия гемоглобинов A, S и C, чтобы обеспечить быстрое определение генотипов гемоглобина HbAA, HbSS, HbSC, HbCC, HbAS и HbAC.HemoTypeSC имеет множество преимуществ, включая простоту использования, быстрое получение результатов и раннее уведомление пациентов с помощью необходимого консультирования. Его также можно использовать в удаленных местах с ранней диагностикой, что приводит к снижению смертности и заболеваемости из-за ВСС [19].
Многоцентровое исследование в Нигерии, в котором оценивали недорогое устройство POCT, HemoTypeSC, показало, что чувствительность и специфичность этого теста составили 93,4% и 99,9% соответственно [19]. Другое исследование, в котором проверялась возможность внедрения программы скрининга на серповидно-клеточную анемию с использованием инновационных устройств для тестирования на месте оказания медицинской помощи в существующие программы иммунизации в учреждениях первичной медико-санитарной помощи в Нигерии, сообщило о 100% чувствительности и специфичности теста HemotypeSC при обнаружении ВСС [ 21].Аналогичным образом, исследование скрининга на ВСС в местах оказания медицинской помощи в условиях ограниченных ресурсов сообщило о 100% чувствительности и специфичности для ВСС [22].
Была рекомендована важность проведения пилотных исследований по инициированию стратегических инициатив по информированию людей о преимуществах скрининга новорожденных (NBS) для успешной реализации программы NBS [23, 24]. Более того, несмотря на высокую распространенность ВСС в Нигерии, только 36% всех родов происходят в медицинских учреждениях [24], что затрудняет скрининг новорожденных.Мы разработали стратегии раннего скрининга во время первого или второго посещения иммунизации, когда младенцев доставляют в государственные центры первичной медико-санитарной помощи (ПМСП), расположенные в общинах. В этом исследовании была апробирована программа скрининга младенцев на ВСС во время посещений иммунизации в районе местного самоуправления (LGA) штата Лагос, Нигерия, чтобы определить осуществимость и приемлемость скрининга детей раннего возраста. Мы также определили распространенность SCD среди изученных младенцев и оценку диагностического теста HemoTypeSC по сравнению с золотым стандартом.
Материалы и методы
Место исследования
На Нигерию проживает около половины населения Западной Африки с приблизительно 202 миллионами человек. Это полиэтническая и культурно разнообразная федерация, которая состоит из 36 автономных государств и федеральной столичной территории (Абуджа) [25]. Уровень грамотности составляет 59,3 процента среди женщин и 79,9 процента среди мужчин в возрасте от 15 до 24 лет. Однако в северном регионе Нигерии этот показатель невысок [26]. В отчете Национального бюро статистики (НБС) за период с 2018 по октябрь 2019 года о бедности и неравенстве говорится, что 40% людей в Нигерии живут за чертой бедности, составляющей 137 430 найр (381 доллар США).75) в год, это составляет около 82,9 млн человек.
Система здравоохранения Нигерии состоит из первичной, вторичной и третичной медицинской помощи. Территории местного самоуправления (МСУ) несут ответственность за первичную медико-санитарную помощь, правительства штатов несут ответственность за оказание вторичной помощи, а федеральное правительство отвечает за разработку политики, регулирование, общее руководство и предоставление третичной помощи. Наличные расходы домохозяйств (НК) оставались основным источником, составляя около 70.3% от общих расходов на здравоохранение (THE) в 2009 году. Государственные расходы на здравоохранение в процентах от ВВП ниже среднего для стран Африки к югу от Сахары. По состоянию на конец 2013 года менее 5% нигерийцев были охвачены какой-либо формой медицинского страхования [27].
Штат Лагос находится в юго-западной геополитической зоне Нигерии и экономической столице Нигерии. Это исследование проводилось в одном (Сомолуский LGA) из двадцати районов местного самоуправления (LGA) [28] в штате Лагос. Сомолу (LGA) — космополитическое сообщество, состоящее из смеси нигерийских этнических групп, в которых преобладает этническая группа йоруба.По состоянию на 2015 год прогнозируемая численность населения составляет 1 361 100 человек, площадь 10,3 км 2 и плотность 132 190 человек / км 2 [29].
Популяция исследования, дизайн, определение размера выборки и отбор участников
Исследуемая популяция включала матерей и их младенцев в возрасте от 2 до 10 недель, посещающих клиники плановой иммунизации в двух выбранных из десяти центров первичной медико-санитарной помощи (ПМСП) LGA. Исследование было поперечным и описательным по дизайну.Участников набирали из числа матерей 18 лет и старше, давших письменное информированное согласие. Формула Кохрана для описательных исследований использовалась для расчета размера выборки (n = z 2 pq / d 2 ) [30] со стандартным нормальным отклонением при 95% доверительном интервале (1,96), предполагаемой распространенностью SCD. 3% [12] и погрешность точности 2,5% (0,025). Расчетный минимальный размер выборки составлял 179 участников на группу пар мать-младенец. Учитывая, что процент отсутствия ответов составляет 20%, был рассчитан размер выборки в 215 человек, но в конечном итоге для исследования была привлечена 291 согласившаяся пара.Все согласные матери младенцев, поступившие на первое или второе послеродовое посещение плановой иммунизации в период с августа 2019 года по январь 2020 года, были включены, в то время как матери младенцев, перенесших переливание крови с рождения, были исключены.
Этические соображения
Этическое одобрение для этого исследования было получено Комитетом по исследованиям и этике в области здравоохранения (HREC) Медицинского колледжа Университета Лагоса (CMUL / HREC / 03/19/503) . Письменное информированное согласие было получено от каждого респондента с гарантией конфиденциальности информации и их права отказаться от участия в исследовании в любой момент времени.Участников посоветовали понять, что участие в исследовании было добровольным. Исследователи обеспечили строгую конфиденциальность информации всех участников. Образцы крови были собраны и отправлены для подтверждения генотипа бесплатно для участников, и были предприняты усилия, чтобы минимизировать дискомфорт для участников во время сбора образцов крови.
Дотестовое консультирование и набор участников
Перед началом исследования было проведено обучение младших научных сотрудников, лаборантов и медсестер-консультантов.После исчерпывающего обзора литературы мы разработали опросный лист для достижения целей исследования и предварительно протестировали его среди пар мать-младенец в аналогичных, но отличных от места исследования условиях. Дотестовое консультирование проводилось для всех согласившихся матерей обученными медсестрами-консультантами, а информированное согласие на тестирование было получено от матери каждого ребенка перед тестированием. Затем был введен короткий вопросник для получения базовой демографической информации о парах мать-младенец и оценки приемлемости скрининга.
Процедуры испытаний
Пятьсот микролитров крови было собрано из пяточного укола каждого из младенцев обученными техниками в пробирку с ЭДТА-микроконтейнером, из которой были взяты 1-2 капли для HemoTypeSC, а у матери был взят образец пальца. Экспресс-тестирование HemoTypeSC TM было проведено сразу на месте после сбора образца. Затем образцы крови младенцев были доставлены в референс-лабораторию, где использовался подтверждающий метод ВЭЖХ.HemoTypeSC сравнивали с системой тестирования гемоглобина для высокоэффективной жидкостной хроматографии Bio-Rad D-10 ™ в качестве эталонного метода для определения точности HemoTypeSC при обнаружении генотипов Hb AA (нормальный), AS (признак HbS), AC (признак HbC), SS (серповидно-клеточная анемия), SC (серповидноклеточная анемия) и CC (гемоглобин C) в Справочной лаборатории гемоглобина в Sickle Cell Disease Foundation Nigeria (SCFN), Лагос, Нигерия.
Послетестовое консультирование и обратная связь с участниками
Результаты тестирования HemoTypeSC были сообщены всем матерям после сеанса послетестового консультирования в тот же день клиники, в то время как результаты подтверждающего теста были сообщены по телефону в течение одной недели при отсутствии противоречивых результатов.Матери и младенцы с подтвержденным диагнозом ВСС были приглашены обратно в клинику иммунизации для дальнейшего консультирования и сразу же были направлены на участие в программе педиатрической серповидно-клеточной анемии в Учебной больнице Университета Лагоса (LUTH).
Возможность раннего скрининга новорожденных на ВСС оценивалась по степени приемлемости> 80% среди участников, ≥ 90% готовности участников немедленно направить ребенка в клинику, если подтверждено наличие ВСС,> 60% готовности участников платить (США $ 1 · 50) для экспресс-теста,> 50% участников доступность стоимости (1,50 долларов США) для экспресс-теста и, по крайней мере, 80% детей с подтвержденной SCD, получивших результаты диагноза и получивших немедленную специализированную помощь.
Анализ данных
Данные были проанализированы с помощью статистического пакета для социальных наук (SPSS) версии 22. Был проведен описательный анализ; рассчитывалась доля младенцев с серповидно-клеточной анемией (HbSS), гетерозиготных по HbS и HbC (HbSC), с серповидно-клеточным признаком (HbAS), гетерозиготных по HbA и HbC (HbAC) и с нормальным гемоглобином (HbAA). Также были рассчитаны чувствительность, специфичность, положительная и отрицательная прогностическая ценность HemoTypeSC по сравнению с «золотым стандартом» ВЭЖХ.
Результаты
Социально-демографические характеристики пар мать-дитя
Двести девяносто одна (291) пара мать-ребенок участвовала в исследовании. Средний возраст матерей (± стандартное отклонение) составил 29,9 ± 5,4 года. Большинство (92%) матерей имели минимальное среднее образование, и большинство (82,2%) были трудоустроены. Двести сорок пять (84,2%) младенцев были 5 недель и старше [Таблица 1].
Осуществимость и приемлемость скрининга детей раннего возраста на ВСС
Сорок одна (14%) из 291 матери отказалась от скрининга своих младенцев, что составляет 86% приемлемости скрининга детей раннего возраста на ВСС в этом исследовании.Девяносто четыре (74,6%) из 126 матерей, отказавшихся от скрининга, знали свой генотип Hb, а 40 (35%) указали свой генотип Hb и генотип своих супругов как HbAA. Следовательно, они считали, что у них не может быть ребенка с ВСС. Большинство матерей (92%), согласившихся на обследование, сделали это, чтобы узнать свой генотип и генотип своих детей; 148 (59%) сделали это еще и потому, что просмотр был бесплатным. В то время как только 23% матерей заявили, что наиболее подходящее время для скрининга — вскоре после родов, около 36% считают, что наиболее подходящее время должно быть в пределах первого месяца рождения, в то время как почти все 283 (97.3%) заявили о своей готовности немедленно направить своих младенцев в клинику SCD, если после скрининга будет обнаружена SCD. Хотя большинство из них были готовы 243 (84%) и могли позволить себе 239 (82%), заплатить 540,00 фунтов стерлингов (1,50 доллара США) за быстрый скрининговый тест на ВСС, только 190 (65%) были готовы заплатить дополнительно 7000,00 фунтов стерлингов ( 20 долларов США), необходимых для подтверждающего тестирования, и только 143 (49%) могли позволить себе такие затраты. Предполагаемые проблемы для раннего скрининга детей в этом исследовании включали стоимость подтверждающего теста 190 (65%), доступность испытательного центра 155 (53%), возможную задержку или неполучение результата теста 149 (51%) и доступность для последующее наблюдение 148 (51%) среди других [Таблица 2].
Результаты испытаний
Двести пятьдесят младенцев прошли скрининг на SCD с помощью экспресс-полосок HemoTypeSC и системы высокоэффективной жидкостной хроматографии Bio-Rad D-10 ™ для определения гемоглобина. В целом, тесты HemoTypeSC выявили 185 (74,0%) HbAA, 53 (21,2%) HbAS, 9 (3,6%) HbAC, 1 (0,4%) HbSS, 1 (0,4%) HbCC и 1 (0,4%) HbSC. Таким образом, у 2 (0,8%) новорожденных была серповидно-клеточная анемия, а у 1 (0,4%) — болезнь HbC. Чувствительность, специфичность, положительные и отрицательные прогностические значения HemoTypeSC по сравнению с «золотым стандартом» ВЭЖХ были рассчитаны независимо.Достоверность и прогностическая точность скринингового теста HemoTypeSC рассчитывалась следующим образом [31];
Чувствительность означает способность экспресс-теста правильно определять положительные случаи ВСС:
Специфичность относится к способности экспресс-теста правильно идентифицировать отрицательные случаи ВСС:
Положительная прогностическая ценность (PPV) относится к вероятности того, что участник с положительным результатом действительно имеет SCD:
Отрицательная прогностическая ценность (NPV) относится к вероятности того, что участник с отрицательным результатом действительно не имеет SCD:
HemoTypeSC показал полностью согласованные результаты с ВЭЖХ с чувствительностью и специфичностью 100%.HemoTypeSC правильно идентифицировал каждый генотип HbSS и HbCC без ложноположительных результатов, демонстрируя чувствительность и специфичность 100% [Таблица 3]. Матери двух подтвержденных младенцев, которым был поставлен диагноз ВСС, были известными носителями аномального варианта гемоглобина (HbAS, HbAC). Обе матери и мать ребенка с Hb CC получили результаты диагностики, их проконсультировали и направили в педиатрическую клинику серповидно-клеточной анемии для оказания специальной помощи [Таблица 3].
Обсуждение
Это исследование продемонстрировало, что скрининг детей раннего возраста (≤10 недель) на ВСС с помощью тестирования на месте (POCT) в центрах первичной медико-санитарной помощи возможен.Она имеет потенциал для широкомасштабной реализации и может быть полностью интегрирована в Национальную программу иммунизации (НПИ) с небольшими дополнительными ресурсами.
Согласно оценкам, в развитых странах универсальная диагностика ВСС у новорожденных и младенцев снижает смертность у 94–99% детей с ВСС, большинство из которых доживают до взрослого возраста [15, 32, 33]. Скрининг новорожденных ведет к снижению заболеваемости и смертности за счет раннего выявления и начала оказания окончательной медицинской помощи, включая раннее начало профилактического лечения пенициллином, пневмококковую вакцинацию, консультирование родителей и другие меры по охране здоровья [34].В Нигерии из-за отсутствия скоординированной национальной универсальной программы скрининга новорожденных у детей с ВСС чаще всего диагностируют серповидно-клеточные осложнения. Хотя федеральное правительство Нигерии инициировало программу скрининга новорожденных (NBS) с созданием шести центров комплексного лечения в каждой из шести геополитических зон, усилия по внедрению всеобщего скрининга новорожденных не увенчались успехом, несмотря на значительные инвестиции со стороны правительства [23 , 35].
Распространенность SCD среди младенческих когорт в этом исследовании была равна 0.8%, в то время как носительство HbAS и HbAC составило 21,2% и 3,6% соответственно. Сто восемьдесят пять (74%) младенцев имели генотип гемоглобина как АА. Аналогичное исследование, проведенное в Абудже, Нигерия, показало распространенность 1,4% для HbSS, 20,5% для HbAS и HbAA 77% [21]. Другое аналогичное исследование, проведенное в Авка на юго-востоке Нигерии, показало распространенность 0,3% для HbSS и 75% для генотипа HbAA среди новорожденных [36]. Исследование, проведенное в Бенине, Южная Нигерия, выявило 75,3% HbAA, 20,6% HbAS, 1,1% HbAC, 2,8% HbSS и 0.2% HbSC [12]. Другое исследование, проведенное в Северной Нигерии, показало, что частота ВСС составляет 2,69% [5]. Результаты нашего исследования подтверждают результаты отчета DHS за 2018 год, в котором сообщалось о 20% HbAS, 1% HbSS и HbSC. Согласно данным демографического и медицинского обследования (DHS) 2008 г., разница в распространенности ВСС в зависимости от географического региона наиболее высока на Юго-Западе (2%), а наименьшая — на Юге-Юге (0,3%) [37].
Наше исследование показало высокую приемлемость раннего скрининга у 250 (86%) респондентов.Этот результат аналогичен результатам многоцентрового исследования приемлемости скрининга новорожденных на ВСС в Нигерии, в котором сообщается о 86,1% [35]. Аналогичным образом исследования в Юго-Западной и Северной Нигерии подтвердили приемлемость диагноза ВСС у новорожденных / младенцев [5, 12]. Более высокие показатели (99%) были зарегистрированы в исследовании, проведенном в Либерии [38], а исследование в Гане документально подтвердило, что скрининг и последующее наблюдение новорожденных на ВСС возможны в развивающихся странах Африки [39]. Эти результаты показывают, что внедрение универсального скрининга детей раннего возраста на ВСС, скорее всего, будет приемлемым в стране.
Все младенцы с диагнозом ВСС были немедленно включены в клинику ВСС для лечения конкретного заболевания в этом исследовании. Матери двух младенцев, которым в этом исследовании был поставлен диагноз ВСС, были известными носителями аномального варианта гемоглобина (HbAS, HbAC), но указали статус Hb у своих супругов как HbAA. Следовательно, они не ожидали, что у них будет ребенок с аномальным вариантом гемоглобина. Таким образом, универсальный скрининг детей раннего возраста, который позволяет диагностировать и начинать профилактическую терапию до появления симптомов, имеет первостепенное значение.
Это исследование демонстрирует возможность включения программы скрининга детей раннего возраста в обычные программы иммунизации в центрах первичной медико-санитарной помощи, которые будут способствовать доступности и устойчивости. Иммунизация как компонент первичной медико-санитарной помощи является устойчивой, и ее можно использовать для создания программы скрининга детей раннего возраста на ВСС. Подход, использованный в этом исследовании с ПМСП, по-видимому, способствовал выполнению программы скрининга.
Большинство матерей обращаются к услугам иммунизации своих младенцев в первичных, а не вторичных и третичных центрах, которые требуют более длительного времени ожидания и более высоких затрат [35]. Скрининговый тест на генотип Hb проводился вместе с плановой иммунизацией, а не как отдельная услуга. Сотрудники ПМСП были вовлечены в программу, что также снизило стоимость услуг. Большинство матерей, участвовавших в этом исследовании, проявили готовность платить за тест на месте оказания медицинской помощи, который был относительно дешевым (1 доллар США.5) по сравнению со стандартным методом испытаний (20 долларов США). Недорогой экспресс-тест в месте оказания медицинской помощи и другие факторы предполагают возможность скрининга детей раннего возраста на ВСС в Нигерии и других развивающихся странах. Кроме того, низкая стоимость скрининга, скорее всего, будет стимулировать покрытие страховыми схемами, что еще больше повысит доступность и устойчивость. Для осуществимой и устойчивой ранней диагностики ВСС и включения в политику программ помощи необходимо рассмотреть использование простых, доступных и подходящих технологий, которые могут применяться на уровне ПМСП, что принесет пользу широким слоям населения [19].
HemoTypeSC продемонстрировал 100% чувствительность и специфичность для обнаружения каждого из трех фенотипов Hb, HbA, HbS и HbC в нашем исследовании. Этот результат подтверждается другими задокументированными лабораторными отчетами, в которых сообщается о 100% чувствительности и специфичности для HbS и HbC в идеальных условиях [19, 22]. HemoTypeSC — это доступный, быстрый, надежный и точный диагностический тест для программ скрининга детей раннего возраста на ВСС в странах с ограниченными ресурсами, где распространенность ВСС высока без организованной национальной программы скрининга новорожденных [19].Аналогичное и более крупное исследование в Абудже, Нигерия, также сообщило о 100% чувствительности и специфичности HemoTypeSC и продемонстрировало надежность и точность тестов в месте оказания помощи при скрининге новорожденных на ВСС [21].
Стоимость подтверждающего теста, наличие испытательного центра, задержка с получением результата теста, наличие / доступность для последующего ухода, доступность результатов теста и время, затраченное на консультирование и тестирование, были среди проблем, которые матери воспринимали при раннем скрининге. .Подобные исследования в различных регионах документально подтвердили высокую стоимость, логистическую сложность традиционных методов диагностики и задержку получения результатов скрининга как ограничение для устойчивости скрининга новорожденных на ВСС в Африке к югу от Сахары и других регионах мира с ограниченными ресурсами [16, 40 , 41]. Исследование, проведенное в Нигерии, показало, что основными препятствиями на пути к скринингу новорожденных ВСС, скорее всего, были финансовые и практические, а не социальные или культурные факторы [35].
Проблемы, заявленные участниками нашего исследования, были смягчены высокой чувствительностью и специфичностью, а также низкой стоимостью POCT, быстрым результатом и легким доступом к учреждению первичной медико-санитарной помощи.Таким образом, мы рекомендуем организовать регулярную базовую медицинскую помощь по ВСС в ПМСП, ежегодную оценку на уровне учреждений вторичной медицинской помощи и только комплексную и сложную помощь в центрах третичной медицинской помощи.
Заключение
Результаты этого исследования показали осуществимость и приемлемость раннего скрининга новорожденных на ВСС с использованием простой, доступной и подходящей технологии, которая может быть адаптирована на уровне сообщества для обеспечения ранней диагностики и быстрого направления к врачу для снижения бремени ВСС в Нигерии. .Это исследование также продемонстрировало, что HemoTypeSC — доступный, быстрый и точный диагностический тест для программ скрининга детей раннего возраста на ВСС в ПМСП в развивающихся странах. Следовательно, правительствам необходимо обеспечить низкую стоимость, равноправие и способствовать доступу к раннему скринингу и диагностике ВСС в сообществе.
Благодарности
Авторы выражают признательность участникам, медицинскому работнику (МЗ) LGA, Аджоке Ойетунджи из SCFN и всей исследовательской группе.
Ссылки
- 1. Афолаян Дж.А., Джолайми Ф.Т. Отношение родителей к детям с серповидноклеточной болезнью в отдельных медицинских учреждениях местного самоуправления Иреподуна, штат Квара, Нигерия. Этно Мед. 2011; 5 (1): 33–40
- 2. Bazuaye GN, и Olayemi EE. Знания и отношение учащихся старших классов средней школы в Бенин-Сити, Нигерия, к серповидно-клеточной болезни. Всемирный журнал медицинских наук. 2009; 4 (1): 46–49.
- 3. Gamit CL, Kanthariya SL, Gamit S, Patni M, Parmar GB, Kaptan KR.Изучение знаний, отношения и практики в отношении серповидно-клеточной анемии у пациентов с положительным серповидно-клеточным статусом в Бардоли Талука. Int J Med Sci Public Health. 2014; 3: 365–368.
- 4. Угву Н.И. Серповидно-клеточная анемия: осведомленность, знания и отношение студентов бакалавриата нигерийского высшего учебного заведения. Азиатский журнал медицинских наук, 2016; 7 (5): 87–92
- 5. Инуса Б.П., Дэниел Й., Лоусон Дж.О., Дада Дж., Мэтьюз К.Э., Сухлин С.М. и др.Скрининг серповидноклеточной болезни в Северной Нигерии: сосуществование-талассемии в педиатрии и терапии. 2015; 5 (3): 3–6.
- 6. Макани Дж., Уильямс Т.Н., Марш К. Серповидно-клеточная анемия в Африке: бремя и приоритеты исследований. Ann Trop Med Parasitol. 2007; 10 (1): 3–14. pmid: 17244405
- 7. Piel FB, Hay SI, Gupta S, Weatherall DJ, Williams TN. Глобальное бремя серповидноклеточной анемии у детей в возрасте до пяти лет, 2010–2050 гг .: моделирование на основе демографических данных, избыточной смертности и вмешательств.PLoS Med. 2013; (10: e1001484). pmid: 23874164
- 8. Рис, округ Колумбия, Уильямс TN, Гладвин MT. Серповидно-клеточная анемия. Ланцет. 2010; 376: 2018–31. pmid: 21131035
- 9. Hsu L, Nnodu OE, Brown BJ, Tluway F, King S, Dogara LG и др. Белая книга: Пути к прогрессу в скрининге новорожденных на серповидноклеточную болезнь в Африке к югу от Сахары. J Trop Dis.2018; 6: 260. pmid: 30505949
- 10. Серповидно-клеточная анемия. Пункт повестки дня 11.4. 59-я сессия Всемирной ассамблеи здравоохранения WHA 59.20, 2006. http://apps.who.int/gb/ebwha/pdf_files/WHA59-REC1/e/WHA59_2006_REC1-en.pdf.
- 11. Omotade OO, Kayode CM, Falade SL, Ikpeme S, Adeyemo AA, Akinkugbe FM. Регулярный скрининг серповидноклеточной гемоглобинопатии с помощью электрофореза в детской клинике. West Afr J Med. 1998. 17 (2): 91–94. pmid: 9715113.
- 12. Одунвбун М.Э., Около А.А., Рахими СМ. Скрининг новорожденных на серповидноклеточную анемию в нигерийской больнице. Здравоохранение. 2008. 122 (10): 1111–6. pmid: 18486954
- 13.Оджевунми О.О., Адейемо Т.А., Айинде О.К., Ивалокун Б., Адекиле А. Текущие перспективы серповидно-клеточной анемии в Нигерии: изменение представлений Современные перспективы серповидно-клеточной анемии в Нигерии: изменение повествования. Эксперт Рев Гематол. 2019; 12 (8): 609–20. pmid: 31195888
- 14. Гарднер К., Дуири А., Драсар Э., Оллман М., Мвириги А., Авогбаде М. Выживание взрослых с серповидно-клеточной анемией в условиях высокого дохода. Кровь. 2016; 128 (10): 1436–1438. pmid: 27439910
- 15.Куинн СТ, Роджерс З.Р., Маккавит Т.Л., Бьюкенен Г.Р. Повышение выживаемости детей и подростков с серповидно-клеточной анемией. Кровь. 2010. 115 (17): 3447–3452. pmid: 20194891
- 16. Грин Н.С., Матур С., Кигули С., Макани Дж., Фашакин В., ЛаРусса П. и др. Соображения семьи, сообщества и системы здравоохранения для снижения бремени серповидно-клеточной анемии у детей в Уганде посредством скрининга новорожденных. Глоб Педиатр Здоровье. 2016; 3: 2333794X16637767.
- 17. Кинг Л., Найт-Мэдден Дж., Рид М.Скрининг новорожденных на серповидноклеточную анемию на Ямайке: обзор — прошлое, настоящее и будущее. West Indian Med J. 2014; 63 (2): 147–50. pmid: 25303249
- 18. Бранделиз С., Пинейру В., Габетта С.С., Хэмблтон I, Сержант Б., Сержант Г. Скрининг новорожденных на серповидноклеточную анемию в Бразилии: опыт Кампинаса. Clin Lab Haematol. 2004. 26 (1): 15–9. pmid: 14738432
- 19. Nnodu O, Isa H, Nwegbu M, Ohiaeri C, Adegoke S. HemoTypeSC, недорогое устройство для тестирования серповидноклеточной анемии в местах оказания медицинской помощи: перспективы и проблемы.Молекулы клеток крови и болезни. 2019; 78: 22–8. pmid: 30773433
- 20. Обаро С.К., Дэниел Й., Лоусон Дж. О. и др. Серповидно-клеточная анемия у детей Нигерии: знания родителей и результаты лабораторных исследований. Геномика общественного здравоохранения. 2016; 19 (2): 102–107. pmid: 26991896
- 21. Nnodu OE, Sopekan A, Nnebe-agumadu U, Ohiaeri C, Adeniran A, Shedul G, et al. Осуществление скрининга новорожденных на серповидно-клеточную анемию в рамках программ иммунизации в Нигерии: технико-экономическое обоснование.Lancet Haematol. 2020; 7 (7): e534–40. Доступен по телефону: pmid: 32589979
- 22. Стил С., Сински А., Асибей Дж., Элана Дж., Бреннан С., Одаме I и др. Скрининг на наличие серповидно-клеточной анемии в условиях ограниченных ресурсов: многоцентровая оценка HemoTypeSC, нового экспресс-теста. Am J Hematol. 2019; 94: 39–45. pmid: 302
- 23. МакГанн П.Т., Феррис М.Г., Рамамурти Ю., Сантос Б., Бернадино Л. и др. A. Перспективная программа скрининга новорожденных и лечения серповидно-клеточной анемии в Луанде, Ангола.Am J Hematol. 2013. 88 (12): 984–989. pmid: 24038490
- 24. Национальная комиссия по народонаселению 2013. Macro IC. Обзор демографии и здравоохранения Нигерии, Абуджа: 2013 г .;
- 25. Всемирный банк в Нигерии: обзор. www.worldbank.org> nigeria (по состоянию на 2 октября 2020 г.)
- 26. Национальное бюро статистики — Нигерия: Нигерия — Кластерное обследование по множественным показателям / национальные обследования охвата иммунизацией 2016-17 гг., Пятый раунд (MICS) и NICS (третий раунд).www.unicef.org> nigeria (по состоянию на 2 октября 2020 г.)
- 27. Отчет об исследовании рынка здравоохранения Нигерии, 2015 г. Исследование проведено по заказу Посольства Королевства Нидерландов в Нигерии. Фонд доступа к фарм. www.rvo.nl> default (по состоянию на 2 октября 2020 г.)
- 28. Правительство LS. О Лагосе 2019 [по состоянию на 18 апреля 2020 г.]. Доступно по адресу: https://lagosstate.gov.ng.
- 29. Район местного самоуправления Шомолу, Лагос, Нигерия. Национальная комиссия по народонаселению Нигерии.2015 г., Статистическое бюро Лагоса (веб-сайт). https://www.Citypopulation.de [цитируется 18 апреля 2020 г.].
- 30. Лванга С.К., Лемешоу С. Определение размера выборки в исследованиях здоровья: практическое руководство. Женева; Всемирная организация здравоохранения. 1991. https://apps.who.int/iris/handle/10665/40062
- 31. Парк К., Учебник Парка по профилактической и социальной медицине., 21-е изд. Джабалпур: Издательство BaPark K.narsidas Bhanot, 2011.
- 32. Couque N, Girard D, Ducrocq R, Haouari Z, Holvoet L, Odievre M-H и др.Улучшение медицинской помощи когорте новорожденных с серповидно-клеточной анемией в Северном Париже: влияние национальных руководств. Br J Haematol. 2016; 173 (6): 927–937. pmid: 27062606
- 33. Telfer PT, Coen PG, Chakravorty S, Wilkey OB, Evans J, Newell H, et al. Клинические результаты у детей с серповидно-клеточной анемией, проживающих в Англии: когорта новорожденных в Восточном Лондоне. Haematologica. 2007. 92 (7): 905–912. pmid: 17606440
- 34. де Монталамбер М. Современные стратегии ведения детей с серповидно-клеточной анемией.Эксперт Рев Гематол. 2009. 2 ((4)): 455–463. pmid: 21082949
- 35. Nnodu OE, Adegoke SA, Ezenwosu OU, Emodi II, Ngozi I, Ohiaeri CN и др. Многоцентровое исследование приемлемости скрининга новорожденных на серповидноклеточную болезнь в Нигерии. 2018; 10 (3). pmid: 32181059
- 36. Ejiofor OS, Efobi C, Emechebe GO, Ifezulike CC, Okeke KN, Mokebe TC и др. Скрининг новорожденных на серповидноклеточную болезнь (ВСС) в Авка на юго-востоке Нигерии. J Переливание крови Disord Transfus. 2018; 9 (2): 398.
- 37. Национальная комиссия по народонаселению Нигерии. Обзор демографии и здравоохранения Нигерии, 2018 г. Абуджа: Национальная комиссия по народонаселению, 2019 г.
- 38. Табман В.Н., Маршалл Р., Джаллах В., Го Д., Ма К., Охене-Фремпонг К. и др. Скрининг новорожденных на серповидноклеточную болезнь в Либерии: пилотное исследование. Педиатр Рак крови. 2016; 63 (4): 671–676. pmid: 26739520
- 39. Охене-Фремпонг К., Одуро Дж., Теттех Х., Нкрума Ф. Скрининг новорожденных на серповидноклеточную болезнь в Гане.Педиатрия. 2008; 121: S120. 2
- 40. Piety NZ, George A, Serrano S, Lanzi MR, Patel PR, Noli MP et al. Бумажный тест для скрининга новорожденных на серповидноклеточную болезнь. Sci. Rep.2017; 7, 45488; pmid: 28367971
- 41. Одаме I. Перспектива: Нам нужно глобальное решение. Природа. 2014; 515 (7526): S10. pmid: 253
ASCP — Повторный электрофорез гемоглобина
Просмотреть все рекомендации этого общества19 октября 2017 г.
Не повторяйте электрофорез гемоглобина (или его аналог) у пациентов, у которых есть предыдущий результат и которым не требуется терапевтическое вмешательство или мониторинг уровней вариантов гемоглобина.
Рекомендуется проводить скрининг с помощью электрофореза гемоглобина до зачатия и во время беременности, особенно в районах с высокой распространенностью серповидноклеточной анемии или талассемии, и он стал рутинной практикой для выявления аномалий гемоглобинов S, C, D-Пенджаб, E, О-Араб, Лепор, признак бета-талассемии, признак дельта / бета талассемии, признак альфа-талассемии (делеция 2 цепей) и наследственная персистенция гемоглобина плода (HPFH). Тестирование партнера должно быть предложено, когда есть риск значительной гемоглобинопатии у младенца.Повторный анализ электрофореза гемоглобина требуется только для постановки более точного диагноза или мониторинга результатов интервенционной терапии у пациентов с известными гемоглобинопатиями. Медицинские работники должны изучить предыдущие результаты, прежде чем запрашивать повторный электрофорез гемоглобина.
Эти предметы предоставляются исключительно в информационных целях и не предназначены для замены консультации с медицинским работником.Пациентам с любыми конкретными вопросами по пунктам этого списка или их индивидуальной ситуации следует проконсультироваться со своим врачом.
1-5: Список Американского общества клинической патологии (ASCP) был разработан под руководством председателя Консультативного комитета Института ASCP и бывшего президента ASCP. В этот процесс были включены эксперты по предметам и использованию тестов в области патологии и лабораторной медицины для получения их знаний и рекомендаций.Экспертная группа рассмотрела сотни вариантов, основанных как на практике патологии, так и на доказательствах, доступных в обширном обзоре литературы. Лабораторные тесты, указанные в наших рекомендациях, были выбраны потому, что они часто проводятся; есть свидетельства того, что тест либо не приносит пользы, либо вреден; использование теста является дорогостоящим и не обеспечивает более качественного лечения; и его устранение или переход на другой тест находится под контролем клинициста.Окончательный список не является исчерпывающим (были также определены многие другие тесты / процедуры, которые также заслуживают рассмотрения), но рекомендации, если они будут введены, приведут к более качественному уходу, снижению затрат и более эффективному использованию наших лабораторных ресурсов и персонала. .
6–15: Список рекомендаций Американского общества клинической патологии (ASCP) был разработан под руководством Специального комитета ASCP «Выбор разумного». Этот комитет, возглавляемый бывшим президентом ASCP, состоит из экспертов по предметам и тестированию в областях патологии и лабораторной медицины.Комитет рассмотрел первоначальный список возможных рекомендаций, составленный в результате опроса, проведенного среди членов Общества, работающих во многих комиссиях, комитетах и советах ASCP. Лабораторные тесты, указанные в наших рекомендациях, были выбраны потому, что они часто проводятся; есть свидетельства того, что тест либо не приносит пользы, либо вреден; использование теста является дорогостоящим и не обеспечивает более качественного лечения; и
отмена этого теста или переход на другой тест находится под контролем клинициста.Выполнение этих рекомендаций приведет к более качественному уходу, снижению затрат и более эффективному использованию наших лабораторных ресурсов и персонала.
16-35 Список рекомендаций Американского общества клинической патологии (ASCP) был разработан под руководством Руководящего комитета ASCP по эффективному использованию тестов. Этот комитет, возглавляемый бывшим президентом ASCP, состоит из экспертов по предметам и использованию тестов в областях патологии и лабораторной медицины.Комитет рассмотрел список возможных рекомендаций, составленный в результате опроса, проведенного среди членов Общества, работающих во многих комиссиях, комитетах и советах ASCP. Кроме того, недавно сформированному Консультативному совету ASCP было сделано объявление о внесении предложений по возможным рекомендациям по привлечению членов. Лабораторные тесты, указанные в наших рекомендациях, были выбраны потому, что они часто проводятся; есть свидетельства того, что тест либо не приносит пользы, либо вреден; использование теста является дорогостоящим и не обеспечивает более качественного лечения; и его устранение или переход на другой тест находится под контролем клинициста.Выполнение этих рекомендаций приведет к более качественному уходу, снижению затрат и более эффективному использованию наших лабораторных ресурсов и персонала.
С политикой раскрытия информации и конфликтов интересовASCP можно ознакомиться на сайте www.ascp.org.
Департамент здравоохранения и социальных служб штата Мичиган. Интерпретация результатов скрининга гемоглобина новорожденных. [Интернет]. Лансинг (Мичиган): Департамент здравоохранения и социальных служб штата Мичиган.2015. [цитируется 14 июля 2017 г.]. Доступно по адресу: http://www.michigan.gov/documents/mdch/Interpretation_of_Newborn_Hemoglobin_Screening_Results_Sep2013_438936_7.pdf
Центры по контролю и профилактике заболеваний, Ассоциация лабораторий общественного здравоохранения. Гемоглобинопатии: текущая практика скрининга, подтверждения и последующего наблюдения. [Интернет]. Сильвер-Спринг (Мэриленд): Центры по контролю и профилактике заболеваний, Ассоциация лабораторий общественного здравоохранения. 2015. [цитируется 14 июля 2017 г.]. Доступно по адресу: https: // www.cdc.gov/ncbddd/sicklecell/documents/nbs_hemoglobinopathy-testing_122015.pdf
переулок ПА. Скрининг новорожденных на нарушения гемоглобина. [Интернет]. 2001. [цитировано 14 июля 2017 г.]. Доступно по адресу https://sickle.bwh.harvard.edu/screening.html
Райан К., Бейн Б.Дж., Уортингтон Д., Джеймс Дж., Плевс Д., Мейсон А., Ропер Д., Рис, округ Колумбия, Де ла Салле Б., Стритли А. Значительные гемоглобинопатии: рекомендации по скринингу и диагностике. Британский журнал гематологии, [Интернет]. 2010 январь [цитируется 14 июля 2017 года]; 149, 35–49
Скрининг на серповидно-клеточную анемию и талассемию
Серповидно-клеточная анемия (ВСС) и талассемия являются наследственными заболеваниями крови.
Если вы являетесь носителем гена серповидной клетки или талассемии, вы можете передать эти заболевания своему ребенку.
Всем беременным женщинам в Англии предлагается сдать кровь на анализ, чтобы выяснить, несут ли они ген талассемии.
Тем, кто подвержен высокому риску быть носителем серповидных клеток, предлагается пройти тест на серповидноклеточные клетки.
Если выясняется, что мать является носителем, отцу также предлагается обследование.
Этот тест следует предложить до 10 недели беременности.Важно, чтобы тест был проведен заранее.
Если вы узнаете, что вы носитель, вы и ваш партнер сможете пройти дополнительные тесты, чтобы узнать, пострадает ли ваш ребенок.
О серповидно-клеточной анемии и талассемии
Серповидно-клеточная анемия и талассемия влияют на гемоглобин, часть крови, которая переносит кислород по всему телу.
Люди с такими заболеваниями нуждаются в специализированной помощи на протяжении всей жизни.
Люди с серповидно-клеточной анемией:
- могут иметь приступы очень сильной боли
- могут получить серьезные опасные для жизни инфекции
- обычно страдают анемией (их организм плохо переносит кислород)
Младенцы с серповидно-клеточной анемией могут заболеть рано лечение, включая вакцинацию и антибиотики.
Это, наряду с поддержкой родителей, поможет предотвратить серьезные заболевания и позволит ребенку вести более здоровый образ жизни.
Узнайте больше о серповидно-клеточной анемии
Люди с талассемией очень анемичны и нуждаются в переливании крови каждые 2–5 недель, а также в инъекциях и лекарствах на протяжении всей жизни.
Узнайте больше о талассемии
Существуют также другие менее распространенные и менее серьезные нарушения гемоглобина, которые можно обнаружить при скрининге.
Почему мне могут предложить скрининг на серповидноклеточную анестезию и талассемию на ранних сроках беременности?
Скрининг предлагается, чтобы выяснить, являетесь ли вы носителем гена серповидноклеточной анемии или талассемии и, следовательно, можете ли вы передать его своему ребенку.
Гены — это коды в нашем организме для таких вещей, как цвет глаз и группа крови.
Гены работают парами: на все, что мы наследуем, мы получаем 1 ген от матери и 1 ген от отца.
Люди болеют серповидно-клеточной анемией или талассемией только в том случае, если они наследуют 2 необычных гена гемоглобина: 1 от матери и 1 от отца.
Люди, унаследовавшие только 1 необычный ген, известны как носители или как имеющие признак.
Носители здоровы и не болеют.
Носители серповидных клеток могут испытывать некоторые проблемы в ситуациях, когда их организм может не получать достаточно кислорода, например, при общей анестезии.
Все носители могут передать необычный ген своим детям.
Когда оба родителя являются носителямиКогда оба родителя являются носителями, каждый раз, когда они ждут ребенка, существует:
- шанс 1 из 4, что ребенок не болен или не является носителем болезни
- 2 из 4 вероятность того, что ребенок будет носителем
- , вероятность того, что ребенок заболеет, 1 из 4
Любой человек может быть носителем гемоглобиновой болезни.Но это чаще встречается у людей, чьи предки были из Африки, Карибского бассейна, Средиземноморья, Индии, Пакистана, Южной и Юго-Восточной Азии и Ближнего Востока.
Узнайте больше о носителях серповидноклеточной анемии или талассемии.
Что включает в себя отборочный тест?
При скрининге на серповидноклеточные клетки и талассемию проводится анализ крови. Лучше всего сдать анализ до 10 недели беременности.
Это связано с тем, что у вас будет возможность пройти больше тестов, чтобы выяснить, пострадает ли ваш ребенок, если этот первый тест покажет, что вы являетесь носителем заболевания крови.
Пройдя тест раньше, вы и ваш партнер сможете узнать обо всех возможных вариантах и принять осознанное решение, если ваш ребенок подвержен риску унаследовать заболевание крови.
Всем беременным женщинам предлагается пройти тест на талассемию, но не всем женщинам автоматически предлагается тест на серповидноклеток.
В регионах, где гемоглобиновые заболевания более распространены, всем женщинам автоматически будет предложен анализ крови на серповидноклеток.
В регионах, где гемоглобиновые заболевания менее распространены, опросник используется для определения происхождения вашей семьи и происхождения отца ребенка.
Если анкета показывает, что вы или отец ребенка рискуете стать носителем серповидных клеток, вам будет предложен скрининговый тест.
Вы можете попросить пройти тест, даже если происхождение вашей семьи не предполагает, что у ребенка будет высокий риск гемоглобиновой болезни.
Может ли этот скрининг навредить мне или моему ребенку?Нет, скрининговый тест не может нанести вред ни вам, ни вашему ребенку, но важно хорошо подумать о том, проходить ли этот тест или нет.
Он может предоставить информацию, которая может означать, что вам придется принимать дальнейшие важные решения.
Например, вам могут предложить дополнительные анализы, при которых существует риск выкидыша.
Обязательно ли мне проходить этот скрининговый тест?
Нет, скрининговый тест проходить не нужно.
Некоторые люди хотят узнать, страдает ли их ребенок серповидно-клеточной анемией или талассемией, а другие нет.
Получение результатов скрининга
Тест покажет вам, носитель вы или нет, или болеете ли вы сами.
Вы получите результат анализа крови в течение недели. Человек, проводящий тест, обсудит порядок предоставления вам результатов.
Если вы окажетесь носителем серповидноклеточной анемии или талассемии, с вами свяжется медсестра-специалист или акушерка для консультации по генетическим вопросам.
Дальнейшие тесты, является ли мать носителем
Проверяет, является ли отец носителемЕсли скрининговый тест обнаруживает, что вы носитель гемоглобиновой болезни, отцу вашего ребенка также предложат анализ крови .
Если анализы покажут, что отец не является носителем, у вашего ребенка не будет серповидно-клеточной анемии или талассемии, и вам не будут предлагать дальнейшие тесты во время беременности.
Но есть шанс 1 из 2, что ваш ребенок может быть носителем и передать необычный ген своим детям.
Вы можете обсудить последствия того, что вы или ваш ребенок являетесь носителем, со своим терапевтом или медицинским работником в вашем местном центре серповидноклеток и талассемии.
Узнайте больше о скрининге для отцов
Обследования, когда оба родителя являются носителямиЕсли тесты показывают, что отец вашего ребенка также является носителем, вероятность того, что ваш ребенок может заболеть, составляет 1 из 4.
Вам будут предложены дополнительные тесты, называемые диагностическими тестами, чтобы выяснить, затронут ли ваш ребенок.
Диагностический тест скажет вам:
- , если у вашего ребенка серповидно-клеточная анемия, талассемия или другое нарушение гемоглобина
- , если ваш ребенок является носителем
- , если ваш ребенок полностью не поражен
Если отец ребенка нет доступны и вы были идентифицированы как носитель, вам будет предложен диагностический тест.
Примерно 1 из 100 диагностических тестов приводит к выкидышу.Вам решать, проходить диагностический тест или нет.
Это может быть очень трудное время, если вам говорят, что вы рискуете зачать ребенка с серповидно-клеточной анемией или большой талассемией. Поговорите со своей акушеркой, медсестрой-специалистом или врачом о возможных вариантах.
Вы также можете получить информацию и поддержку от благотворительной организации Antenatal Results and Choices (ARC).
У ARC есть телефон доверия, по которому вы можете позвонить для получения информации и поддержки по телефону 0845077 2290 или 020 7713 7486 с мобильного телефона.
Есть 2 типа диагностических тестов.
Взятие пробы ворсин хориона (CVS)Обычно это делается на сроке от 11 до 14 недель беременности.
Тонкая игла, которую обычно вводят в животик матери, используется для взятия крошечного образца ткани из плаценты.
Клетки ткани можно проверить на серповидно-клеточную анестезию или талассемию.
Узнайте больше о CVS
АмниоцентезЭто делается с 15 недели беременности.
Тонкая игла вводится через животик матери в матку, чтобы взять небольшой образец жидкости, окружающей ребенка.
Жидкость содержит некоторые клетки ребенка, которые можно проверить на серповидно-клеточную анестезию или талассемию.
Подробнее об амниоцентезе
Если вы обнаружите, что у вашего ребенка серповидно-клеточная анемия или талассемия
Если результат покажет, что у вашего ребенка серповидно-клеточная анемия или талассемия, вам будет предложен прием к врачу.
Вы сможете получить информацию о конкретном заболевании крови, унаследованном ребенком, и обсудить свой выбор.
Некоторые заболевания крови более серьезны, чем другие. Некоторые женщины решают продолжить беременность, в то время как другие решают, что они не хотят продолжать беременность, и делают прерывание (аборт).
Если вы столкнулись с этим выбором, вы получите профессиональную поддержку, которая поможет вам принять решение.
Поддержка родителей также предоставляется благотворительной организацией Antenatal Results and Choices (ARC).
Если тест показывает, что вы носитель, есть вероятность, что другие члены вашей семьи также могут быть носителями.
Вы можете предложить им пройти тест, особенно если они планируют беременность.
Узнайте больше о том, нашли ли что-то дородовые скрининговые тесты
Что, если я решу не проходить обследование?
Если вы решите не проходить скрининговый тест во время беременности, ваш ребенок все равно может пройти скрининг на серповидноклеточную анемию в рамках скрининга пятен крови новорожденного через несколько дней после рождения.
Может ли кто-нибудь пройти тест на серповидноклеток и талассемию?
Несмотря на то, что тестирование на серповидно-клеточную анемию и талассемию предлагается только во время беременности, любой может попросить своего терапевта или местного центра серповидно-клеточной анемии и талассемии бесплатно пройти тест в любое время.
Если вы или ваш партнер обеспокоены тем, что вы можете быть носителем, возможно, потому, что кто-то в вашей семье страдает заболеванием крови или является носителем, рекомендуется пройти обследование до того, как вы создадите семью.
Таким образом вы сможете понять свой риск передачи заболевания крови любым своим детям и обсудить варианты здоровой беременности со своим терапевтом или другим медицинским работником.
Как узнать, что вы носитель
Если анализ покажет, что вы носитель серповидноклеточной анемии, талассемии или другого варианта гемоглобина, с вами свяжется медсестра-специалист или акушерка для генетического консультирования.
Вы получите конкретный результат носительства в зависимости от унаследованного вами необычного гена гемоглобина.
Вы можете найти более подробную информацию о различных типах носителей в этих брошюрах:
Носитель серповидных клеток
Носитель бета-талассемии
Носитель дельта-бета-талассемии
Гемоглобин O Арабский носитель
Гемоглобин C-носитель
Гемоглобин D-носитель
Гемоглобин E-носитель
Гемоглобин E-носитель
Гемоглобин E-носитель Гемоглобин Лепор-носитель
Есть вероятность, что другие члены вашей семьи тоже могут быть носителями.
Вы можете предложить им пройти тест, особенно если они планируют беременность.
Они могут попросить своего терапевта или местного центра серповидноклеток и талассемии бесплатно пройти тест в любое время.
Что делать, если я забеременею и я или мой партнер являюсь носителем?
Если 1 родитель является носителемЕсли вы знаете, что ваш или ваш партнер является носителем серповидноклеточной анемии или талассемии, другой родитель должен как можно скорее пройти обследование, если вы хотите понять риск наследственности вашего ребенка. одно из этих заболеваний крови, чтобы вы могли узнать обо всех возможных вариантах.
Если оба родителя являются носителямиЕсли вы беременны и уже знаете, что и вы, и ваш партнер являются носителями (например, потому что вы узнали об этом во время предыдущей беременности), поговорите со своим терапевтом или акушеркой, как только возможный.
После этого вам будет предложено пройти диагностический тест, чтобы узнать, заболел ли ваш ребенок.
Узнайте больше о носителях серповидноклеточной анемии или талассемии.
Информация о вас
Если похоже, что вы или ваш ребенок страдаете серповидно-клеточной анемией или талассемией, эта информация будет передана в Национальную службу регистрации врожденных аномалий и редких заболеваний (NCARDRS).
Это помогает программе NHS по скринингу на серповидноклеточные клетки и талассемию улучшить услуги скрининга.

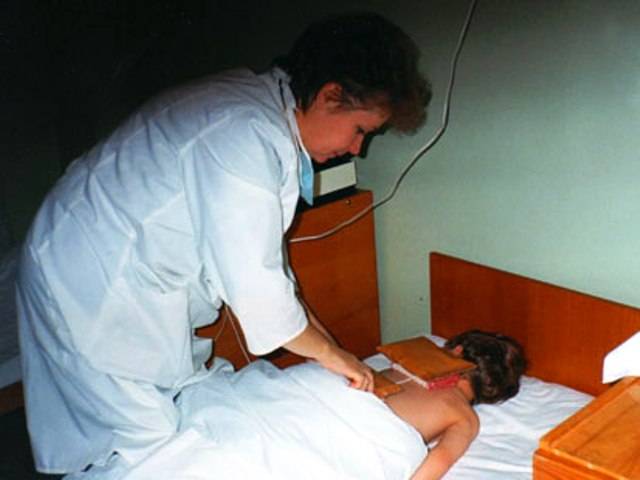
 Силу тока и длительность процедуры увеличивают постепенно. Курс лечения – 10-12 процедур.
Силу тока и длительность процедуры увеличивают постепенно. Курс лечения – 10-12 процедур.
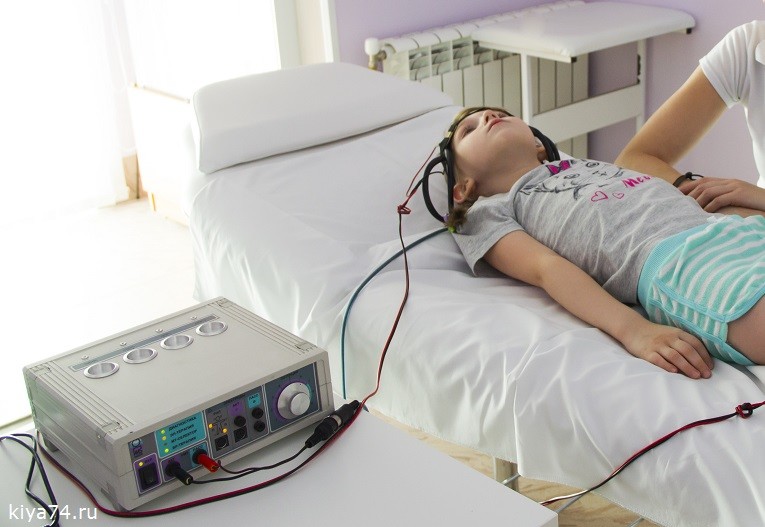
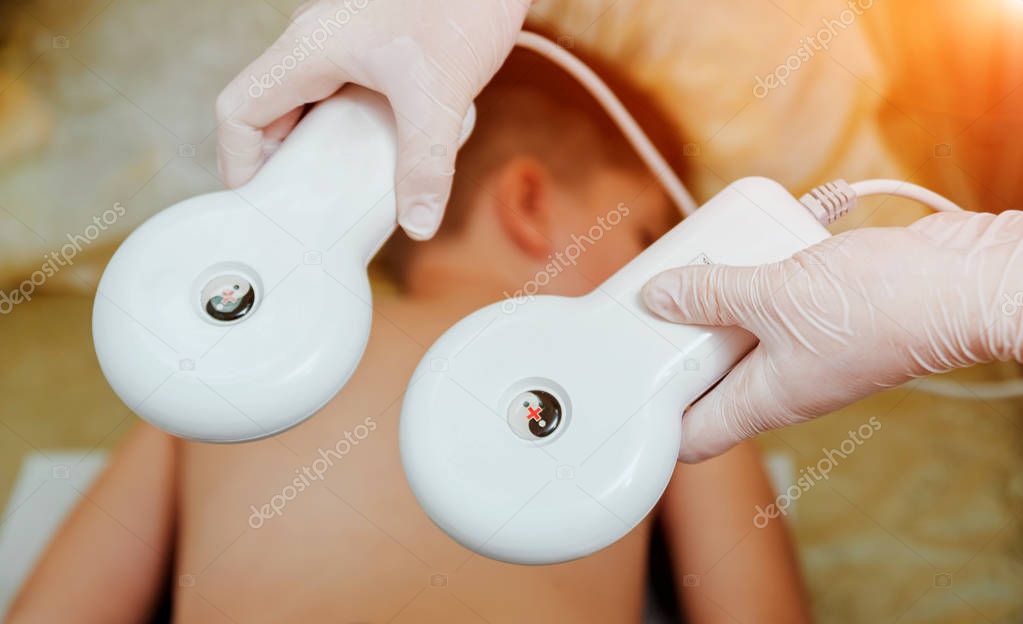 Курс терапии включает 10 сеансов.
Курс терапии включает 10 сеансов.