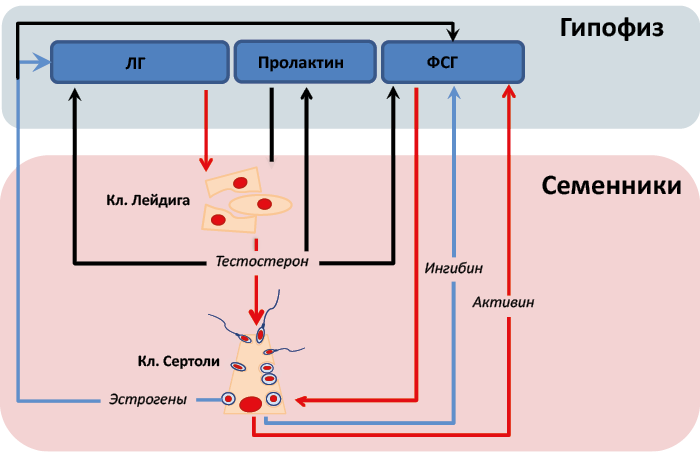
Гормон стресса пролактин: Этот «загадочный » пролактин .
эндокринолог, профессор, д.м.н Поздняк Александр Олегович.
14 ноября 2019
Журнал «Здоровье семьи»Когда в семье стоит вопрос о рождении ребенка, но женщина наблюдается с диагнозом первичное или вторичное бесплодие, в первую очередь, необходимо исключить эндокринную патологию. Возможно несколько групп эндокринных заболеваний, дающих синдром бесплодия. В первую очередь, это патология щитовидной железы. Мы хорошо знаем, что наш регион относится к зоне йодного дефицита, и все мы в той или иной степени испытываем его последствия. Если для большинства здоровых людей это может быть не так существенно, то для женщины, которая готовится стать матерью, данный фактор принципиально важен. Йодный дефицит непосредственно отражается на развитии и формировании ребенка.



- пролактин четко повышается при стрессовых ситуациях (пролактин – гормон стресса)
- при значительных физических нагрузках
- при приеме огромного количества известных лекарственных препаратов (антидепрессанты, транквилизаторы, препараты церукал и мотилиум, которые применяются в гастроэнтерологии, некоторые препараты, применяемые при лечении язвенной болезни)
- бесконтрольное использование гормональных контрацептивных препаратов (женские половые гормоны – эстрогены повышают уровень пролактина).

Кроме воздействия внешних факторов, уровень пролактина часто повышается при хронических заболеваниях печени и почек. Самая серьезная и достаточно частая проблема – это формирование опухоли гипофиза у женщин. С помощью магниторезонансной томографии головного мозга (МРТ) мы ежедневно выявляем подобных пациенток. Любые, даже небольшие опухоли гипофиза хорошо визуализируются при этом исследовании. Оказывается, что у очень большого процента женщин с нарушением менструального цикла и бесплодием выявляются аденомы гипофиза. Это самая частая и нередко поздно выявляемая опухоль гипофиза у женщин, поскольку ее очень трудно заподозрить. В дебюте заболевания субъективных жалоб практически не отмечается: нет головных болей, нарушения зрения, так как опухоль пока еще мала. Единственная жалоба, с которой женщина приходит к гинекологу – нарушенный менструальный цикл и бесплодие. Иногда гинеколог без исследования уровня пролактина в крови принимает решение о назначении женщине гормональных контрацептивов для коррекции менструального цикла.
Парадоксальное бесплодие
Есть категория пациенток, у которых отмечается регулярный менструальный цикл и овуляция, но беременность почему-то не наступает – это женщины с так называемым парадоксальным бесплодием. Дело в том, что у этих пациенток уровень пролактина повышается не постоянно, а в отдельные моменты времени:
- ночью (в этом случае мы просим пациентку сдать пролактин в 1.00-2.00 часа ночи).
- в середине менструального цикла, при этом овуляция происходит, но сдвигается на более позднее время – синдром укороченной лютеиновой фазы.

Правила взятия крови на пролактин:
- необходимо состояние полного покоя, чтобы у женщины накануне и в день анализа не было стрессовой ситуации
- перед анализом необходимо успокоиться, посидеть 15-20 минут
- за день до исследования исключаются сауны, бани, любые тепловые процедуры
Известна еще одна патология, с которой часто приходится иметь дело и эндокринологам и гинекологам – синдром поликистозных яичников. Это очень серьезная эндокринная патология, которая имеет хроническое течение и, как правило, не достигается полное излечение, а только временное улучшение состояния пациентки. На сегодняшний день доказано, что во многом развитие синдрома поликистозных яичников происходит за счет повышения секреции гормона инсулина в поджелудочной железе. Любое повышение уровня инсулина влечет за собой повышенный аппетит, избыточный вес, ожирение, а в последующем – метаболический синдром, плавно переходящий в более старшем возрасте в сахарный диабет 2-го типа. Развитие поликистоза яичников начинается с подросткового периода (14-16 лет). Сначала девочка просто имеет избыточный вес, затем у нее исчезает овуляция, нарушается менструальный цикл, появляется избыточное оволосение, в более старшем возрасте формируется первичное бесплодие, при этом ожирение все больше прогрессирует. Поэтому когда мы говорим о поликистозе яичников, то на сегодня во всех алгоритмах лечения на первом месте стоит коррекция массы тела, а потом уже применение специфической терапии данного заболевания. Для коррекции веса необходимо правильное питание, дозированные физические нагрузки, специальное обучение в школах для больных с избыточным весом (такие школы в Казани уже существуют). Пациентка с поликистозом яичников должна наблюдаться как у гинеколога, так и у эндокринолога одновременно.
Любое повышение уровня инсулина влечет за собой повышенный аппетит, избыточный вес, ожирение, а в последующем – метаболический синдром, плавно переходящий в более старшем возрасте в сахарный диабет 2-го типа. Развитие поликистоза яичников начинается с подросткового периода (14-16 лет). Сначала девочка просто имеет избыточный вес, затем у нее исчезает овуляция, нарушается менструальный цикл, появляется избыточное оволосение, в более старшем возрасте формируется первичное бесплодие, при этом ожирение все больше прогрессирует. Поэтому когда мы говорим о поликистозе яичников, то на сегодня во всех алгоритмах лечения на первом месте стоит коррекция массы тела, а потом уже применение специфической терапии данного заболевания. Для коррекции веса необходимо правильное питание, дозированные физические нагрузки, специальное обучение в школах для больных с избыточным весом (такие школы в Казани уже существуют). Пациентка с поликистозом яичников должна наблюдаться как у гинеколога, так и у эндокринолога одновременно.
Патология надпочечников.
Эту патологию необходимо исключать у пациенток, имеющих выраженное вторичное оволосение на теле и нарушения менструального цикла. Для женщины нормальным является умеренное вторичное оволосение в области голени и предплечья. Но если имеется диссеминированное, распространенное вторичное оволосение на конечностях, животе, в области грудных желез – это уже является патологией, при этом необходимо исключить так называемый адреногенитальный синдром. Он бывает врожденным и скрытым. Скрытый адреногенитальный синдром проявляет себя после полового развития, в возрасте старше 15-16 лет, когда девушка вполне сформирована. Происходит избыток секреции мужских половых гормонов (причем не в яичниках, а в надпочечниках), и у женщины появляется повышенное вторичное оволосение и дисфункция яичников. Субъективно состояние пациентки существенно не меняется. Однако адреногенитальный синдром представляет серьезную помеху нормальному зачатию и вынашиванию ребенка. Если женщина все же беременеет, у нее имеется большой риск выкидыша.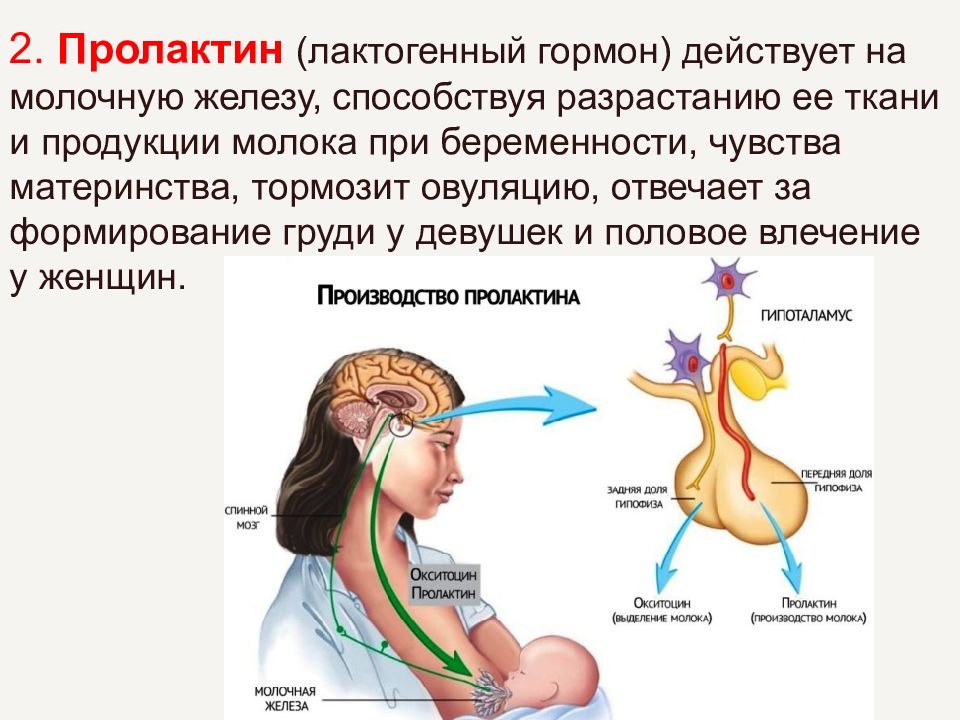 Поэтому принципиально важно диагностировать эту патологию (отмечается повышенный уровень 17-гидроксипрогестерона и адренокортикотропного гормона при иммуноферментном исследовании). При выявлении адреногенитального синдрома женщина и до беременности и во время нее принимает малые дозы гормональных глюкокортикоидных препаратов. Здесь названы только наиболее частые эндокринные причины бесплодия. В жизни их намного больше. Все перечисленные эндокринные заболевания вносят большой вклад в общую структуру бесплодия у женщин. И поэтому, конечно, при любом случае бесплодия необходима консультация врача– эндокринолога.
Поэтому принципиально важно диагностировать эту патологию (отмечается повышенный уровень 17-гидроксипрогестерона и адренокортикотропного гормона при иммуноферментном исследовании). При выявлении адреногенитального синдрома женщина и до беременности и во время нее принимает малые дозы гормональных глюкокортикоидных препаратов. Здесь названы только наиболее частые эндокринные причины бесплодия. В жизни их намного больше. Все перечисленные эндокринные заболевания вносят большой вклад в общую структуру бесплодия у женщин. И поэтому, конечно, при любом случае бесплодия необходима консультация врача– эндокринолога.
На сегодня возможна диагностика практически любой эндокринной патологии. Быструю и комплексную диагностику эндокринной патологии, консультацию врача и качественное лечение пациенты могут получить, придя в медицинский центр «Здоровье семьи». Если синдром повышенной секреции пролактина дает 30% эндокринного бесплодия, то поликистоз яичников еще 20-30%, а гипотиреоз – 15-20%.
Поделиться в соц. ôis Краткие сообщения
ôis Краткие сообщения
О 2002, СПб РО РААКИ
ВЛИЯНИЕ ПРОЛАКТИНА НА ИЗМЕНЕНИЕ КОНЦЕНТРАЦИИ КОРТИКОСТЕРОИД В КРОВИ И ИНТЕНСИВНОСТЬ ИММУНОЛОГИЧЕСКИХ РЕАКЦИЙ У КРЫС ПРИ СТРЕССЕ
Немирович-Данченко Е.А., Фомичева Е.Е.
Отдел общей патологии и патофизиологии
ГУ «НИИэкспериментальной медицины РАМН», Санкт-Петербург, Россия
Резюме. Исследовали механизмы иммуномодулирующего действия пролактина при стрессе. Показано, что стрессорное воздействие (охлаждение в камере крыс- самцов Wistar при -20°С, 20 мин) вызывало значительное повышение концентрации кортикостерона в крови и угнетение гуморального иммунного ответа. Предварительное внутрибрюшинное введение пролактина (Human, Sigma) в дозе 25 нг/100 г массы (до стресса и иммунизации) предотвращало развитие стрессобусловленной иммуносупрессии. В ответ на стрессорное воздействие и введение пролактина наблюдалась усиленная продукция лимфоцит-активирующих факторов, важнейшим из которых является интерлейкин-1. Освобождение лимфоцит-активирующих факторов макрофагами еще больше усиливалось при дополнительной стимуляции макрофагов липополисахаридом. Стрессорное воздействие не изменяло активированный пролактином уровень освобождения лимфоцит-активирующих факторов, что может свидетельствовать об увеличении под влиянием пролактина функционального резерва макрофагов и продукции ими иммуномодулирующих цитокинов, в том числе интерлейкина-1, играющего, по-видимому, определенную физиологическую роль в иммунопротективных эффектах пролактина при стрессе.
В ответ на стрессорное воздействие и введение пролактина наблюдалась усиленная продукция лимфоцит-активирующих факторов, важнейшим из которых является интерлейкин-1. Освобождение лимфоцит-активирующих факторов макрофагами еще больше усиливалось при дополнительной стимуляции макрофагов липополисахаридом. Стрессорное воздействие не изменяло активированный пролактином уровень освобождения лимфоцит-активирующих факторов, что может свидетельствовать об увеличении под влиянием пролактина функционального резерва макрофагов и продукции ими иммуномодулирующих цитокинов, в том числе интерлейкина-1, играющего, по-видимому, определенную физиологическую роль в иммунопротективных эффектах пролактина при стрессе.
Ключевые слова: стресс, пролактин, глюкокортикоидные гормоны, лимфоцит-активирующие факторы.
Nemirovich-Danchenko Е.А., Fomichyova Е.Е.
PROLACTIN EFFECT ON CHANGES IN BLOOD CORTICOSTERONE CONCENTRATIONS
AND INTENSITY OF RAT IMMUNOLOGICAL REACTIONS UNDER STRESS
Abstract. Mechanisms of immunomodulatory action of prolactin under stress were studied. It was shown that stress influence (Wistar male rats cooling in special chambers at -20°C during 20 min) caused significant increase in blood corticosterone concentration as well as pronounced supression of humoral immune response/ Preliminary intraperitoneal administration of prolactin (human, Sigma) in dose 25ng/100g body weight before stress application and immunization prevented development stress-induced immunosuppression. Spontaneous production of lymphocyte-activating factors, the main component of which is interleukin-1, was observed as the response to stress exposure and prolactin administration. The release of lymphocyte-activating factors by macrophages was even more increased after additional stimulation of macrophages by lypopolysaccharide. Stress influence did not change the level of lymphocyte-activating factors release, activated by prolactin, that might be due to prolactin-induced elevation of macrophages’ functional reserves and their production of immunomodulatory cytokines, including interleukin-1, which seems to play significant physiological role in manifestation of prolactin effects under stress.
Mechanisms of immunomodulatory action of prolactin under stress were studied. It was shown that stress influence (Wistar male rats cooling in special chambers at -20°C during 20 min) caused significant increase in blood corticosterone concentration as well as pronounced supression of humoral immune response/ Preliminary intraperitoneal administration of prolactin (human, Sigma) in dose 25ng/100g body weight before stress application and immunization prevented development stress-induced immunosuppression. Spontaneous production of lymphocyte-activating factors, the main component of which is interleukin-1, was observed as the response to stress exposure and prolactin administration. The release of lymphocyte-activating factors by macrophages was even more increased after additional stimulation of macrophages by lypopolysaccharide. Stress influence did not change the level of lymphocyte-activating factors release, activated by prolactin, that might be due to prolactin-induced elevation of macrophages’ functional reserves and their production of immunomodulatory cytokines, including interleukin-1, which seems to play significant physiological role in manifestation of prolactin effects under stress. (MetLImmunoL, 2002, vol.4, N 4-5, pp 613-618)
(MetLImmunoL, 2002, vol.4, N 4-5, pp 613-618)
Изучение механизмов влияния стресса на защит — главными составляющими стрессорной реакции явные функции организма является одной из важней- ляется активация гипоталамо-гипофизарной-адрено-
ших задач современной медицины. Как известно, кортикальной системы (ГГАКС), сопровождающая-
—————————————— ся повышением концентрации АКТГ и глюкокорти-
Адрес для переписки: коидных гормонов (ГК) в крови, что может быть од-
Немирович-Данченко Елена Алексеевна ной из причин развития стрессобусловленной имму-
Санкт-Петербург, 197376, ГУ «НИИ носупресии [3]. Одновременно в ответ на стрессор-
Экспериментальной медицины РАМН». НОе воздействие отмечено увеличение уровня пролак-
НОе воздействие отмечено увеличение уровня пролак-
Тел.: (812) 234-15-83, факс: (812) 234-94-93, тина в крови [9]. Хотя при стрессе пролактин и ГК
e-mail: [email protected]
гормоны секретируются в кровь одновременно, характер их взаимовлияния и действие на функции иммунной системы неоднозначны. Установлено, что при некоторых видах стресса ГК гормоны угнетают функции иммунной системы [3]. Повышение уровня эндогенного пролактина при стрессе не препятствует развитию стрессобусловленной иммуносупрессии, которая может быть предотвращена введением экзогенного пролактина [5]. По данным ряда авторов, пролак-тин активирует функции иммунной системы [9, 12], усиливает пролиферацию иммунокомпетентных клеток [14], повышает фагоцитарную активность макрофагов [16] и продукцию ими иммуномодулирующих цитокинов [10], стимулирует гуморальный и клеточно-опосредованный иммунный ответ [5]. Иммуномодулирующие эффекты пролактина связывают с наличием рецепторов к данному гормону практически на всех клетках иммунной системы [11, 14]. Однако механизмы иммуномодулирующего действия пролактина в целостном организме и его кооперативных эффек-
Иммуномодулирующие эффекты пролактина связывают с наличием рецепторов к данному гормону практически на всех клетках иммунной системы [11, 14]. Однако механизмы иммуномодулирующего действия пролактина в целостном организме и его кооперативных эффек-
тов с другими иммуномодуляторами (IL-1, ГК гормоны и др.) раскрыты далеко не исчерпывающе. Исследования о взаимном влиянии ГК гормонов и пролактина немногочисленны и выполнены в основном in vitro. Так, показано, что пролактин усиливает освобождение кортикотропин-рилизинг фактора клетками гипоталамуса и синтез АКТГ в клетках гипофиза [13], дозозависимо стимулирует продукцию кортикостеро-на, воздействуя прямо на клетки ретикулярной зоны коры надпочечников [7]. ГК гормоны негативно влияют на эффекты пролактина, тормозят дифференциров-ку лактотрофов гипофиза и синтез пролактина [13], отменяют стресс-, эстроген- и IL-1 -индуцированный подъем уровня пролактина в крови в опытах in vivo [6, 9,18]. В то же время показаны дозозависимые эффекты ГК гормонов на концентрацию пролактина в крови: низкие дозы гормона стимулируют освобождение пролактина, а высокие — его угнетают [б].
В то же время показаны дозозависимые эффекты ГК гормонов на концентрацию пролактина в крови: низкие дозы гормона стимулируют освобождение пролактина, а высокие — его угнетают [б].
В настоящей работе была поставлена задача проанализировать действие пролактина, введенного
А (без стресса)
физ.р-р
■ прл 5 нг
■ прл 25 нг
Б 10 мин 2 ч 24 ч 5 сут
Рис.1. Изменения уровня Кс в крови нестрессированных (А) и стрессированных (Б) крыс после введения физиологического раствора, пролактина в дозах 5 нг/100 г и 25 нг/100 г массы (В). По оси ординат — концентрация Кс в сыворотке крови крыс, нг/ мл, по оси абсцисс — время после аппликации стресса и группы животных, Б — базальный уровень кортикостерона у инташых животных.
* Р < 0,05 по сравнению с базальным уровнем Кс у интакгных животных л Р < 0,05 по сравнению с контрольной группой животных, которым вводили физиологический раствор.
внутрибрюшинно (в/бр) крысам, на стрессиндуци-рованные изменения концентрации ГК гормонов в крови, интенсивность гуморального иммунного ответа и продукции макрофагами лимфоцитактивиру-ющих факторов (LAF), важнейшим из которых является IL-1 [8].
Материалы и методы
Работа проведена на 72 крысах-самцах Wistar, массой 180-200 г. В качестве стрессорного воздействия использовали охлаждение животных в Холодовой камере при -20°С в течение 20 мин. По окончании процедуры стрессирования животных дека-питировали через 10 мин, 2 часа, 24 часа, а также на 5-е сутки. За 20 мин до начала стрессирования животным вводили в/бр пролактин человека (Sigma) в дозе 5 нг/100 г и 25 нг/100 г массы. Известно, что использование препаратов пролактина человеческого, а также бычьего, овечьего происхождения возможно у животных, находящихся на более низкой ступени эволюционного развития (в данном случае
Известно, что использование препаратов пролактина человеческого, а также бычьего, овечьего происхождения возможно у животных, находящихся на более низкой ступени эволюционного развития (в данном случае
— у крыс) [14]. В ряде опытов сразу по окончании охлаждения животных иммунизировали эритроцитами барана (ЭБ) в дозе 1х109 кл./животное. Уровень гуморального иммунного ответа оценивали на 5-е сутки после иммунизации по общим титрам ан-
тител в сыворотке крови методом прямой гемагглю-тинации [1].
Концентрацию кортикостерона (Кс) в сыворотке крови определяли радиоиммунологически по методу Н.П. Гончарова и соавт. [2].
При исследовании влияния пролактина на продукцию лимфоцит-активирующих факторов (LAF) перитонеальными макрофагами крыс, после 18-часового культивирования мононуклеарных фагоцитов в среде RPMI-1640 с добавлением LPS (Sigma) в концентрации 20 мкг/мл и без дополнительной стимуляции, лимфоцит-активирующие свойства инкубатов оценивали по их способности оказывать комитогенное действие на пролиферацию тимоцитов, стимулированных конканавалином A (Con А) в субоптимальной дозе по методу Rosenwasser, Dinarello [15]. Включение меченого тимидина в ДНК делящихся клеток оценивали с помощью сцинтиляционного ß-счетчика (LKB). За единицу активности LAF принимали такую его концентрацию (в 1 мл), которая вызывала усиление пролиферации тимоцитов, равное 50% по отношению к её максимальной стимуляции, вызванной субоптимальной дозой лектина.
Включение меченого тимидина в ДНК делящихся клеток оценивали с помощью сцинтиляционного ß-счетчика (LKB). За единицу активности LAF принимали такую его концентрацию (в 1 мл), которая вызывала усиление пролиферации тимоцитов, равное 50% по отношению к её максимальной стимуляции, вызванной субоптимальной дозой лектина.
Материалы обработаны статистически с использованием i-критерия Стьюдента [4]. Данные представлены в виде среднего арифметического±ошиб-ка к среднему (М±т).
1 2 3
1 2 3
Рис.2. Изменение величины гуморального иммунного ответа у нестрессированных (А) и стрессированных животных (Б) при введении пролактина. По оси ординат — уровень общих антител в сыворотке крови крыс, -log 2; По оси абсцисс — группы животных, которым вводили: 1- физиологический раствор (контрольные), 2 — пролактин в дозе 5 нг/100 г, 3 — пролактин в дозе 25 нг/100г массы. * Р < 0,05 по сравнению с группой 1,А, # Р< 0,05 по сравнению с группой 1,Б, я Р< 0,05 по сравнению с группой 3,А
* Р < 0,05 по сравнению с группой 1,А, # Р< 0,05 по сравнению с группой 1,Б, я Р< 0,05 по сравнению с группой 3,А
А (10 мин, без стресса) В (10 мин после стресса)
■ без дополн. стимуляции
■ стимуляция ЛПС
Б (24 часа, без стресса)
10
им
к
прл 5 нг прл 25 нг
Г ( 24 часа после стресса)
10
к
прл 5 нг прл 25 нг
Рис. З. Влияние введения пролактина на продукцию ДО перитонеальными макрофагами стрессированных и нестрессиро-ванных животных. По оси ординат — 1АР активность супернатантов перитонеальных макрофагов в уел. ед. х 10’3. По оси абсцисс- группы животных. К- контрольные животные, которым вводили физиологический раствор.
З. Влияние введения пролактина на продукцию ДО перитонеальными макрофагами стрессированных и нестрессиро-ванных животных. По оси ординат — 1АР активность супернатантов перитонеальных макрофагов в уел. ед. х 10’3. По оси абсцисс- группы животных. К- контрольные животные, которым вводили физиологический раствор.
* Р < 0,05 по сравнению с продукцией 1АЯ нестимулированными клетками контрольной группы животных, которым вводили физиологический раствор. А Р < 0,05 по сравнению с продукцией 1_АЯ стимулированными клетками контрольной группы животных
Результаты и обсуждение
В/бр введение пролактина в дозах 5 и 25 нг/100 г массы вызывало увеличение концентрации Кс в сыворотке крови крыс в течение первых часов по сравнению с базальным уровнем Кс у интактных животных (рис.1,А). Под влиянием стрессорного воздействия как у животных контрольной группы (в/бр введение физиологического раствора с последующей аппликацией стресса), так и у животных опытных групп (комбинация стрессорного воздействия и введения пролактина), наблюдалось повышение концентрации Кс в крови, которое в случае введения пролактина сохранялось в течение суток, чего не наблюдалось у контрольных животных (рис. 1,Б). Следует отметить, что стрессорное воздействие на животных, которым вводили пролактин, практически не увеличивает у них уровня кортикостерона по сравнению с этим же показателем у нестрессированных животных, регистрируемым на соответствующих сроках (сравнить рис.1, А и Б).
1,Б). Следует отметить, что стрессорное воздействие на животных, которым вводили пролактин, практически не увеличивает у них уровня кортикостерона по сравнению с этим же показателем у нестрессированных животных, регистрируемым на соответствующих сроках (сравнить рис.1, А и Б).
Величина гуморального иммунного ответа на ЭБ при введении пролактина в обеих выбранных дозах не изменялась по сравнению с этим показателем у контрольных животных, получавших физиологический раствор (рис.2,А). При аппликации холодового стресса отмечалось значительное угнетение иммунного ответа (рис.2, Б, гр.1, Р<0,05). Предварительная инъекция пролактина в дозе 25 нг/100г массы (до стрессорного воздействия и иммунизации) предотвращала развитие стрессобусловленной иммуносупрессии, при этом величина гуморального иммунного ответа у этих животных возрастала по сравнению с ее величиной у стрессированных животных 1 группы и даже превышала значения этого показателя у нестрессированных животных (рис. 2, гр.З, Р<
2, гр.З, Р<
0,05). При введении пролактина в дозе 5 нг/100 г этот эффект не наблюдался, (рис.2, гр.2)
Полученные в работе данные показывают, что предварительное введение пролактина перед стрес-сорным воздействием, хотя и сопровождается повышением концентрация Кс в крови, тем не менее, пре-
дотвращает угнетение гуморального иммунного ответа. По мнению Sandy et.al. [17], проводивших исследования в условиях in vitro, конечный результат сочетанного действия пролактина и ГК гормонов зависит от соотношения доз этих гормонов в среде. Возможно, что в данном случае характер влияния холодового стресса на функции иммунной системы зависит от баланса уровня пролактина при его введении в дозе, превышающей физиологическую, и эндогенных колебаний ГК гормонов.
При исследовании влияния пролактина на способность перитонеальных макрофагов животных продуцировать лимфоцит-активирующие факторы (LAF), установлено, что в/бр введение пролактина нестрессированным животным в разных дозах вызывало освобождение LAF макрофагами, которое сохранялось в течение суток (рис. З,А). Спонтанная продукция LAF наблюдалась в ответ на стрессорное воздействие и при последовательной аппликации пролактина и стресса. Добавление пролактина усиливало спонтанную продукцию LAF макрофагами, как через 10 мин, так и через 24 часа после аппликации стресса, превосходя в 1,5-2 раза значения LAF, зарегистрированные в случае стрессорного воздействия у контрольных животных, получавших физиологический раствор (рис.З, Б,Г). При дополнительной стимуляции перитонеальных макрофагов LPS наблюдалось усиление продукции LAF у животных, получавших пролактин, в 1,5-2 раза превышающее ее значения у стимулированных клеток животных контрольной группы (Р<0,05), а также по сравнению с нестимулированными клетками животных этих же групп (рис.З Р<0,05). Дополнительная стимуляция макрофагов стрессированных животных, которым вводили пролактин, не вызывала увеличения продукции LAF макрофагами этих животных по сравнению с ее значениями у контрольных стрессированных животных.
З,А). Спонтанная продукция LAF наблюдалась в ответ на стрессорное воздействие и при последовательной аппликации пролактина и стресса. Добавление пролактина усиливало спонтанную продукцию LAF макрофагами, как через 10 мин, так и через 24 часа после аппликации стресса, превосходя в 1,5-2 раза значения LAF, зарегистрированные в случае стрессорного воздействия у контрольных животных, получавших физиологический раствор (рис.З, Б,Г). При дополнительной стимуляции перитонеальных макрофагов LPS наблюдалось усиление продукции LAF у животных, получавших пролактин, в 1,5-2 раза превышающее ее значения у стимулированных клеток животных контрольной группы (Р<0,05), а также по сравнению с нестимулированными клетками животных этих же групп (рис.З Р<0,05). Дополнительная стимуляция макрофагов стрессированных животных, которым вводили пролактин, не вызывала увеличения продукции LAF макрофагами этих животных по сравнению с ее значениями у контрольных стрессированных животных.
Полученные данные свидетельствуют о высоком уровне активации макрофагов животных, которым вводили пролактин, как без дополнительной стимуляции, так и при добавлении к ним LPS. Стрессорное воздействие не изменяет активированное про-лактином освобождение LAF (Р>0,05), что, по-видимому, может быть связано с увеличением под влиянием пролактина функционального резерва макрофагов и продукции ими LAF. В этом плане полученные данные согласуются с литературными, в которых отмечено, что пролактин (в условиях in vitro) усиливает активность макрофагов и продукцию ими цитокинов [10, 16].
Стрессорное воздействие не изменяет активированное про-лактином освобождение LAF (Р>0,05), что, по-видимому, может быть связано с увеличением под влиянием пролактина функционального резерва макрофагов и продукции ими LAF. В этом плане полученные данные согласуются с литературными, в которых отмечено, что пролактин (в условиях in vitro) усиливает активность макрофагов и продукцию ими цитокинов [10, 16].
Активация клеток системы мононуклеарных фагоцитов, как начального звена обеспечения защиты организма в условиях стресса и введения пролактина, увеличение резервных возможностей макрофагов и продукции ими LAF, в том числе и IL-1, играет определенную физиологическую роль в предотвра-
щении пролактином развития стрессиндуцирован-ных иммуносупрессий, и может, по-видимому, рассматриваться как проявление одного из механизмов иммунопротективного действия пролактина.
Список литературы
1. Вязов О.В., Ходжаева Ш.Х. Руководство по иммунологии. — М.: Медицина, 1973, С.З — 13.
Вязов О.В., Ходжаева Ш.Х. Руководство по иммунологии. — М.: Медицина, 1973, С.З — 13.
2. Гончаров Н.П., Воронцов В.И., Кадия Г.К., Ан-тоничев А.В., Бутнев В.Н. Изучение гормональной функции надпочечников и половых желез в опытах на обезьянах.// Вестник АМН СССР — 1977. — №8. -С. 13-20.
3. Корнева Е.А., Шанин С.Н., Рыбакина Е.Г. Интерлейкин-1 в реализации стрессиндуцированных изменений функций иммунной системы. // Росс. Физиол. Журнал. — 2000. Т. 86. — № 3. — С. 292-302.
4. Стрелков Р.Б. Метод вычисления стандартной ошибки и доверительных интервалов средней арифметической с помощью таблиц. — Алашара, Сухуми
— 1966. — 39 с.
5. Berczi I., Nagy Е., The influence of pituitary hormones and neurotransmitters on the immune system. // J. Immunol. Immunopharmacol. — 1988 — Vol.8 — №3, P. 186-194.
// J. Immunol. Immunopharmacol. — 1988 — Vol.8 — №3, P. 186-194.
6. Brann D.W., Putnam C.D., Mahesh V.B. Corticosteroid regulation of gonadotropin and prolactin secretion in the rat. // Endocrinology. — 1990. — V.126. -№ 1. — P.159-166.
7. Chang L.L., Lo M.Y., Kan S.F., Huang W.Y. Direct effects of prolactin on corticosterone release by zona fasciculata reticularis cells from male rats. // J. Cell. Biochem. — 1999. — V.74. — № 4. — P. 563-572.
8. Dinarello C.A. Induction of interleukin-1 and interleukin-1 receptor antagonist. // Seminars in oncology. — 1997. — V. 24. — № 3. — Suppl.9. — S9-81- S9-93.
9. Gala R.R. Physiology and mechanism of the stress-induced changes in prolactin secretion in rats. // Life Science. — 1990. — Vol.46. — P.1407-1420.
10. Gaytan F„ Morales C., Bellido C., Aguilar E., Sanchez-Criado JE. Role of prolactin in the regulation of macrophages and in the proliferative activity of vascular cells in newly formed and regressing rat corpora lutea. // Biology of reproduction. — 1997. — Vol.57. — № 2. — P.478-486.
Gaytan F„ Morales C., Bellido C., Aguilar E., Sanchez-Criado JE. Role of prolactin in the regulation of macrophages and in the proliferative activity of vascular cells in newly formed and regressing rat corpora lutea. // Biology of reproduction. — 1997. — Vol.57. — № 2. — P.478-486.
11. Kelly P.A., Djiane J., Postel-Vinay M.C., Ed-ery M. The prolactin / growth hormone receptor family. // Endocrine reviews. — 1991. — Vol.12. — №3, P.235-251.
12. Matera L. Action of pituitary and lymphocyte prolactin.//Neuroimmunomodulation. — 1997. — Vol.4.
— P. 171-180.
13. Moro М., Maraschini C., Cavaguini F. Dopamine infusion enhances the ACTH and cortisol response to metoclopramide in hyperprolactinemic patients but not in normal subjects. // Gynecological Endocrinology. — 1997. — Vol.11. — № 3. — P.155-162.
— № 3. — P.155-162.
14. Murphy W.J., Rui H., Longo Dan L. Effect of growth hormone and prolactin immune development and function. // Life Science. — 1995. -Vol.57.-X21.-P. 1-
14.
15. Rosenwasser L.J., Dinarello C.A. Ability of human leucocytic pyrogen to enhance phytohemagglutinin induce murine thymocyte proliferation. // Cell. Immunology. — 1981. — Vol. 63. — № 1. — P.134-142.
16. Ortega E., Former M.A., Barriga C. Effect of prolactin on the in vitro phagocytic capacity of macrophages. // Comp. Immunol. Microbiol. Infect. Dis. — 1996. -Vol. 19. — № 2. — P. 139-146.
17. Sandi C., Cambronero J.C., Borrell G., Guaza C. Mutually antagonistic effects of corticosterone and prolactin on rat lymphocyte proliferation. // Neuroendocrinology. — 1992. — Vol.56. — № 4. — P. 574-581.
— 1992. — Vol.56. — № 4. — P. 574-581.
поступила в редакцию 21.12.2001 принята к печати 28.02.2002
Гормоны которые вырабатываются во время стресса. Пролактин и кортизол — гормоны стресса
Гормоны относятся к одним из самых неизученных веществ в организме. Благодаря им органы правильно выполняют свои функции, но сбой почти всегда становится причиной для развития заболеваний. Одним из самых противоречивых является пролактин, который вырабатывается в гипофизе. С одной стороны, благодаря ему у женщин появляется грудное молоко после рождения малыша, с другой — его количество увеличивается при стрессе. Последнее может стать предпосылкой гормонального дисбаланса.
Что такое пролактин?
Пролактин считается женским гормоном, поскольку вырабатывается при грудном вскармливании и поддерживает в яичнике существование желтого тела.Это гормон, вырабатываемый в передней части гипофиза. Его образование происходит благодаря дофамину, который вырабатывается ядрами гипоталамуса. Попадая с помощью системы кровообращения в гипофиз, он приводит к блокировке пролактина. Его выработку снижает и прогестерон, появляющийся у женщин после овуляции.
Его образование происходит благодаря дофамину, который вырабатывается ядрами гипоталамуса. Попадая с помощью системы кровообращения в гипофиз, он приводит к блокировке пролактина. Его выработку снижает и прогестерон, появляющийся у женщин после овуляции.
Вещество представляет собой одноцепочечный полипептид. В его составе есть 199 аминокислот. В одной молекуле существует три дисульфидных мостика. Из-за гетерогенности молекулы анализы могут показывать разные результаты. Рецепторы пролактина есть в молочных железах печени, почках, поджелудочной железе, надпочечниках, мышечном каркасе, коже и в некоторых отделах ЦНС.
Самое большое количество гормона вырабатывается в фазе глубокого сна и сразу после пробуждения. Со временем его количество уменьшается. Гормон стресса выполняет несколько функций:
- участвует в формировании вторичных половых признаков у женщин в период развития;
- подавляет возможность овуляции во время кормления грудью;
- обладает обезболивающим эффектом;
- снижает уровень других гормонов;
- активизирует правильный иммунный ответ;
- стимулирует баланс различных веществ в организме.

Медики отмечают, что до сих пор не выявлены все особенности описываемого гормона. Современные исследования направлены на получение полной картины о нем, его функциях.
Взаимосвязь пролактина и стресса
На фоне физической переутомляемости, при нарушении психологического или душевного равновесия количество пролактина в крови резко повышается. При наличии травмирующего фактора происходят физиологические изменения. Наиболее восприимчивы к различным агрессорам эндокринные ткани.
При первых признаках опасности начинают активно работать надпочечники. Ими вырабатывается адреналин и норадреналин. Значения первого повышаются при тревоге, различных шоковых состояниях, страхе. При поступлении в кровь он приводит к усилению сердцебиения и расширению зрачков. Слишком длительное воздействие адреналина становится причиной уменьшения защитных сил организма.
Норадреналин выделяется при сильном стрессе, в основном приводит к повышению артериального давления. Если адреналин по-другому называется «гормон страха», то «норадреналин» — ярости.
Если адреналин по-другому называется «гормон страха», то «норадреналин» — ярости.
При сильной физической нагрузке вырабатывается кортизол. Он не оказывает слишком большого влияния на организм, но при его накоплении, постоянном воздействии, возникает чувство депрессии, появляется тяга к продуктам с большим содержанием глюкозы.
В цепочке биохимических реакций при стрессе участвует и пролактин. Он появляется не только в состоянии стресса, но и депрессии. На фоне его чрезмерного увеличения происходит нарушение в обмене веществ. Он необходим для защиты организма: запускаются особые механизмы, позволяющие человеку адаптироваться к новым условиям.
В маленьких дозах стрессовые гормоны регулируют состояние человека, но при высоких объемах начинают причинять вред. Особенно сильное негативное влияние вещества имеют при хронических стрессах.
Повышение пролактина становится причиной хронической усталости и нарушения сна.
Последствия повышения гормона стресса
Пролактин регулирует работу половой системы, оказывает влияние на обмен веществ. При стрессе происходит моментальное его увеличение в крови. Это запускает ряд патологических процессов:
При стрессе происходит моментальное его увеличение в крови. Это запускает ряд патологических процессов:
- анорексию;
- синдром поликистозных яичников;
- цирроз печени;
- повышение холестерина и артериального давления;
- нарушение в сонных циклах;
- истончение кожного покрова.
Разные последствия наблюдаются у мужчин и женщин. У представителей сильного пола при повышенном количестве гормона стресса происходит ослабление потенции, отсутствие полового влечения. Это связана со снижением вырабатываемых половых гормонов и сперматозоидов. Происходит резкое уменьшение тестостерона (мужского гормона), интенсивная выработка эстрогена (женского гормона).
Если уровень пролактина повысился на фоне физического переутомления, чрезмерных нагрузок, временная реакция не влияет на гормональное равновесие. В других случаях возможны затяжные депрессии, появление лишнего веса, снижение жизненного тонуса, бесплодие и импотенция.
Поскольку тестостерон и пролактин зависят друг от друга, чем больше в организме пролактина, тем меньше тестостерона. Соответственно, чем ниже уровень мужского гормона, тем больше различных проблем может возникнуть.
Соответственно, чем ниже уровень мужского гормона, тем больше различных проблем может возникнуть.
При долговременном повышении пролактина, не связанном с грудным вскармливанием, может наблюдаться нарушение менструального цикла. Иногда этот симптом является единственной жалобой. Дополнительно может появиться:
- Бесплодие. Связано с тем, что у женщины не наступает овуляции, а значит, зачатие ребенка.
- Гиперэстрогения. Происходит увеличенное количество эстрогенов. Из-за этого уменьшается количество выделяемой естественной смазки, снижается либидо. На фоне длительно протекающих реакций может развиться миома матки, эндометриоз, остеопороз.
- Ожирение. Увеличение гормонов приводит к увеличенному потреблению еды, особенно сладкого. Из-за этого формируется большее количество подкожной жировой клетчатки.
- Ухудшение зрения. При длительной гиперпролактинемии происходит увеличение клеток гипофиза, который локализуется рядом со зрительными нервами. Это приводит к ухудшению зрения.

При продолжительных стрессах и депрессиях начинается бесконтрольная выработка гормона, что в следствие может привести к формированию раковых опухолей.
Как выявить повышенное количество гормона стресса?
Рекомендовать сдать анализы на уровень пролактина может любой врач. Но при выявлении повышенных значений назначается консультация у эндокринолога. Кровь на исследование может браться несколько раз, поскольку повышение пролактина зависит от уровня асоциального настроя и общего самочувствия. По этой причине рекомендуется проводить диагностику с интервалом в 10 дней. Оптимальное время — через 2-3 часа после пробуждения. Если гиперпролактинемия сохраняется в нескольких пробах, врачи могут предположить наличие серьезных патологий.
Диагностика включает лабораторные и аппаратные методы исследования, позволяющие найти причину повышения гормона стресса.
Кроме анализа крови могут быть назначены дополнительные исследования. Это:
- рентгенологическое обследование,
УЗИ чаще назначается женщинам для обследования молочных желез. Метод подтверждает наличие увеличенного объема железистой ткани. У мужчин ультразвук позволяет выявить уменьшение в размерах яичек.
Метод подтверждает наличие увеличенного объема железистой ткани. У мужчин ультразвук позволяет выявить уменьшение в размерах яичек.
МРТ позволяет показать аденому, некоторые типы опухолей. Новообразования исследуют с помощью контрастных веществ, которые вводят внутривенно. Дополнительно используется рентгенограмма, позволяющая выявить опухоли гипофиза.
Таким образом, аппаратные исследования позволяют определить первопричину, по которой произошло увеличение гормона стресса в организме. При исследовании на другие гормоны стресса можно предположить наличие в жизни травмирующих факторов, определяющих причину сбоя работе систем и органов.
Лечение пациентов с высоким пролактином
Не нужно лечить при повышенных показателях, если:
- концентрация гормона до 1000 Ед/л;
- структура гипофиза не изменена;
- работа органов половой системы происходит без изменений;
- человек имеет нормальный вес.
Главным помощником в борьбе с повышенным пролактином является дофамин. Они «соперничают» между собой, создавая баланс. Для нормализации состояния рекомендуется заниматься тем, что приносит удовольствие, давать организму время для отдыха. Положительный эффект на гормональный фон оказывают:
Они «соперничают» между собой, создавая баланс. Для нормализации состояния рекомендуется заниматься тем, что приносит удовольствие, давать организму время для отдыха. Положительный эффект на гормональный фон оказывают:
- бананы,
- яблоки,
- арбузы,
- клубника,
- чернослив.
Хорошим расслабляющим эффектом является массаж, позволяющий нормализовать эмоциональное состояние.
Снизить уровень гормона стресса можно регулярными физическими нагрузками. Они не должны быть изнуряющими, поскольку это может стать предпосылкой для его повышения. Оптимальный вариант — проводить гимнастику в хорошо проветриваемом помещении или на улице.
Перед сном можно делать и принимать успокаивающие настои, в составе которых есть мята, мелисса и хмель. Понижает уровень тревожности и таблетки с экстрактом валерианы. При использовании прутняка отдайте предпочтение настойке из семян. Для этого 40 гр. сырья заливают спиртом или водкой в количестве 230 гр., настаивают в течение двух недель в темном месте. Принимается настойка по большой ложке, разведённой в 60 мл. воды за 30 минут до еды.
Принимается настойка по большой ложке, разведённой в 60 мл. воды за 30 минут до еды.
При медикаментозном лечении используются разные терапевтические методики для женщин и мужчин. К ним обращаются только в том случае, если другими способами уменьшить уровень гормона не получается.
Можно ли предотвратить гормональный сбой при стрессе?
Главное правило — слушайте свое тело. При гормональных изменениях на фоне стресса появляется беспричинное сердцебиение и беспокойство. Сон перестает дарить чувство отдыха. Утром присутствует усталость, туман в голове, боли в мышцах. Происходит снижение сексуального влечения и сбой в пищевом поведении.
Нужно давать время для отдыха и расслабления. Старайтесь проводить больше времени на свежем воздухе. Не забывайте и об общении, которое помогает снизить уровень тревоги, переключиться на положительные переживания.
Таким образом пролактин — в большей степени женский гормон стресса, поскольку его повышение чаще наблюдается у представительниц слабого пола. Повышение определенных веществ в организме является защитным действием. Но при отсутствии корректировки состояния проявляются физиологические проблемы. Поэтому важно следить за своим эмоциональным состоянием.
Повышение определенных веществ в организме является защитным действием. Но при отсутствии корректировки состояния проявляются физиологические проблемы. Поэтому важно следить за своим эмоциональным состоянием.
Экология жизни. Здоровье: Стресс — это важный элемент нашей жизни. Здоровая доза стресса помогает нам просыпаться по утрам, избегать опасных ситуаций, быть эффективными на работе, ставить и достигать цели.
Стресс — это важный элемент нашей жизни. Здоровая доза стресса помогает нам просыпаться по утрам, избегать опасных ситуаций, быть эффективными на работе, ставить и достигать цели.
Поэтому, небольшие дозы стресса в каждодневной жизни просто необходимы. К сожалению, современная жизнь переполнена всякого рода стрессовыми ситуациями, и наша задача научиться контролировать стресс, а не позволять стрессу быть хозяином нашей жизни, лишая нас сна и аппетита, нарушая гормональный баланс, тем самым нанося непоправимый ущерб нашему здоровью.
Как известно, стресс — это реакция нашего организма на ситуацию, в результате которой в кровь выбрасываются гормоны, которые и помогают нам справится с проблемой резервными силами организма.
Кортизол – главный гормон стресса .
Кортизол – это гормон, который выделяется надпочечниками и регулирует нашу способность управлять стрессом. Он оказывает сильное воздействие на многие физиологические процессы в организме: процессы пищеварения, работу сердечно-сосудистой системы, показатели кровяного давления. Он влияет на уровень физической активности, качество сна, а также может стимулировать непреодолимую тягу к сладкому.
Во время неожиданной стрессовой ситуации (например, во время управления автомобилем вы не заметили знак и нарушили правила), ваши надпочечники в доли секунд выбрасывают в кровь большое количество кортизола, в результате чего вы чувствуете прилив энергии и начинаете быстро соображать: чем это вам грозит и что надо сделать, чтобы избежать проблем. Быстро оценив ситуацию и поняв, что опасность вам не угрожает (потому что вас никто не видел!), вы покидаете место происшествия и возвращаетесь к нормальной жизни.
К сожалению, для многих людей проблема в том как раз и состоит, чтобы вернуться к нормальной жизни — жить настоящим моментом, а не бесконечно переживать драматический опыт прошлого или рисовать пессимистические картины будущего. При таком состоянии сознания (лучше сказать — подсознания) организм человека постоянно находится в стрессе, что порождает череду разного рода нежелательных реакций: повышенное давление, лишний вес, предменструальный синдром, плохой сон, гормональный дисбаланс и многое, многое другое.
При таком состоянии сознания (лучше сказать — подсознания) организм человека постоянно находится в стрессе, что порождает череду разного рода нежелательных реакций: повышенное давление, лишний вес, предменструальный синдром, плохой сон, гормональный дисбаланс и многое, многое другое.
Чтобы понять, как кортизол взаимодействует со всеми остальными гормонами, такими как: прогестерон, эстроген, тестостерон, гормон роста, инсулин, окситоцин, гормоны щитовидной железы и т.д., представьте себе пожарную машину, которая мчится по городу с мигалкой и громкой сиреной. По пути следования пожарки все машины, уступая дорогу, останавливаются.
Тоже самое происходит и с большинством гормонов в нашем организме при стрессе: при наличии кортизола работа их приостанавливается или вообще блокируется.
В результате – лишние килограммы на талии и бедрах, резкие перепады настроения, нерегулярный менструальный цикл, предменструальный синдром, пониженный иммунитет, проблемы с пищеварением, плохой сон, доброкачественные и злокачественные новообразования.
Устойчиво высокий уровень кортизола (дни, недели, месяцы) в крови ведет к атрофии гиппокампуса (структуры головного мозга, ответственной за память), приводя к потере фокуса, депрессиям, нестабильному настроению и бессоннице. Постоянно производя мегадозы кортизола, надпочечники постепенно истощаются и начинают резко снижать синтез кортизола, что приводит к синдрому хронической усталости, мышечным болям, деминерализации костей и полной потере интереса к жизни.
Самое большое, что вы можете сделать для вашего здоровья – это контролировать уровень стресса, а соответственно и уровень кортизола в крови. Фармакологическая индустрия предлагает богатый выбор антидепрессантов и релаксантов для нормализации самочувствия, но к сожалению, все они обладают побочными эффектами и развивают стойкую зависимость. Да и, как показывает практика, основную проблему таблетками не решишь. А вот осознанное бытие, контроль и коррекция своего поведения и собственной жизни приводит к желаемым и стойким результатам. Маленькие перемены ведут к большим изменениям, особенно, если это делать регулярно.
Маленькие перемены ведут к большим изменениям, особенно, если это делать регулярно.
Итак, как же контролировать уровень кортизола в крови:
1. Каждый день учитесь наблюдать за своим состоянием и оценивать его по 10- бальной шкале, где 10 баллов – это ваше идеальное физическое, эмоциональное и энергетическое состояние. Отмечайте что и кто у вас вызывает негативные эмоции и приводит к неконтролируему ментальному диалогу, который, в свою очередь, запускает физиологическую реакцию стресса и поднимает уровень кортизола. Находясь в позиции наблюдателя, вы учитесь управлять своими эмоциями и мыслями, не допуская нежелательных реакций тела. Будьте терпеливы к себе и окружающим. Несколько раз в день делайте паузы и глубоко дышите в течении 1-2 минут, помогая восстановить внутренний покой и умиротворение.
2. Молитесь .
Практикуйте спокойные физические упражнения, — расслабляющие практики не только успокаивают нервную систему, но и балансируют уровень нейротрансмитеров головного мозга – серотонина и допамина, ответственных за хорошее настроение. Побольше улыбайтесь, смейтесь, смотрите юмористические передачи и кинокомедии. Смех повышает уровень серотонина и снижает уровень кортизола. Относитесь к жизни легко, со здоровым чувством юмора, ведь все относительно!
Побольше улыбайтесь, смейтесь, смотрите юмористические передачи и кинокомедии. Смех повышает уровень серотонина и снижает уровень кортизола. Относитесь к жизни легко, со здоровым чувством юмора, ведь все относительно!
3. Утро вечера мудренее — гласит русская народная пословица . Полноценный ночной сон творит чудеса! Желательно быть в постели до десяти вечера и спать минимум 8-9 часов ежедневно. На ночь старайтесь не смотреть телевизор и не работать на компьютере, так как искусственный свет снижает активность гормона мелатонина, ответственного за полноценный сон. Крепкий сон гармонизирует работу нервной системы и способствует нормализации уровня кортизола.
4. Информация для любителей кофе :
каждая чашка кофе стимулирует выделение кортизола надпочечниками и, как следствие, вы сразу же ощущаете прилив сил и подъем настроения. К сожалению, этот эффект длится недолгое время, и вы тянитесь за второй чашкой кофе… Кроме поднятия уровня кортизола, кофеин сужает сосуды и обезвоживает организм. Даже небольшое количество кофе утром снижает эффективность вашего ночного сна.
Даже небольшое количество кофе утром снижает эффективность вашего ночного сна.
Кофеин стимулирует беспричинное беспокойство и вызывает мышечное напряжение (особенно в челюстной – лицевой области). Кроме того, кофеин нарушает нормальное всасывание многих витаминов и микроэлементов , приводя к минерально-витаминному голоданию организма.
Если вам сразу трудно отказаться от кофе, то хотя бы уменьшите его употребление до одной или половины чашки в день. Добавление в кофе корицы, кардамона или мускатного ореха значительно снижает негативное действие кофеина на организм.
5. Травотерапия :
многочисленными исследованиями доказано, что элеутерококк и радиола являются не только иммуномодуляторами, но и нормализуют работу надпочечников и регулируют уровень кортизола крови. Кроме того, они увеличивают стрессоустойчивость организма и регулируют аппетит. Стимулируя активность серотонина и допамина, элеутерококк и радиола повышают настроение, помогая справиться с депрессией. опубликовано
опубликовано
Стрессовые факторы воздействуют как на душевное состояние, так и на организм в целом. При травмирующих ситуациях запускаются биохимические изменения, которые могут привести к гормональному дисбалансу. Сбой вызывает различные реакции – увеличивается масса тела, ухудшается настроение, снижается иммунитет. Причиной этого явления становится кортизол, именно он назван .
Механизм выработки гормона стресса
О кортизоле наслышаны многие, но особенно волнует его присутствие женщин, так как имеется связь влияния гормона на увеличение веса. Как же вырабатывается и действует на организм кортизол?
Во время стресса человеческий организм переходит в состояние боевой готовности. Надпочечники отправляют гормон в кровь, в результате появляется энергия для противодействия.
При постоянной тревоге и отрицательных переживаниях количество кортизола увеличивается, что приводит к отрицательному воздействию на здоровье. Если в малых дозах стрессовый гормон регулирует состояние человека, то при высоких объемах он наносит вред. Как правило, серьезные нарушения связывают с .
Как правило, серьезные нарушения связывают с .
Помимо стресса, сбой в работе гормональной системы и увеличение кортизола вызывают большие дозы алкоголя, нарушения в работе яичников, плохая экология, употребление наркотических веществ.
Отрицательное влияние кортизола на организм
Гормональные нарушения на фоне избытка кортизола приводят к следующим осложнениям:
- увеличение жировой ткани в области талии как у женщин, так и у мужчин;
- повышается риск развития сердечно-сосудистых заболеваний, сахарного диабета;
- происходит сбой в работе щитовидной железы, ее функции подавляются;
- снижаются иммунные силы, в результате организм становится восприимчив к развитию инфекционных и простудных заболеваний;
- происходят нарушения в сонных циклах. Сон становится поверхностным, сбивчивым, после такого отдыха нет прилива сил;
- уменьшается плотность тканей, это приводит к риску получения травм, начинаются боли в спине и суставах;
- истончается кожный покров, начинается выпадение волос;
- повышение уровня холестерина, артериального давления.

Таким образом, гормональный сбой в связи со стрессом влияет практически на весь организм.
Влияние кортизола на организм женщины
Сильный стресс меняет гормональный фон, при этом его воздействию особенно подвержена часть женщин. Это влияние связано с особенностями женского организма. Повышенный уровень кортизола снижает полезное действие других гормонов, также существует связь между стрессом и гормонами яичника. Рассмотрим эти явления более подробно.
Признаки гормональных изменений на фоне стресса
Как определить ранние симптомы гормональных изменений по ?
Во-первых, у части женщин присутствует беспричинное беспокойство и учащенное сердцебиение перед началом менструального цикла. Волнение очень сильное и не дает расслабиться.
Во-вторых, повышенный уровень кортизола негативно влияет на сон. После ночного отдыха присутствует усталость, туман в голове, боли в мышцах.
В-третьих, присутствует снижение сексуального влечения, а также сбой в пищевом поведении. Часть женщин отмечают тягу к нездоровой пище, желание что-то все время есть.
Часть женщин отмечают тягу к нездоровой пище, желание что-то все время есть.
Итак, когда нарушается уровень гормонов, то это негативно отражается на здоровье и общем состоянии. Стресс обостряет заболевания, которые в спокойной фазе жизни не проявились бы. Гормональный сбой ухудшает самочувствие, усугубляются психологические переживания. Организм начинает подавать сигналы, пытаясь вернуть здоровье. От него требуется все больше жизненной энергии, наступает депрессия и эмоциональный спад. Специалисты советуют при перепадах настроения, раздражительности, упадке сил и других проявлениях обратиться к эндокринологу. Вполне возможны, что причины нездоровья кроются именно в гормональных сбоях.
Но в более серьезной, кризисной ситуации одновременно с ним активизируются ещё два гормона, адреналин и норадреналин. Вместе они оказывают на организм очень мощное воздействие и помогают ему справиться со стрессом.
Роль надпочечников
Когда человек оказывается в стрессовой ситуации, эндокринная система реагирует моментально и выбрасывает в кровь гормоны, основное действие которых является мобилизовать организм и помочь ему преодолеть проблему. При этом основные биологически активные вещества, действующие в этом направлении, вырабатывают надпочечники, которые являют собой две парные эндокринные железы, расположенные сразу над почками.
При этом основные биологически активные вещества, действующие в этом направлении, вырабатывают надпочечники, которые являют собой две парные эндокринные железы, расположенные сразу над почками.
Состоят надпочечники из двух частей и производят гормоны, которые действуют в трех направлениях. Биологически активные вещества, что синтезируются в клубочковой зоне, влияют на обмен веществ, гормоны, вырабатываемые в сетчатой зоне – на работу репродуктивной системы. Те из них, что помогают организму преодолеть кризисные ситуации и справляться со стрессом, производит пучковая зона (кортизол) и мозговое вещество надпочечников (адреналин и норадреналин).
Адреналин и норадреналин
В стрессовой ситуации адреналин и норадреналин усиливают и ускоряют сердцебиение, возбуждают нервную систему, повышают кровяное давление, сужают сосуды, расширяют зрачки, отключают все органы, что отвечают за пищеварение для обеспечения максимального тока крови к головному мозгу. Чтобы предоставить организму необходимое количество энергии, гормоны усиливают превращение гликогена в глюкозу.
В результате усталые мышцы забывают об усталости, и открывается «второе дыхание»: увеличивается работоспособность, улучшается умственная активность, четче воспринимается ситуация, наблюдается общий подъем тонуса и огромный всплеск энергии.
При этом адреналин считается гормоном страха, норадреналин – ярости, вместе они исполняют функцию под названием «нападай или беги», что даёт возможность человеку быстро среагировать, принять решение и предпринять действия, которые он не смог бы совершить в обычном состоянии. Действие этих гормонов длится не более пяти минут, затем их уровень спадает и возвращается в нормальное состояние. Если этого не происходит, их продолжительное влияние сильно истощает организм.
Функции кортизола
Кортизол обладает несколько иным действием: тогда как гормоны, что вырабатывает мозговое вещество надпочечников, мобилизуют все силы организма для того, чтобы справиться с ситуацией, глюкокортикоид (именно к этой группе относится кортизол) оказывает сильнейшее антистрессовое и противошоковое воздействие. Его количество резко возрастает при стрессах, потерях крови, травмах, в шоковом состоянии: так, организм адаптируется к ситуации.
В результате повышается артериальное давление, увеличивается чувствительность мышечного среднего слоя сердца и стенок сосудов к воздействию адреналина и норадреналина, при этом кортизон снижает чувствительность рецепторов, если гормоны мозгового вещества поднимаются на очень высокий уровень.
Кортизол, как и адреналин и норадреналин, повышает количество глюкозы в крови. Если гормоны мозгового вещества просто преобразуют гликоген в сахар, действие кортизола более широко: он способствует образованию глюкозы из неуглеводных соединений, тормозит захват и утилизацию сахара клетками периферических тканей, а также не даёт расщепляться глюкозе. Кортизол способствует задержке в организме воды, хлора, натрия и усиливает вывод кальция и калия.
Глюкокортикоид влияет активно и на деятельность других гормонов. Например, он тормозит синтез гормона роста, задерживая анаболические процессы и линейный рост, понижает чувствительность клеток к гормонам щитовидки, а также андрогенов и эстрогенов.
Поскольку кортизол стимулирует выработку глюкозы, он оказывает подавляющее воздействие на гормон инсулин, основной функцией которого является понизить уровень сахара в крови, и доставить глюкозу и другие питательные элементы ко всем клеткам тела.
Ещё одно отличие глюкокортикоидов в том, что если в результате действия адреналина и норадреналина сжигаются жировые запасы, и человек после спада этих гормонов чувствует голод, здесь наблюдается обратная картина: кортизол усиливает распад белков и способствует накоплению жиров. Если человек долго пребывает в стрессовой ситуации, кортизол постоянно держится на высоком уровне, что способствует увеличению массы тела.
Превышение нормы
Хотя адреналин, норадреналин и кортизол в первые секунды после выброса оказывают положительное влияние на иммунитет, поскольку обладают способностью снимать воспаление, противостоять аллергии, вирусам, бактериям и другим патогенным организмам, если через некоторое время их уровень не спадает, вся их польза исчезает.
Они будут продолжать тормозить деятельность внутренних органов, систем, ферментов, гормонов, которые были блокированы, чтобы организм справился с ситуацией. Это со временем спровоцирует в организме серьезные сбои.
Прежде всего, ухудшится состояние нервной системы, что крайне негативно отобразится на психике: человек станет раздражительным, беспокойным, нервным, перестанет адекватно воспринимать ситуацию, окажется подвержен приступам паники.
Основным виновником такого состояния является повышение уровня глюкозы: гормоны будут продолжать способствовать её выработке, в то время как действие инсулина, единственного вещества, что может снизить её уровень, будет блокировано кортизолом. Это приведет к избытку в организме энергии, которую необходимо будет выплеснуть, что и будет проявляться в нервных расстройствах.
Продолжительное воздействие адреналина нарушит работу сердечно-сосудистой системы, провоцирует развитие почечной недостаточности и другие заболевания внутренних органов. Также будут наблюдаться снижение массы тела, постоянные головокружения, человек будет ощущать потребность к постоянному действию.
Если речь идет о мелких неурядицах, которые нарушают работу нервной системы по нескольку раз в день, но не требуют больших выбросов адреналина, в крови преобладает кортизол. Именно гормон стресса является причиной ожирения, поскольку под его воздействием человек ощущает постоянное чувство голода (так, организм восполняет запасы, что были преобразованы в глюкозу).
Учитывая, что кортизол блокирует работу многих гормонов, которые принимают активное участие в жизнедеятельности организма, если стресс перейдет в хроническую стадию, это может спровоцировать:
- высокое кровяное давление;
- сбои в работе нервной и сердечно-сосудистой систем;
- ухудшение работы щитовидки, что означает снижение синтеза тиреоидных гормонов и кальцитонина, которые принимают активное участие в метаболизме, что приведёт к сбоям во всех системах организма;
- гипергликемию – повышенное содержание глюкозы в крови, следствием недуга является сахарный диабет;
- хрупкость костей;
- понижение иммунитета;
- разрушение тканей.
Точно определить, присутствует ли в организме гормональный дисбаланс и насколько велики его отклонения от нормы, можно с помощью анализа крови на гормоны. Необходимо иметь в виду, что препаратов, направленных на снижение уровня адреналина или кортизола, нет. Врач может назначить средства, предназначенные успокоить нервную систему. Но это рекомендуется лишь в крайнем случае, для начала советуют более щадящие методы.
Восстановление баланса
Чтобы восстановить гормональный баланс и привести в норму уровень адреналина, норадреналина и кортизола, необходимо исключить стрессовые ситуации. Если человек не в состоянии этого сделать, требуется предпринять действия, снижающие нагрузку на нервную систему. Снижают их концентрацию в крови занятия спортом или умеренные физические упражнения, продолжительные прогулки, полноценный отдых. Хорошо помогают упражнения йоги, созерцания, аутотренинг.
Успокаивающе воздействует на нервную систему фитотерапия с соответствующими травами (мята, валериана, шалфей). Рекомендуется диета, богатая на витамины и минералы с акцентом на овощи и фрукты и минимальным употреблением мяса, поскольку животные во время смерти испытывают сильнейший стресс, что приводит к выбросу в кровь соответствующих гормонов. Также нежелательно увлекаться продуктами с большим количеством сахара, поскольку концентрация глюкозы в крови и так достаточно высока.
Также врачи рекомендуют общение, это поможет избежать депрессии, поскольку человек, оказавшись в стрессовой ситуации, склонен уходить в себя, и сводит к минимуму общение с окружающими. Разговор с друзьями и знакомыми часто помогает снизить внутреннюю напряженность, даже если они не в состоянии будут помочь.
Помогают привести нервную систему в порядок и снизить уровень стрессовых гормонов, любимые занятия: рисование, музыка, водные процедуры, хобби. Нельзя подменять понятия и отдавать предпочтение курению или алкоголю: пользы они не принесут, зато спровоцируют развитие алкогольной и никотиновой зависимости.
В случае обнаружения у себя каких-либо симптомов заболеваний обращайтесь к вашему лечащему врачу. Копирование материалов сайта разрешено только в случае установки активной индексируемой ссылки на наш сайт.
Гормон стресса в крови — хотел как лучше, а получилось как всегда
Гормон стресса в крови вызывает в теле человека те же реакции, которые заставляли наших далеких предков сражаться или убегать при столкновении с хищниками или другими опасностями окружающей среды.
Для желез, вырабатывающих гормоны, несколько тысяч лет — не срок.
Так что именно им мы можем сказать «спасибо» за «легкое переигрывание» в ответ на стрессовые факторы.
Давайте же узнаем, какие гормоны вырабатываются при стрессе и что делать, чтобы эффективно возвращать организм в норму.
Share your Results:
Гормон стресса кортизол
Стероидный гормон кортизол — самый известный гормон стресса из всех ответственных за это неприятное состояние.
Как и все вещества, которые вырабатывает наше тело, он зачем-то нужен.
И вот зачем: в критические моменты кортизол берет под контроль баланс жидкостей и давление, гасит те функции организма, которые не играют большой роли в спасении жизни, и улучшает работу систем, которые могут нас спасти.
Таким образом, кортизол угнетает:
Не следует поддаваться стрессу и позволять им вами руководить
В краткие моменты опасности или тревоги это не играет роли, однако ситуация полностью меняется, когда вы находитесь под влиянием длительного стресса (что для современной жизни практически норма).
В таком случае повышенный уровень кортизола в крови заметно снижает эффективность, с которой иммунная система борется с инфекциями и вирусами.
Повышает давление до дискомфортного уровня, увеличивает количество сахара в крови, становится причиной половой дисфункции, проблем с кожей, ростом и т. д.
Диетологи отмечают, что гормон стресса кортизол вызывает желание постоянно есть что-нибудь высококалорийное и сладкое.
А они, в свою очередь, вносят свою лепту в и без того длинный список стрессовых факторов.
5+ способов снизить выработку кортизола
Прогулки на свежем воздухе оказывают положительное воздействие на организм
К счастью, мы не заложники кольца негативных последствий, к которым приводит высокий уровень гормона стресса кортизола.
Советы о том, как его уменьшить, помогут вам эффективно восстановить нормальную работу организма.
Итак, чтобы снизить выработку гормона на 12–16%, просто пожуйте жвачку! Это простое действие помогает отвлечься и расслабиться.
Отделы мозга, которые активизируются при запуске пищеварительной системы (а жевание является катализатором процесса), снижают нагрузку на надпочечники, вырабатывающие кортизол.
Если вы предпочитаете природные лакомства, съешьте пару ложек меда с грецкими орехами.
Он не только поможет нервам, но и укрепит иммунитет.
Совет: используйте жвачку, а не мелкий перекус, вроде печенья или бутерброда — так вы не наберете лишних калорий.
Химическая формула кортизола
Медитации помогают уменьшить выработку кортизола примерно на 20%.
Кроме того, регулярные практики релаксации снижают давление и помогают отвлекаться от тяжелых мыслей и стрессовых обстоятельств — на работе, в личной жизни и т. д.
Любые занятия, которые обращают ваше внимание на духовную сферу, в принципе отлично снижают стресс.
Вы можете выбрать то, что вам ближе:
- Прогулка на природе, вдали от городской суматохи
- Медитативное ручное творчество
- Посещение службы в церкви
- Восточные практики: йога, цигун, тай-чи и другие
Эффективным способом борьбы со стрессом, а, значит, и с выработкой кортизола, является массаж.
Расслабляющая сессия буквально физически поможет стряхнуть с плеч накопившиеся тревоги, увеличит содержание в крови так называемых гормонов счастья: дофамина и серотонина.
Медитируйте, чтобы снять стресс
Совет: если вы — приверженец активного образа жизни, не забывайте про спорт. Он действует подобным образом, заодно укрепляя ваше здоровье и увеличивая выносливость. Прекрасным выбором будет бег.
Высыпайтесь — или хотя бы не жалейте времени на дневную дрему. Сон имеет огромное значение для снижения уровня кортизола в крови.
Выспавшись, вы намного эффективнее решаете ежедневные проблемы, не позволяя им накапливаться в огромном коме стрессовых обстоятельств.
Отлично помогает вымотаться небольшая тренировка с гантелями дома.
Чашечка ароматного чая отлично поднимает настроение!
Натуральным релаксантом, который наверняка есть у вас дома, является обычный черный чай.
Заварите чашечку сладкого, ароматного чая и дайте себе несколько минут на спокойное чаепитие — оно поможет снизить уровень гормонов стресса в крови на 40–50%, благодаря действию флавоноидов и полифенолов.
Совет: выбирайте крупнолистовой чай вместо пакетированного — в нем присутствует намного больше полезных веществ.
И самый простой рецепт напоследок, который также является одним из наиболее эффективных: слушайте музыку!
Приятный, позитивный, расслабляющий или тонизирующий плейлист способствует секреции дофамина и серотонина и снижению выработки кортизола.
Особенно полезной во время стресса считается классическая музыка, активизирующая максимум отделов мозга и формирующая новые нейронные связи — буквально отращивая вам обновленные нервные клетки.
Музыка оказывает целебное воздействия на нервы
Адреналин: что такое стресс на самом деле
Адреналин как гормон стресса недвусмысленно намекает нам на природу тревожащих обстоятельств.
Как известно еще из школьной программы, адреналин вырабатывается, когда вы испуганы.
Он заставляет сердце и мышцы работать активнее, а мозг — сосредотачиваться на одной проблеме: как спастись из угрожающей ситуации.
Стоит ли с ней сражаться? Стоит ли бежать?
Под влиянием адреналина организм функционирует на пределе, ограничивая также ваш кругозор, креативность и способность расслабляться.
Повышенная нагрузка при длительном воздействии этого гормона приводит к чрезмерной утомляемости, головным болям: из-за концентрации на проблеме кажется, что ничего, кроме нее, в жизни не существует.
Как успокоиться и распрощаться с адреналином
Чтобы перестать бояться, необходимо в первую очередь бороться с причиной страха.
Присмотритесь к своей жизни: что вызывает у вас отчетливый дискомфорт?
Стрессовыми факторами могут быть:
- Работа
- Личная жизнь
- Финансовое состояние
- Неспокойная обстановка в местности, где вы живете
- Проблемы со здоровьем
Если вы испытываете сложности с самостоятельным выявлением проблемных областей жизни, поговорите с партнером, другом, которому вы доверяете, или обратитесь к специалисту.
Зачастую страх связан с опытом, происходящим из детства, и чтобы полностью избавиться от этого чувства, помощь психолога будет очень кстати.
Особенно опасен адреналин для беременных, в этом случае прибегнуть к помощи со стороны необходимо для здоровья малыша.
Говорите о своих проблемах с близкими. Это важно!
Совет: не нужно бояться похода к специалисту. Внимательно подберите врача и не стесняйтесь сходить на пробные консультации к нескольким из них, чтобы выбрать того, кто вызывает у вас доверие и расположение.
Кроме того, снизить выработку гормона стресса адреналина можно с помощью здорового сна и диеты, исключающей сладкое, жирное и мучное.
Гормон стресса у женщин
В женском организме есть еще один неожиданный враг, который при обычных обстоятельствах не несет ничего плохого — это пролактин.
В норме он отвечает за лактацию и естественно повышается во время беременности, после кормления ребенка грудью или после секса.
Однако в стрессовой ситуации выработка его может увеличиваться, превращая пролактин в гормон стресса.
Длительное воздействие пролактина на организм женщины приводит к проблемам с репродуктивной системой, нарушениям менструального цикла и овуляции, снижению уровня эстрогена и «отключению» полового влечения.
Наиболее страшным заболеванием, которое он может вызвать, является сахарный диабет.
Также пролактин угнетает действие дофамина, еще больше мешая вам получать удовольствие от того, что обычно радует — и тем самым увеличивая стресс.
Нормализация уровня пролактина
Главным помощником в борьбе с повышенным уровнем пролактина является дофамин.
Эти гормоны своеобразно соперничают в организме, и активизация производства дофамина угнетает выработку гормона женского стресса.
Занимайтесь тем, что приносит вам удовольствие, отводите время для хобби и отдыха — это будет первым шагом к нормализации вашего состояния.
Не оставайтесь со своими проблемами в одиночестве.
Огромное значение имеет правильное питание.
Необходимые вещества можно найти в разнообразных фруктах и ягодах:
Нелишним будет прием витаминов, особенно, если стресс настиг вас в осенне-зимний период.
Спасите себя от авитаминоза и помогите телу справиться с беспокойством!
Как предотвратить гормональный сбой при стрессе
Зная, как называются гормоны стресса, и как эффективно бороться с их повышенной выработкой в организме, можно быстро справиться с негативным состоянием.
Однако еще важнее знать, как не допустить гормонального сбоя — ведь так вы сможете бороться со стрессом еще до того, как он поглотит вас.
Главное правило — слушайте свое тело.
Давайте себе время на отдых и расслабление, занимайтесь спортом, правильно питайтесь и больше времени проводите на свежем воздухе.
Находите время для отдыха и восстановления сил
Не забывайте об общении, которое помогает психике разгрузиться и переключиться с тревоги на более позитивные переживания.
Делайте частые перерывы на отдых и используйте антистресс-игрушки для облегчения напряжения.
Совет: выбирайте встречи с людьми, которые вам приятны. Общество отталкивающих личностей может только усугубить состояние.
Не забывайте: вы можете управлять своим стрессом так же, как и удовольствием. А потому не давайте ему взять верх.
Будьте здоровы и счастливы!
Последние Новости
Рецепты соусов в домашних условиях — 30+ лучших
Свадебные прически на средние волосы — 100+ фото лучших укладок 2018
Стрижка лесенка на длинные волосы с челкой и без — главные тренды 2018 (50+ фото)
Микроблейдинг бровей — эффект до и после процедуры + фото
Камень александрит — 20+ фото, свойства и значение минерала для человека
Как заставить ребёнка учиться в школе и делать уроки — эффективные приемы
Как вырастить лимон из косточки в домашних условиях с плодами — правила + фото
Как вырастить авокадо из косточки в домашних условиях — 2 способа + пошаговое фото
Как ухаживать за розой в горшке в домашних условиях — 5+ правил
Блог о том, как сделать свою жизнь совершенней.
Советы, практики, рецепты, лайфхаки. Life Reactor — запускаем жизнь на полную!
Copyright. Life Reactor. Все права защищены
Гормоны стресса и их регуляция
Стресс может быть обусловлен различными причинами. Это могут быть личные проблемы (разрыв с любимым человеком, неприятности с детьми, заболевание), а могут быть и внешние обстоятельства, например, потеря работы. В такой ситуации в организме человека происходят различные биохимические процессы, которые могут оказать негативное влияние на здоровье, если их воздействие продолжается в течение длительного периода времени. Чтобы нейтрализовать последствия стресса, задействуются практически все системы человеческого организма, но наибольшую роль играет эндокринная. Именно в процессе ее работы выделяются различные гормоны стресса.
Роль адреналина в стрессе
Разбираясь, какие гормоны вырабатываются первыми, следует отметить, что это адреналин и норадреналин. Они участвуют в регуляции процессов организма в моменты пиковых нервных нагрузок. Они отвечают за запуск встроенных механизмов, которые адаптируют организм к состоянию стресса. Их вбрасывают в кровь надпочечники. Уровень адреналина резко растет в момент испытания тревоги, в условиях шока или, когда человек испытывает страх. Поступая в кровеносную систему и распространяясь по организму, адреналин приводит к учащенному сердцебиению, у человека становятся расширенными зрачки. При этом необходимо учитывать, что его длительное воздействие на системы человека приводят к истощению защитных сил.
Выделение же норадреналина сопровождается резким ростом артериального давления. Данный гормон стресса также выделяется в момент повышенных нервных нагрузок или, когда человек испытывает шок. С психологической точки зрения адреналин считается гормоном страха, а норадреналин – ярости. Оказывая различное воздействие на организм, оба гормона заставляют его системы работать практически на пределе возможного и, таким образом, с одной стороны, защищают организм от стресса, а с другой стороны помогают человеку выпутаться из сложной ситуации. Если выработка данных гормонов нарушена, поведение человека в стрессовой ситуации может быть неадекватным.
Механизм действия кортизола
Другой гормон стресса, который называется кортизол, и стресс практически неразлучны. Резкий рост уровня гормона наблюдается именно в моменты пиковых физических или эмоциональных нагрузок. Это является своего рода защитной реакцией организма. Влияя определенным образом на нервную систему, данный гормон побуждает мозг искать оптимальный выход из ситуации, он максимально активизирует его деятельность. Если для выхода из сложной ситуации требуются мышечные усилия, то кортизол может дать им неожиданный импульс. Именно действием данного гормона объясняются резкое увеличение скорости и умение лазать по деревьям у охотников, которые убегали от медведя. Или резкий прилив сил у матерей, которые оказались вынуждены защищать детей.
Действие кортизола состоит в том, что организм находит источники быстрой энергии, которыми является глюкоза или мышцы. Поэтому длительный стресс и, соответственно, поддержание уровня кортизола на высоком уровне на протяжении длительного времени могут привести к разрушению мышц (ведь постоянно они не могут снабжать человека энергией) и набору веса. Организм требует восстановления запасов глюкозы, и человека начинает увеличивать потребление сладкого, что и приводит к увеличению массы тела.
Последствия действия кортизола на организм
В нормальном состоянии, гормон стресса кортизол не только не вреден, но и полезен для нормального функционирования систем жизнедеятельности человека. Благодаря ему происходит регулирование баланса сахара, обеспечивается нормальный обмен веществ, выработка инсулина в нужных объемах и стабильное расщепление глюкозы. В условиях же стресса происходит резкое увеличение уровня кортизола. Как описано выше, краткосрочное влияние пиковой выработки гормона даже полезно, но при нахождении в состоянии стресса на протяжении длительного времени это наносит вред.
Постоянное повышение содержания кортизола в крови приводит к следующим последствиям:
- Повышенное артериальное давление, что негативно сказывается на самочувствии человека и может привести к негативным последствиям, вплоть до инсульта.
- Ухудшение работы щитовидной железы, что в перспективе может привести к снижению выработки инсулина и появлению сахарного диабета.
- Резкий рост уровня глюкозы в крови, что в совокупности с ухудшением работы щитовидной железы может привести к нарушению работы основных систем организма.
- Нарушение функционирования эндокринной системы в целом, что может привести, в том числе, к повышенной хрупкости костей и разрушению некоторых тканей организма.
- Уменьшение иммунитета из-за сбоя в работе систем жизнедеятельности человека.
Влияние кортизола на вес
Еще одно негативное влияние данного гормона на жизнь человека – это образование новых жировых тканей. При хроническом стрессе и постоянном повышенном уровне кортизола у человека развивается тяга к жирной и сладкой пище. Чтобы постоянно бороться со стрессовыми явлениями, организму необходимы запасы быстрой энергии – глюкоза и аминокислоты. Первая содержится в крови и поступает туда в результате потребления сахара или сладкой пищи, а второй компонент – в мышцах. Получается замкнутый круг. Организм требует сладостей, которые состоят из глюкозы и углеводов, глюкоза потребляется для борьбы со стрессом, а углеводы преобразуют в жир и накапливаются для создания резервов энергии. Причем такой жир ликвидировать достаточно сложно, он формируется у мужчин внизу живота, а у женщин – на бедрах. В этих местах убрать его очень сложно даже путем физических упражнений.
Более того, наличие высокого уровня кортизола часто и мешает сбросить лишний вес. Во-первых, организм подает сигналы, что ему необходимо дополнительное питание, что ведет к появлению чувства голода, а значит, вес не уменьшается. Во-вторых, под воздействием кортизола происходит разрушение мышц на аминокислоты, которые требуются для защитной реакции для борьбы со стрессом. Это приводит к тому, что на физические упражнения у человека сил не остается. Таким образом, человеку сложно сбросить вес, как с помощью физических нагрузок, так и путем диеты. Чтобы похудеть, необходимо сначала уменьшить содержание кортизола в организме.
Пролактин и стресс
Гормон стресса пролактин действует в большинстве случаев на женщин. Это связано с тем, что он связан с реализацией функции рождения детей. Уровень данного гормона у женщин также резко возрастает в период неожиданных психических нагрузок. Его негативное влияние заключается в том, что при длительном воздействии он приводит к нарушению овуляции, графиков менструации, а значит, проблемам с зачатием ребенка. Кроме того, он может привести к различным заболеваниям женских половых органов и системы размножения.
Пролактин повышается и в период беременности, что приводит к различным эмоциональным всплескам у женщин. Однако постоянный гормональный сбой может привести в последующем к проблемам с грудным вскармливанием. Поэтому, если в процессе беременности у женщины возникают признаки депрессии, следует обязательно сделать анализ на уровень содержания данного гормона. Своевременная реакция и назначение лекарственных препаратов будут способствовать рождению здорового ребенка и позитивному настроению будущей мамы.
Постоянный стресс у женщин, а значит, повышенное содержание пролактина в крови может привести не только к проблемам с беременностью, но и к другим критическим последствиям. Поэтому крайне важно научиться бороться со стрессом, смотреть на жизнь позитивно и избегать сильных нервных перегрузок.
Борьба со стрессом
Чтобы избежать проблем со здоровьем, вызванных гормонами стресса, необходимо научиться управлять своим психическим и нервным состоянием. Существует достаточно большое количество методов борьбы со стрессом и повышения стрессоустойчивости. Кто-то ежедневно проводить время наедине с собой в тихом спокойном месте, кто-то выезжает в пустое место и просто кричит, чтобы выплеснуть негативную энергию, а для кого-то лучший антистресс – поход в зал бокса. Главное найти свой способ и активно пользоваться им. Также необходимо помнить, что здоровый и спокойный сон – залог стабильной нервной и эндокринной систем.
Полезно заниматься спортом. При этом тренировки должны быть не до изнеможения, а просто достаточными. Слишком активные занятия спортом могут наоборот спровоцировать выброс кортизола и привести к набору веса, а не к положительному психотропному эффекту. В целом же участие в спортивных мероприятиях и регулярные физические нагрузки (особенно на свежем воздухе) способствуют выработке эндокринной системой эндорфинов – гормонов радости и счастья, значительно повышающих стрессоустойчивость.
Полезно слушать хорошую музыку, заранее распределять дела, чтобы исключить ощущение, что надо все сделать одновременно, а времени нет (это является одной из самых распространенных причин стресса). Также положительное влияние на психическую, нервную и эндокринную системы оказывает массаж, мануальная терапия, медитация, дыхательные упражнения.
Итак, при стрессе у человека протекают сложные биохимические процессы в организме, которые сопровождаются резким ростом выбора специальных веществ, которые называются гормонами стресса. С одной стороны, они формируют защитную реакцию, помогают быстро найти выход из сложной ситуации, но, с другой стороны, при длительном нервном напряжении стресс гормоны приводят к нарушениям в организме, разбалансированию его систем. Последствием постоянного стресса могут стать различные хронические и неизлечимые заболевания. Поэтому со стрессом нужно бороться и учиться управлять своим эмоциональным состоянием.
В современных условиях человек подвергается различным стрессовым условиям. Условия могут привести к изменениям концентрации многих гормонов стресса, в том числе кортизола, адреналина, дофамина, серотонина, гормона роста и пролактина. Некоторые из этих изменений необходимы чтобы защитить себя. Многие из этих стрессовых реакций могут привести к эндокринным нарушениям и изменить клиническое состояние существующих расстройств здоровья.
Стрессовое состояние можно определить как любую ситуацию, которая стремится нарушить равновесие между живым организмом и окружающей средой.
В повседневной жизни возникает много стрессовых ситуаций, таких как напряженная работа, экзамены, психологические вопросы, физические нагрузки из-за травм, операций и различных заболеваний.
Реакцией на внезапные события является повышенная секреция ряда гормонов стресса, действие которых заключается в увеличении мобилизации источников энергии и адаптации индивида к новым обстоятельствам.
Активация гипофиза мозга человека и надпочечниковой системы является видным нейроэндокринным ответом, способствующим выживанию. Ядро гипоталамуса мозга отвечает за комплексный ответ на стимуляцию производства гормона стресса. Это приводит к увеличению сердечного выброса и притока крови, снижению перистальтики кишечника, повышению глюкозы.
Гормоны как способ борьбы
За широкий спектр физических и психических реакций организма влияет целый ряд гормонов стресса, которые отвечают за добавление «топлива в огонь».
Адреналин
Широко известное биологически активное вещество управляющее функцией «нападать или бежать» производится надпочечными железами после получения сигнала от мозга, что стрессовая ситуация наступила.
Адреналин, совместно с норадреналином является основной причиной немедленной реакции.
Представьте, что вы пытаетесь изменить полосу движения вашего автомобиля. Вдруг из слепой зоны появляется автомобиль со скоростью 120 км в час. Сердце бьется чаще, мышцы напряжены, дышите быстрее, может начаться потливость. Это выделился адреналин.
Наряду с увеличением частоты сердечных сокращений, адреналин также дает прилив энергии, чтобы убежать от опасной ситуации и для сосредоточения внимания.
Норадреналин
Вещество похоже на адреналин и зависит от надпочечных желез и от мозга. Основная функция норадреналина, как адреналина, возбуждение и агрессия. Он также помогает перенести поток крови к более важных областям организма, чтобы подготовить мышцы, по принципу «нападай или беги».
Хотя норадреналин, может показаться излишним с учетом адреналина (который также иногда называют эпинефрин), оба гормона работают как тип системы резервного копирования и спасают людей от катастрофы как острая реакция на стресс.
В зависимости от долгосрочного воздействия гормонов это может занять от получаса до нескольких дней, чтобы вернуться в нормальное состояние покоя. В некоторых случаясь необходимы советы от стресса .
Кортизол
Стероидное биологически активное вещество, широко известно как гормон стресса, производится надпочечными железами.
Его производство занимает немного больше времени — минуты, а не секунды, чтобы почувствовать эффект потому что выпуск этого гормона занимает несколько этапов процесса с участием двух дополнительных незначительных гормонов.
Во-первых часть мозга, которая называется миндалины должна признать угрозу. Затем отправляет сообщение в часть мозга, называемый гипоталамус, который выпускает рилизинг гормон, указывающий надпочечным железам производить гормон стресса кортизол.
В обычном режиме жизни нормальное количество кортизола помогает поддерживать баланс жидкости и кровяное давление, а также регулирование некоторых функций организма, которые не являются решающими в момент, как иммунитет, пищеварение и рост.
Организм постоянно выпускает кортизол и хронически повышенный уровень может привести к серьезным проблемам. Слишком много кортизола может угнетать иммунную систему, повысить кровяное давление и сахар, снизить либидо, способствует акне, ожирению и многому другому.
Конечно, эстроген и тестостерон являются также гормонами стресса, которые влияют как мы реагируем на обстановку, как нейротрансмиттер допамин и серотонин.
Гормон роста
Гормон роста повышается во время острого физического стресса. Его уровень может увеличиться от двух до десяти раз
Пролактин
В зависимости от местной нормативно-правовой среды во время стресса уровень пролактина может либо увеличиться, либо уменьшиться. Это может повлиять на иммунную систему или некоторые аспекты саморегуляции и внутреннего состояния.
Инсулин
Инсулин может уменьшиться в случае опасности. Это может способствовать стресс-индуцированной гипергликемии.
Сахарный Диабет
Сильный стресс может быть фактором риска для диабета. Проведенные исследования показали, что реакция организма на воздействие различных неблагоприятных факторов у молодых в начале жизни может быть фактором риска для диабета. В более позднем возрасте у взрослых фактор риска получения сахарного диабета уменьшается.
Половые дисфункции
Гормон стресса у женщин может привести к ановуляции и другим нарушениям менструального цикла. У мужчин, может быть снижено количество сперматозоидов, подвижность и изменение морфологии, Расстройства эякуляции, импотенция могут быть связаны с психологическими факторами мужского бесплодия.
Эндокринные нарушения как реакция организма
Одной из основных причин, по которой у некоторых людей начинаются эндокринные нарушения (очищение и регуляция организма) из-за действия гормона стресса кортизола. Миллионы лет назад организм человека эволюционировал для быстрого реагирования на опасность. Как и дикие животные люди были в постоянной готовности, чтобы защищаться или убегать, если была угроза.
Когда мозг определяет, что жизнь находится в опасности, он стимулирует освобождение адреналина и кортизола. Эта реакция защиты или быстрого покидания места опасности невероятно умна и тщательно эффективна.
Реакция обеспечивает мгновенную энергию на 5-10 минут, позволяя оперативно реагировать на опасные ситуации.
В эти дни, многие из нас живут в условиях хронического стресса. Но организм человека не может сильно различать степень опасности как резкий рост долга, ярость начальника, семейные споры или серьезная жизненная опасность – организм готовится на вызов. Поэтому он реагирует точно так же, как это делает всегда.
Проблема современного образа жизни, что предполагаемая угроза почти непрерывна и поставляется без обоснований как любое действие.
Эта дополнительная энергия откладывается в виде жира и глюкозы, ей некуда деться приводя к эндокринным нарушениям.
После стрессовых событий кортизол в крови часто остается высоким на некоторое время, эффективно увеличивая аппетит, потому что тело думает, что должны заправляться после всех этих боевых действий или убегания. Это означает, что люди при постоянном напряжении довольно часто чувствуют себя постоянно голодными. Что еще хуже их тело призывает запастись продуктами, которые как организм думает будет наиболее полезным для своей деятельности – углеводы (как сахар) и жиры. Человек употребляет сахара, жирные продукты и нездоровую пищу, которую многие люди жаждут. Начинаются эндокринные нарушения.
Если после воздействия опасности человек не борется или убегает, а гормоны стресса поспособствовали выделению энергии, она сохраняется в виде жира в теле приводя к обменным нарушениям. И если человек ест что-то сладкое или жирное вследствие перенапряжения аппетит улучшается. Мозг продолжает предоставлять энергию, которую он думает что нужна и пытается сохранить жир для дальнейшего использования, создает тягу и повышает аппетит для обеспечения поставок необходимого топлива, если точнее потребления еды.
Таким образом, гормоны стресса в нормальной обстановке приводят к эндокринным нарушениям.
Рекомендуем также
Повышенный пролактин у мужчин
Для профилактики различных заболеваний нелишним будет знать, какие тайны может хранить человеческий организм, какие гормоны он вырабатывает и на что конкретно способна положительно или отрицательно влиять их выработка.О гормоне пролактин необходимо знать хотя бы потому, что излишняя его выработка у мужчин ведет к понижению либидо, уменьшению созревания сперматозоидов и, следовательно, прекращению детородной функции. Кроме того, отслеживается влияние гормона на работу печени и почек, а также процесса обмена веществ. Это вполне весомые доводы, чтобы уделить серьезное внимание проблеме повышеннного пролактина у мужчин.
Что такое пролактин
Пролактин – гормон, вырабатывающийся в передней доле гипофиза головного мозга. Нельзя сказать, что его физиологическая роль в организме мужчины изучена полностью, но все эффекты, производимые этим пептидным гормоном, связаны с функцией размножения. С функцией, которую пролактин выполняет в женском организме, все значительно проще – там он связан с процессом образования, накопления и выведения молока в молочных железах, повышением секреции молозива, превращением молозива в зрелое молоко.
Структура самого гормона достаточно сходна со структурой соматотропного гормона, который отвечает за рост организма, а его рецепторы располагаются в совершенно разных частях организма, кроме органов, отвечающих за производительность, это почки, печень, легкие, тимус, поджелудочная железа, надпочечники, селезенка, отделы нервной системы, скелетные мышцы и даже кожа.
При подозрении на бесплодие мужчины, помимо прочих, сдают анализ на уровень пролактина. Если уровень гормона завышен постоянно, врачи называют такое состояние гиперпролактинемией, и грозит оно в итоге полной дисфункцией половой системы.
Лечение повышенного пролактина
Как же можно уберечь свой организм от повышенного уровня пролактина? Надо отметить, что повышен он может быть как по физиологическим, так и патологическим причинам. После перенесенного стресса, чрезмерных физических нагрузок, будь то физическая работа, занятие спортом или процесс полового акта – возможно временное повышение этого гормона. Однако это будет как раз случай физиологический, а не патологический, поскольку спустя определенное время уровень пролактина должен прийти в норму. А вот если содержание гормона в организме завышено вследствие опухоли гипофиза или гипоталамуса, хронической болезни печени или почек, заболевания эндокринной системы, это патологический случай, требующий медицинского вмешательства. Повышение уровня пролактина могут вызвать некоторые лекарственные средства.
В любом случае, при возникновении каких-либо подозрений на неполадки с гормонами, в обязательно порядке обратитесь к урологу
Как бы там ни было, старайтесь беречь свое здоровье и не забывать о важности воспроизводительной функции! Воздерживайтесь от табакокурения и чрезмерного употребления спиртных напитков, не употребляйте никакие наркотики и психотропные вещества, избегайте возникновения стрессовых ситуаций. Забота о здоровье – забота о своем будущем и будущем вашего потомства!
Симптомы и причины гиперпролактинемии | Лечение гиперпролактинемии в Самаре
Гиперпролактинемия это повышение концентрации гормона пролактина в крови.
Пролактин наряду с лютеинизирующим (ЛГ) и фолликулостимулирующим (ФСГ) гормонами вырабатываются в эндокринной железе гипофиза.
Пролактин иногда называют еще «молочным гормоном», т. к. он стимулирует образование молока у женщин после родов. В меньших количествах этот гормон образуется в организме мужчин.
Пролактин, наряду с ЛГ и ФСГ регулируют половую жизнь и размножение. У женщин они стимулируют образование женских половых гормонов — эстрогенов и созревание яйцеклетки, а также регулируют менструальный цикл.
У мужчин эти гормоны стимулируют выработку мужского полового гормона — тестостерона, а также подвижность сперматозоидов.
Какие причины приводят к гиперпролактинемии?
Выделяют физиологическую и патологическую гиперпролактинемию.
- Действие физиологических факторов не связанно ни с какими заболеваниями и встречается у здоровых женщин. Так, уровень пролактина повышается во время сна, кормления грудью, стресса, усиленной физической нагрузки, при половом акте, при беременности и в послеродовом периоде.
- Патологическая гиперпролактинемия может быть органической и функциональной.
- Органическая вызывается опухолями гипофиза (микро- и макропролактиномами). Это доброкачественное образовоние, вырабатывающее пролактин. Аденомы растут очень медленно или не растут вообще. Что именно вызывает ее образование, пока еще до конца не ясно. Пролактиномы бывают различных размеров, но подавляющее большинство имеет диаметр менее 10 мм и называется микропролактиномами. Гораздо реже встречаются пролактиномы размером 10 мм и более, которые называются макропролактиномами. Симптомы пролактиномы зависят как от пола пациента, так и от размера опухоли.
- Функциональная гиперпролактинемия связана с различными заболеваниями: недостаточность функции щитовидной железы — гипотиреоз («Заболевания щитовидной железы и бесплодие»), хроническая почечная недостаточность, цирроз печени, синдром поликистозных яичников и др.
Гиперпролактинемия может возникать после операций и травм в области грудной клетки, частых выскабливаний полости матки.
Уровень пролактина может повышаться при приеме некоторых лекарственных препаратов в больших дозах: нейролептиков, антидепрессантов, гипотензивных средств, простагландинов, эстрогенов и пероральных контрацептивах.
Следует отметить, что довольно часто повышенный уровень пролактина встречается и при отсутствии видимой причины. Это так называемая идиопатическая форма гиперпролактинемии. Ее причина кроется в повышенной функции клеток гипофиза, количество которых при этом остается нормальным или увеличивается крайне незначительно.
Как проявляется гиперпролактинемия?
Повышение уровня пролактина в крови может проявляться по-разному.
У женщин наблюдается:
- недостаточность II фазы менструального цикла;
- задержки месячных или полное их отсутствие;
- нарушение овуляции;
- выделение молозива или молока из молочных желез (галакторея).
В мужском организме избыток пролактина приводит к уменьшению уровня тестостерона в крови, в результате чего снижается интерес к половой жизни (либидо), развивается импотенция и бесплодие («Мужское бесплодие»).
Как ставится диагноз гиперпролактинемии?
Ведущим методом в обследовании больных с гиперпролактинемией принадлежит гормональному обследованию — определению пролактина в крови. Забор крови производится из вены, в утренние часы, между 5-м и 8-м днями менструального цикла.
Как правило, при повышенном уровне гормона необходимы повторные определения (не менее 3-х). Это связано с возможностью временного повышения уровня пролактина, которое не говорит о наличии какого-либо заболевания.
Для диагностики органической гиперпролактинемии применяют обследование области гипофиза с помощью краниографии (рентгеновский снимок черепа в 2-х проекциях), компьютерной (КТ) и магнитно-резонансной томографии (МРТ).
Последние 2 метода обладают значительно большей точностью и информативностью.
Лечение гиперпролактинемии
Наиболее распространенным лекарственным средством для лечения гиперпролактинемии является бромокриптин и каберголин. Все эти препараты способствуют уменьшению выделения пролактина опухолью, уровень которого в крови часто снижается до нормы уже через несколько недель после начала лечения.
У женщин по мере нормализации пролактина восстанавливаются менструальный цикл и способность к зачатию. Беременность, кстати, может наступить достаточно быстро, поэтому, если Вы не планируете в данное время рождение ребенка, Вам следует обсудить с лечащим врачом наиболее подходящий способ контрацепции.
У мужчин вместе со снижением уровня пролактина возрастает уровень тестостерона, что нормализует качество половой жизни.
На фоне приема парлодела почти все пролактиномы уменьшаются в размерах. Если у Вас очень большая опухоль, может потребоваться проведение нескольких томографических снимков в динамике для оценки изменений размеров пролактиномы на фоне лечения.
В связи с эффективностью медикаментозного лечения при пролактиномах редко прибегают к операциям и лучевой терапии. Лишь небольшой части больных с макропролактиномами, у которых размер опухоли не уменьшается на фоне медикаментозного лечения, может понадобиться операция или лучевая терапия.
В Диагностической Лаборатории Вы можете пройти обследование для определения концентрации гормонов в крови.
При повышении уровня пролактина, а так же при бесплодии Вы можете проконсультироваться у врача акушера-гинеколога (репродуктолога).
Высокий уровень пролактина. Лечение в клинике Агада.
Уровень пролактина.
Гиперпролактинемия появляется при высоком уровне содержания гормона пролактина в крови. Это может быть как вариантом нормы, так и проявлением болезни. Пролактин вырабатывается гипофизом. Нормальные значения пролактина различаются у мужчин и женщин, они также отличны у людей разного возраста. Максимальный результат в анализах по этому показателю у женщин детородного возраста. После наступления климакса уровень пролактина снижается в 1,5–2 раза. Выделение пролактина в течение дня происходит циклически. Наиболее высокий уровень наблюдается ранним утром часы, а наименьший с 9 до 11 часов утра.
Действие пролактина на организм.
Биологическая функция пролактина заключается в поддержке деторождения, его главное действие заключается в становлении и регуляции лактации. Гормон участвует в формировании молочных желез, способствуя росту млечных протоков во время беременности и в подростковом возрасте. Пролактин стимулирует выработку грудного молока и способствует естественному вскармливанию детей. Воздействие пролактина на организм не ограничено молочными железами. Он оказывает влияние на поджелудочную и щитовидную железу, надпочечники, яичники. В надпочечниках пролактин увеличивает выработку адреналина, норадреналина, кортизола, андрогенов, альдостерона. Все эти гормоны помогают кормящей женщине легче переносить эмоциональные и физические перегрузки. Под действием этого гормона в поджелудочной железе возрастает функционирование клеток, производящих инсулин, благодаря чему поступающие в организм питательные вещества используются максимально полно. Воздействие пролактина на щитовидную железу позволяет уменьшить синтез кальцитонина, а значит, увеличить содержание минеральных веществ в грудном молоке. К пролактину особенно чувствительны яичники. Высокая концентрация гормона тормозит овуляцию и вызывает нарушение менструального цикла. Пролактин регулирует работу иммунной системы, позволяя плоду развиваться в матке без реакции отторжения. Пролактин в высоких дозах подавляет либидо, также он участвует в наступлении оргазма. Повышение содержания пролактина в организме происходит во время беременности и в период грудного вскармливания, это нужно для рождения и нормального развития ребенка.
Причины повышения пролактина.
Причины гиперпролактинемии могут быть органическими при заболеваниях гипофиза или функциональными при заболеваниях других органов. Поражения гипофиза приводят к большому увеличению уровня пролактина. Причиной органической гиперпролактинемии чаще всего является микроаденома гипофиза, при этом его концентрация может превышать 2000–4000 мМЕ/л. Функциональная гиперпролактинемия может появиться как реакция на длительный и сильный стресс. Кратковременное повышение уровня пролактина, как правило, без клинических проявлений называется транзиторной гиперпролактинемией. Это состояние может быть связано с нарушением сна, половым актом или приемом пищи. В некоторых случаях врачи не могут установить причину повышения уровня пролактина.
Повышенный пролактин. Симптомы у мужчин и женщин.
Гиперпролактинемия может как минимально влиять на самочувствие человека, так и давать крайне тяжелые проявления. Самыми распространенными жалобами у мужчин с повышенным уровнем пролактина являются жалобы на снижение потенции. У женщин первым симптомом чаще всего являются жалобы на выделения из молочных желез. Симптомы гиперпролактинемии у женщин: отсутствие менструаций; нарушения менструального цикла, сухость влагалища, боль при половом акте, ановуляция и бесплодие. Симптомы гиперпролактинемии у мужчин: гинекомастия, уменьшение активности сперматозоидов, импотенция. Значительно чаще это заболевание встречается у женщин. Подтверждения диагноза у пациента проводится при помощи анализа на пролактин. При выявлении повышенного уровня, рекомендуется сдать гормоны щитовидной железы, анализ на сахар крови, пройти магнитно-резонансную или компьютерную томографию гипофиза.
Повышенный пролактин у женщин — симптомы, причины, последствия
Повышенный пролактин у женщин приводит к развитию симптомов гиперпролактинемии. Заболевание известно со второй половины девятнадцатого века. Сегодня существует достаточно много методов его лечения.
Что собой представляет пролактин
Пролактин – гормон, экспрессия которого наряду с лютеинизирующим и фолликулостимулирующим гормонами происходит в гипофизе. Это вещество полипептидной природы, молекула которого состоит из ста девяноста восьми аминокислот и трёх дисульфидных мостиков. Он в небольших количествах секретируется в кровь. Выброс гормона осуществляется в строго определённом суточном ритме, максимальное его количество в крови – во время сна. В это время его концентрация в семь раз выше, чем днём.
Пролактин по принципу обратной связи сам влияет на собственную экспрессию. Он по принципу обратной связи действует на клетки гипоталамуса и способствует освобождению из них дофамина, который из серобугорных и паравентрикулярного ядра гипоталамуса поступает в гипофиз и связывается с рецепторами на лактотропных клетках. Таким образом, ингибируется не только секреция пролактина, но и гонадотропов. При нарушении механизмов регуляции у женщин появляются симптомы повышенного уровня гормона.
В регуляции уровня пролактина участвуют две группы факторов:
- ингибирующие этот процесс: ГАМК, дофамин, гастрин, соматостатин, гастрин-релизинг-пептид, а также гистидил-пролил-дикетопиперазин;
- стимулирующие продукцию гормона: тиролиберин, бомбезин, серотонин и вазоинтестинальный пептид, опиаты, а также люлиберин и нейротензин.
Его секрецию усиливают эстрогены и тиролиберина. Она также повышается под воздействием нервных импульсов от сосков. Пролактин способствует подготовке молочных желез к лактации, поэтому его концентрация в крови постоянно увеличивается во время беременности и становится высокой в третьем триместре. Это и есть физиологическая гиперпролактинемия. Когда уровень гормона в сыворотке крови становится высоким вне беременности, говорят о патологической гиперпролактинемии.
Повышенный пролактин у женщин. Причины
К повышению уровня пролактина у женщин приводят много разнообразных факторов. Физиологическая гиперпролактинемия развивается у женщин, не страдающих никакими заболеваниями, которые могли бы вызвать повышенный уровень данного гормона. Причина этому – сон, кормление грудью, стресс и усиленная физическая нагрузка. Повышается его концентрация в сыворотке крови женщины во время полового акта, при беременности и после родов.
Патологическая гиперпролактинемия бывает органической и функциональной. Доброкачественные опухоли гипофиза вырабатывают данный гормон. Они могут либо расти медленно, либо вовсе не прогрессировать. Размер большинства из них не превышает десяти миллиметров. Они называются микропролактиномами. Макропролактиномы – это новообразования гипофиза, размер которых более десяти миллиметров. Они встречаются довольно редко. Симптомы повышенного уровня пролактина у женщин могут появляться как у мужчин, так и у женщин. Они зависят от размера новообразования.
Причиной функциональной гиперпролактинемии являются многие заболевания:
- гипотиреоз – недостаточность функции щитовидной железы;
- цирроз печени;
- хроническая почечная недостаточность;
- синдром поликистозных яичников.
Гиперпролактинемия может возникнуть после травм и операций в области грудной клетки, а также частых выскабливаний полости матки. Повышенный уровень этого гормона у женщин и мужчин имеет место при приёме больших доз антидепрессантов, нейролептиков, простагландинов, гипотензивных средств, пероральных контрацептивов и эстрогенов. Известна также идиопатическая форма гиперпролактинемии, когда повышенная концентрация пролактина у женщин встречается без видимых причин. Это происходит в связи с повышенной функциональной активностью клеток гипофиза, количество которых остаётся при этом нормальным или крайне незначительно увеличивается.
Повышенный пролактин у женщин. СимптомыСимптомы данной патологии у женщин и мужчин бывают разными. Так, например, женщины, страдающие гиперпролактинемией, жалуются на задержку или полное отсутствие месячных, галакторею (выделение молока или молозива из грудных желез). У них имеет место недостаточность второй фазы менструального цикла и нарушение овуляции. Часто гиперпролактинемия становится причиной бесплодия.
Другим симптомом у женщин часто является гирсутизм. При гиперпролактинемии начинают интенсивно расти волосы на лице, вокруг сосков и по белой линии живота. Может появиться угревая сыпь (акне). По причине снижения плотности костной ткани развивается остеопороз.
Пациентки, страдающие подобной патологией, склонны к ожирению из-за повышенного аппетита. У них отмечаются психоэмоциональные нарушения. Часто нарушается сон, ослабевает внимание и память, появляются депрессивные состояния и повышенная утомляемость. Могут иметь место нарушения функции зрения.
В связи с гормональным дисбалансом появляется повышенная потливость, может беспричинно повышаться температура тела, беспокоить тошнота, постоянный гул в голове и головокружение, а также боль в грудной клетке. Пациентки жалуются на сонливость, их лицо может быть гиперемированным. Если причиной гиперпролактинемии является опухоль гипофиза, то в связи со сдавлением перекреста зрительного нерва наступает резкое ухудшение остроты зрения, может иметь место паралич черепно-мозговых нервов.
В организме мужчин повышенная концентрация пролактина в сыворотке крови приводит к уменьшению уровня мужского полового гормона тестостерона в крови. У них снижается либидо (половое влечение), развивается эректильная дисфункция. Мужчины, страдающие гиперпролактиемией, часто бесплодные.
Повышенный пролактин у женщин. Последствия
Наиболее тяжёлым последствием подобной патологии является бесплодие. Неспособность к зачатию развивается по причине нарушения гормонального гомеостаза, нарушения менструального цикла и развития синдрома поликистозных яичников. Дело в том, что при повышенной концентрации пролактина в крови он сам же подавляет синтез этого гормона, а вместе с ним и продукцию гонадотропов, экспрессия которых также происходит в гипофизе.
Фолликулостимулирующий и лютеинизирующий гормоны регулируют функцию яичников. В случае изменения их концентрации в крови не происходит овуляция и тормозится развитие фолликулов. В этом случае не созревает яйцеклетка и развивается эндокринное бесплодие.
Последствие повышенного уровня данного гормона у мужчин – то же бесплодие по причине низкой концентрации тестостерона. Это приводит к нарушению сперматогенеза и эректильной дисфункции. Тогда последствием повышенной концентрации пролактина становится нарушение психоэмоционального состояния, которое рано или поздно приводит к депрессии.
Диагностика гиперпролактинемии
О повышенном уровне пролактина в крови женщин и мужчин можно говорить на основании результатов анализа. Для определения его уровня в сыворотке крови производят забор венозной крови. Накануне исследования женщина не должна заниматься физическим трудом и сексом. Не разрешается также стимуляция сосков молочной железы. Ей следует воздержаться от тепловых процедур и инсоляции. Также за сутки до исследования женщину следует оберегать от эмоциональных нагрузок.
Кровь сдают натощак. Это лучше делать между пятым и восьмым днями менструального цикла. Оптимальным временем для сдачи крови считаются первые три часа после сна, но не позже десяти часов утра. Если же по какой-то причине в это время кровь сдать не удалось, то женщине в течение шести часов следует воздержаться от приёма пищи, а затем прийти в лабораторию.
Референсные значения уровня пролактина в сыворотке крови женщин находятся в диапазоне от 109 до 557 мЕд/л, а у мужчин от 73 до 407 мЕд/л. Тем не менее, в разных диагностических учреждениях могут использовать неодинаковые методы исследования, поэтому цифры могут отличаться. По этой причине на бланке лаборатории, которая проводила исследование, должны быть указаны референсные значения, принятые в конкретном диагностическом учреждении. Норма гормона в крови беременных и кормящих грудью женщин, а также у детей, иная.
Расшифровка результатов проводится врачом лаборантом. Повышенная концентрация пролактина в сыворотке крови характерна для таких заболеваний:
- опухоли гипофиза и гипоталамуса;
- гипотиреоз;
- поликистоз яичников;
- аутоиммунные заболевания;
- эстрогенпродуцирующие опухоли.
Сниженная концентрация гормона определяется при истинном перенашивании беременности и синдроме Шихана. При отклонении полученных результатов исследования от референсных значений надо повторить исследование не менее трёх раз. Это делается с целью исключения физиологического или идиопатического повышения уровня пролактина, которое никоим образом не связано с наличием патологического процесса.
Вторым методом исследования, который помогает выяснить причину гиперпролактинемии, является исследование черепа рентгенологическими методами. С этой целью выполняют краниографию (рентгеновский снимок черепа в двух проекциях), компьютерную и магнитно-резонансную томографию. Последние два метода более информативны и точны.
Также необходимо выполнить женщине ультразвуковое исследование органов малого таза, определить состояние и соотношение других гормонов. У мужчин целесообразно выполнить УХИ органов мошонки и определить концентрацию тестостерона. Если речь идёт о бесплодии, то необходимо исключить другие факторы этого состояния.
Лечение гиперпролактинемии
Наиболее часто для лечения пациентов, страдающих гиперпролактинемией, является бромокриптин, более известный под коммерческим названием парлодел. Также врачи назначают при повышенном уровне пролактина каберголин (достинекс) и норпролак. Эти препараты влияют на опухоль гипофиза и способствуют уменьшению выделения ею пролактина. Терапевтический эффект препаратов наблюдается спустя несколько недель от начала лечения.
Как только уровень этого гормона в крови приходит к норме, у женщины восстанавливается менструальный цикл. Она вновь может зачать, причём, беременность может наступить достаточно быстро. У мужчин по мере нормализации его уровня повышается концентрация тестостерона, либидо и эрекция. Положительным моментом является то, что на фоне приёма препаратов происходит уменьшение объёмов пролактином. Это можно увидеть во время мониторинга при помощи рентгенологических методов исследования.
Для лечения пролактином, которые в большинстве случаев являются причиной гиперпролактинемии, редко применяют лучевую терапию или прибегают к оперативному их удалению. Такое лечение может понадобиться только пациентам, у которых диагностированы макропролактиомы, не чувствительные к бромокриптину.
Гиперпролактинемия – заболевание, которое подлежит лечению. Если у вас возникла в этом необходимость, обращайтесь в «Центр ЭКО» в Калининграде. Наши специалисты проведут необходимое обследование, выяснят причину заболевания и назначат эффективное лечение.
Запишитесь на прием по телефону
+7 (4012) 92-06-76
или
воспользуйтесь формой записи:От физиологической адаптации к стрессу и нейрогенеза к психопатологии
Фронт-эндокринол (Лозанна). 2016; 7: 25.
Лус Торнер
1 Neuroendocrinología, Departamento de Neurociencias, Centro de Investigación Biomédica de Michoacán, Instituto Mexicano del Seguro Social, Морелия, Мексика
Neología de Neología de Neología, Departamento Departament де Мичоакан, Instituto Mexicano del Seguro Social, Морелия, Мексика
Отредактировал: Дебора Сучеки, Федеральный университет Сан-Паулу, Бразилия
Рецензент: Кэрол Ф.Элиас, Мичиганский университет, США; Габор Б. Макара, Венгерская академия наук, Венгрия
Специализированный раздел: Эта статья была отправлена в раздел «Нейроэндокринная наука» журнала «Границы эндокринологии»
Поступила в редакцию 18 августа 2015 г .; Принято 14 марта 2016 г.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора (авторов) или лицензиара и ссылки на оригинальную публикацию в этом журнале в соответствии с принятой академической практикой.Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья цитируется в других статьях в PMC.Abstract
Пролактин (ПРЛ) — один из самых универсальных известных гормонов. Он считается адаптивным гормоном из-за ключевой роли, которую он играет в модуляции реакции на стресс, а также во время беременности и кормления грудью. Внутри мозга ПРЛ действует как нейропептид, стимулируя физиологические реакции, связанные с воспроизводством, адаптацией к стрессу, нейрогенезом и нейрозащитой.Действие ПРЛ на нервную систему способствует широкому спектру изменений, которые происходят в женском мозге во время беременности и приводят к ослаблению оси гипоталамус-гипофиз-надпочечники. Вместе все эти изменения способствуют поведенческой и физиологической адаптации новой матери, чтобы обеспечить репродуктивный успех. Адаптации мозга, вызванные ПРЛ, также важны для регуляции материнской эмоциональности и благополучия. ПРЛ также влияет на мужской мозг во время стрессовой реакции, но его эффекты менее изучены.ПРЛ регулирует нейрогенез как в субвентрикулярной зоне, так и в гиппокампе. Следовательно, изменения в системе ПРЛ из-за стресса или воздействия веществ, которые снижают нейрогенез или другие состояния, могут способствовать дезадаптивным реакциям и патологическим поведенческим результатам. Здесь мы рассмотрим систему ПРЛ и ее роль в модуляции реакции на стресс и регуляции эмоций. Мы обсуждаем влияние ПРЛ на нейрогенез и нейрозащиту, предполагаемые нейронные механизмы, лежащие в основе этих эффектов, и их вклад в возникновение психопатологических состояний, таких как депрессия.
Ключевые слова: тревога, депрессия, рецепторы пролактина, расстройства настроения, нейрогенез
Введение
Пролактин (ПРЛ) — плейотропный гормон гипофиза с более чем 300 известными физиологическими эффектами. Этот белковый гормон регулирует воспроизводство, иммуномодуляцию, ангиогенез, энергетический метаболизм, осмотический баланс и развитие. Помимо своих периферических функций, ПРЛ также играет много важных ролей в качестве нейропептида. ПРЛ проникает через гематоэнцефалический барьер, а локальная продукция гипоталамуса способствует достижению нескольких областей мозга, вызывающих сильные модулирующие эффекты.В частности, ПРЛ вносит вклад в регуляцию стрессовых реакций посредством ингибирования оси гипоталамус-гипофиз-надпочечники (HPA). Более того, ПРЛ модулирует тревожность и депрессивное поведение. ПРЛ также регулирует нейрогенез, генерацию новых нейронов как в субвентрикулярной зоне (SVZ), так и в гиппокампе. Уровни ПРЛ и условия окружающей среды могут вызывать изменения в нейрогенезе, потенциально влияя на эмоциональное поведение. Действительно, снижение уровня ПРЛ на ранних сроках беременности влияет на нейрогенез обонятельной луковицы и увеличивает послеродовую тревогу у самок крыс.Кроме того, ПРЛ может оказывать нейропротекторное действие в гиппокампе взрослых животных, подвергшихся хроническому стрессу или подвергнутых инфузии каиновой кислоты в гиппокамп. Однако ПРЛ снижает нейрогенез при введении на ранних стадиях развития и способствует депрессивному поведению во взрослом возрасте. Некоторые из этих эффектов опосредованы активацией различных нейрональных сигнальных систем и ионных каналов. Здесь мы суммируем некоторые аспекты действий ПРЛ в головном мозге и их вклад в возникновение психопатологических состояний, таких как депрессия.
Система пролактина
Синтез ПРЛ
Пролактин вырабатывается в основном лактотрофными клетками передней доли гипофиза. ПРЛ находится под ингибирующим контролем дофамина, высвобождаемого тубероинфундибулярными дофаминергическими (TIDA) нейронами (1). Несмотря на многочисленные попытки картировать ПРЛ в церебральных областях с использованием нескольких методов, синтез ПРЛ в головном мозге оказался под вопросом. PRL-положительные нейроны были локализованы методом иммуноцитохимии у самцов и самок разных видов (2).МРНК ПРЛ была обнаружена с помощью ПЦР в паравентрикулярном ядре (ПВЯ) и супраоптическом ядре (3) и с помощью кПЦР в гипоталамусе самок крыс (4). In situ гибридизация показала экспрессию ПРЛ в медиальной преоптической области (MPOA), перивентрикулярном преоптическом ядре, ядре ложа концевой полоски, PVN и латеральной перегородке у домашней индейки, а также у эмбрионов и взрослых овец (5 , 6). Недавние исследования с использованием методов микроматрицы обнаружили экспрессию ПРЛ в гиппокампе устойчивых мышей (7).
Периферический ПРЛ считается основным эффектором в головном мозге. Было высказано предположение, что ПРЛ может пересекать гематоэнцефалический барьер посредством рецепторно-опосредованного механизма, происходящего в клетках сосудистого сплетения (8). Однако недавние исследования с использованием мышей с нокаутом рецептора PRL (PRL-R) показали, что транспорт PRL зависит не от PRL-R, а от другого, еще не идентифицированного механизма (9). Через 30 минут после периферического введения ПРЛ активирует нейроны мозга за счет индукции фосфорилирования сигнального преобразователя и активатора транскрипции 5 [pSTAT5 (9)].Пики ПРЛ в спинномозговой жидкости (ЦСЖ) через 30 мин (10) или 90 мин (9) после его периферического введения. Эти последние исследования также предполагают, что ПРЛ не попадает в мозг после попадания в спинномозговую жидкость (9). Поскольку иммунореактивный ПРЛ наблюдался в сосудистом сплетении и эпендимных клетках желудочков головного мозга, было высказано предположение, что ПРЛ может транспортироваться из этих участков для достижения своих целевых областей (11, 12). Однако до сих пор неизвестно, как ПРЛ получает доступ к своим отдаленным целевым областям в головном мозге.Принимают ли эпендимные клетки или нейроны ПРЛ и высвобождают его в непосредственной близости от своих клеток-мишеней, или если ПРЛ высвобождается во внеклеточное пространство, чтобы диффундировать, пока не достигнет его рецепторов, все еще остается предметом споров.
Рецепторы ПРЛ
Рецепторы пролактина относятся к суперсемейству цитокиновых рецепторов класса 1 (1). PRL-R кодируется одним геном, но альтернативный сплайсинг дает несколько изоформ PRL-R. И у человека, и у крыс три изоформы (длинная, промежуточная и короткая — e.g., размер внутриклеточного домена). Ответ запускается после димеризации рецепторов с образованием гомодимеров. Длинно-длинные димеры способны активировать пути вторичных мессенджеров, в частности, сигнальный каскад преобразователя JAK-сигнала и активатора транскрипции (JAK-STAT) посредством активации STAT3 и STAT5. Короткая изоформа PRL-R активирует путь митоген-активируемой протеинкиназы (MAPK) (13). И длинные, и короткие гетеродимеры рецепторов ингибируют передачу сигналов ПРЛ (14) и способствуют модуляции действий ПРЛ.
Реакция на стресс и ПРЛ
Стресс — критический фактор, который может привести к депрессивным расстройствам. Воздействие стресса активирует ось HPA, вызывая высвобождение кортикотропин-рилизинг-гормона (CRH) в PVN, который способствует секреции адренокортикотропина (ACTH) из гипофиза. В свою очередь, АКТГ запускает выброс глюкокортикоидов из надпочечников. ПРЛ также секретируется гипофизом в ответ на ряд стрессорных факторов. Первоначальные исследования показали, что ПРЛ может противодействовать воздействию глюкокортикоидов на иммунную систему во время стрессовой реакции (15).Однако более поздние исследования показали, что предотвращение экспрессии PRL-R в мозге с помощью антисмыслового зонда сильно увеличивает вызванную стрессом секрецию АКТГ у девственных и кормящих крыс, предполагая, что ПРЛ играет ингибирующую роль в реактивности оси HPA (16, 17 ). Была выдвинута гипотеза, что ПРЛ модулирует активность оси HPA за счет уменьшения нервных входов в PVN. Как острые, так и хронические интрацеребровентрикулярные введения ПРЛ у девственных самок крыс снижают активацию нейронов миндалины и экспрессию гипоталамуса CRH в ответ на стресс (18).Кроме того, ПРЛ локально высвобождается из PVN и MPOA в ответ на физиологические стимулы, включая стресс (4).
Пролактин недавно был связан с устойчивостью в модели хронического легкого стресса (CMS). Взрослые крысы, ранее подвергавшиеся CMS, были выбраны как отвечающие и не отвечающие на лечение в соответствии с их реакцией на стресс. Устойчивые животные (т. Е. Не отвечающие) имели более высокие уровни ПРЛ в плазме и более высокие уровни мРНК ПРЛ-Р в сосудистом сплетении, чем у их уязвимых (т.е., респонденты) аналог (19). Соответственно, исследование микроматрицы, проведенное на гетерозиготных 5-Htt-дефицитных потомках, подвергшихся пренатальному стрессу, показало, что ПРЛ, гормон роста и рецептор галанина 3 по-разному экспрессируются в гиппокампе устойчивых мышей по сравнению с контролем (7). Эти результаты предполагают роль ПРЛ в регуляции стресса на уровне гиппокампа.
ПРЛ и эмоциональная реакция
Эффекты ПРЛ на тревожность и депрессивное поведение были изучены, но они различаются в зависимости от используемых видов и физиологического состояния.
ПРЛ и тревога
Внутрицеребровентрикулярное или внутривенное введение ПРЛ оказывает дозозависимый анксиолитический эффект как у самцов, так и у девственных самок крыс (16). Уровень тревожности у беременных и кормящих крыс постепенно снижается (20, 21). Эти эффекты, вероятно, опосредуются ПРЛ, о чем свидетельствует повышенная тревожность, проявляемая кормящими самками крыс в приподнятом крестообразном лабиринте после блокады экспрессии ПРЛ-Р в головном мозге (17). Было показано, что хроническое ICV-введение ПРЛ крысам-самкам с удаленной овариэктомией (используемым для моделирования эндокринного статуса во время беременности) снижает уровень тревожности в приподнятом крестообразном лабиринте (18).Взятые вместе, эти результаты убедительно свидетельствуют о том, что ПРЛ оказывает анксиолитическое действие на грызунов.
Исследования инбредных линий грызунов показали связь между повышенным уровнем ПРЛ и повышенной тревожностью. Сообщалось о повышенных базальных и стресс-индуцированных уровнях ПРЛ у крыс-самцов, разводимых с высоким тревожным поведением (HAB), по сравнению с крысами с низким тревожным поведением (LAB) (22). Римская линия крыс с низким уровнем избегания (RLA / Verh) (т. Е. Крысы, отобранные для низкой производительности в двустороннем тесте активного избегания) демонстрирует повышенные реакции на стресс, более высокие уровни ПРЛ и пассивный стиль совладания по сравнению с римскими высокими. линия крыс-избегание (RHA / Verh) (i.е., крысы, отобранные для достижения высоких результатов в тесте двустороннего активного избегания) аналог (23). Повышенные уровни ПРЛ, обнаруженные в этой линии животных, могут быть результатом дисбаланса одного или нескольких стимуляторов секреции ПРЛ (серотонина, ГАМК и т. Д.). В качестве альтернативы, высокие концентрации ПРЛ могут помочь улучшить избыточную реактивность оси HPA, наблюдаемую у этих животных. Напротив, клинические исследования на людях показали корреляцию между высокими уровнями ПРЛ и психологическим стрессом. Пациенты женского пола с гиперпролактинемией обычно сообщают о большем количестве симптомов тревоги и враждебности, чем женщины контрольной группы (24).
ПРЛ и депрессивные состояния
Было показано, что искусственное индуцирование гиперпролактинемии у взрослых самцов крыс путем помещения трансплантатов гипофиза крысы-донора в почку животного-рецептора оказывает антидепрессивный эффект в тесте принудительного плавания (25).
У людей некоторые пациенты с гиперпролактинемией проявляют симптомы депрессии. Однако различий в распространенности депрессии у пациентов с гиперпролактинемией по сравнению с контрольной группой не наблюдалось (24, 26).Примечательно, что в нескольких исследованиях проводилось различие между происхождением гиперпролактинемии (например, опухоль гипофиза или нарушение регуляции нервных путей из-за изменений нейротрансмиттеров) и ее связь с тревогой и депрессией. Поскольку ПРЛ модулирует экспрессию собственных рецепторов, было высказано предположение, что пациенты с гиперпролактинемией могут экспрессировать больше ПРЛ-Р в головном мозге. Однако неизвестно, активированы ли рецепторы функционально. Избыточные уровни ПРЛ могут препятствовать образованию гомодимеров, необходимых для физиологических функций ПРЛ.Кроме того, длительная гиперпролактинемия снижает способность тубероинфундибулярных нейронов синтезировать дофамин (27). Высокие концентрации ПРЛ вызывают повышенные уровни фрагмента ПРЛ 16К, называемого вазоингибином. Этот фрагмент оказывает действие, противоположное действию нативного гормона (28, 29).
Депрессивно-подобные состояния и материнство
В нескольких исследованиях на животных сообщается о причинной связи между снижением материнской заботы и депрессивно-подобным состоянием или изменениями эмоционального поведения у потомства.Воздействие стресса во время беременности изменяет нейронные механизмы, которые подготавливают женщину к ее материнской роли, и способствует развитию психических заболеваний, таких как депрессия или тревога (30, 31). Самки крыс, подвергшиеся хроническому психосоциальному стрессу во время беременности, демонстрируют послеродовое депрессивное состояние (32–34). Активация систем окситоцина и ПРЛ во время лактации способствует ослаблению активации оси HPA и вызывает позитивное настроение (35). Следовательно, изменения в этих системах могут способствовать развитию аффективных расстройств, наблюдаемых в послеродовом периоде.Действительно, экспрессия окситоцина снижена в гипоталамусе послеродовых самок крыс, подвергшихся хроническому стрессу во время беременности (34). Послеродовой уровень циркулирующего окситоцина снижается у женщин, проявляющих депрессивные симптомы во время беременности (36). Низкие концентрации окситоцина могут увеличить риск развития послеродовой депрессии (37).
Нарушение регуляции реакции PRL-R может быть связано с послеродовыми расстройствами (38). Действительно, низкие уровни ПРЛ были обнаружены у женщин, страдающих послеродовым депрессивным расстройством (39).Введение бромокриптина на ранних стадиях беременности снижает уровень ПРЛ, вызывает депрессивное состояние и ухудшает материнское поведение у самок крыс, что позволяет предположить, что ПРЛ может играть ключевую роль в возникновении послеродовой депрессии (40, 41). Более того, повышение уровня ПРЛ, вызванное грудным вскармливанием, оказывает положительное влияние как на здоровье матери, так и на связь между матерью и младенцем. Была обнаружена корреляция между стрессом, дисфорическим настроением и сниженным уровнем гамма-интерферона у матерей, кормящих из бутылочки (42).Напротив, кормящие матери получили меньше баллов в тестах на тревожность, депрессию и гнев (43).
Нейрогенез и нейропротекция
Известно, что хроническое стрессовое воздействие и депрессивные состояния влияют на нейрогенез. Нейрогенез — это процесс, который производит новые нейроны на протяжении всей жизни. Считается, что новые нейроны временно улучшают нейронную связь. Во взрослом мозге обнаружены две нейрогенные ниши: гиппокамп и SVZ. Гиппокамп отрицательно контролирует активность оси HPA и участвует в эмоциональной модуляции.Антидепрессивные препараты усиливают нейрогенез в гиппокампе и показывают корреляцию с улучшением настроения (44). Нейрогенез обонятельной луковицы и обонятельная дисфункция также снижаются при воздействии CMS — процедуры, которая, как известно, вызывает депрессивные состояния (45).
Пролактин — регулятор нейрогенеза. Рецепторы ПРЛ экспрессируются в СВЗ и гиппокампе (46–48). Первоначальные доказательства взаимосвязи между ПРЛ и нейрогенезом были получены в исследованиях, показывающих усиление нейрогенеза в СВЗ беременных женщин.Было обнаружено, что это увеличение опосредовано ПРЛ (47), и была выдвинута гипотеза, что обонятельная дискриминация запахов, связанных с детенышами, имеет решающее значение для материнского успеха. Другие обонятельные сигналы являются важными сигналами, которые также вызывают нейрогенез в SVZ и в гиппокампе. Воздействие феромонов доминирующего самца вызывает пролиферацию клеток как в обонятельной луковице, так и в гиппокампе самок мышей. Эти эффекты опосредуются ПРЛ в обонятельной луковице и лютеинизирующим гормоном в гиппокампе, и оба гормона вносят вклад в регуляцию женского воспроизводства (49).Воздействие мужских феромонов увеличивает нейрогенез SVZ и способствует материнскому поведению у девственных и послеродовых женщин (50). Инъекции бромокриптина, агониста дофамина, самкам крыс в первые дни беременности для снижения уровня ПРЛ, снижают обонятельный нейрогенез и вызывают послеродовые изменения поведения (41). Эти сообщения ясно указывают на то, что ПРЛ может регулировать нейрогенез SVZ и играть ключевую роль в регуляции настроения.
Уменьшение нейрогенеза гиппокампа из-за воздействия хронического стресса предотвращалось ежедневным введением ПРЛ самцам мышей.Было показано, что ПРЛ способствует судьбе нейронов и оказывает нейропротекторное действие в гиппокампе (51). Первоначально считалось, что эффекты ПРЛ противодействуют глюкокортикоидному снижению пролиферации и выживаемости нейросферы. Однако инкубация ПРЛ вместе с дексаметазоном не могла подавить эффекты дексаметазона на нейросферы, несмотря на индукцию ERK1 / 2. Таким образом, было высказано предположение, что ПРЛ может влиять на нейрогенез гиппокампа через косвенный механизм (52). Следующие исследования показали как in vitro (в первичных клетках взрослого гиппокампа), так и in vivo (прямая инъекция в зубчатую извилину взрослых мышей), что введение ПРЛ увеличивает число нейросфер, что предполагает прямое влияние этого нейропептида на гиппокамп ( 53).Кроме того, эти авторы сообщили о поведенческих дефицитах у мышей с нулевым ПРЛ, обученных задачам обучения, зависящим от гиппокампа, и предположили роль ПРЛ в процессах обучения и памяти (53). Напротив, ежедневные инъекции ПРЛ крысам в течение первых двух постнатальных недель снижают нейрогенез как в зубчатой извилине, так и в обонятельной луковице и вызывают депрессивное состояние как у взрослых самцов, так и у самок крыс (54). Эти результаты предполагают, что ПРЛ по-разному влияет на нейрогенез в зависимости от возраста животных, и это может быть связано с эмоциональной регуляцией.
Во время беременности и кормления грудью ПРЛ защищает гиппокамп от высоких концентраций глюкокортикоидов (55). Введение овечьего ПРЛ в желудочек головного мозга девственных самок с удаленными яичниками буферизует нейродегенеративный процесс, вызванный инфузией каиновой кислоты в областях СА1, СА3 и СА4 гиппокампа (56, 57). Эти результаты предполагают нейрозащитную роль ПРЛ в гиппокампе.
Нейронные механизмы действия ПРЛ
Действие пролактина на нейрогенез опосредуется его активацией киназы 5 (ERK5), регулируемой внеклеточными сигналами.ERK5 экспрессируется в нейрогенных нишах мозга (58). Более того, ПРЛ увеличивает как экспрессию, так и уровни белка нестина и связанного с микротрубочками белка 2 (MAP2) в клетках нейробластомы (SK-N-SH). Это предполагает, что ПРЛ регулирует синтез белка цитоскелета и, следовательно, способствует дифференцировке нейронов (59). Кроме того, ПРЛ модулирует Ca 2+ -зависимые каналы K + , которые могут влиять на высвобождение нейротрансмиттеров в различных областях мозга (60).В гипоталамусе ПРЛ стимулирует путь ERK / MAPK в нейронах CRH, вазопрессина и окситоцина (61) и способствует экспрессии EGR-1 в магноцеллюлярных нейронах (62). Активация этих путей ПРЛ может способствовать пластическим изменениям, наблюдаемым в головном мозге во время беременности. Стимуляция ПРЛ транскрипции CRH в культивируемых клетках гипоталамуса интерпретируется как косвенный ингибирующий контроль ПРЛ на активность оси HPA (62). Однако до сих пор неизвестно, как PRL влияет на ось HPA.
Заключительные замечания и направления на будущее
Пролактин изменяет нейронные цепи, чтобы помочь человеку справиться со стрессом.Сниженная активация нервных входов, активация ионных каналов или модуляция нескольких сигнальных путей — вот некоторые из предполагаемых механизмов действия, лежащих в основе эффектов ПРЛ на мозговые цепи. Неизвестно, как ПРЛ регулирует функцию оси HPA во время стрессовой реакции. ПРЛ может влиять на активность гипоталамуса и / или гиппокампа, регулируя эмоциональность. Вклад ПРЛ в послеродовую депрессию до сих пор неизвестен. Низкий уровень ПРЛ у кормящих женщин был связан с послеродовой депрессией.Ингибирование ПРЛ снижает нейрогенез в обонятельной луковице, но механизмы, которые приводят к послеродовому депрессивному состоянию, неизвестны. Кроме того, пути, на которые влияет ПРЛ на регуляцию тревожности, еще не известны, и остается неясным, вносят ли эффекты ПРЛ на нейрогенез гиппокампа в модулирование тревожности. Введение ПРЛ на ранних постнатальных стадиях снижает нейрогенез в гиппокампе и обонятельной луковице и способствует депрессивному состоянию во взрослом возрасте. Это говорит о том, что ПРЛ влияет на критическое окно во время развития мозга и что действия ПРЛ зависят от возраста, в течение которого он применяется.Необходимы дальнейшие исследования, чтобы понять механизмы действия ПРЛ в головном мозге и то, как этот гормон модулирует эмоциональность и тревогу на разных этапах развития.
Вклад авторов
Автор подтверждает, что является единственным соавтором этой работы, и одобряет ее к публикации.
Заявление о конфликте интересов
Автор заявляет, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы рассматриваться как потенциальный конфликт интересов.
Финансирование
Финансирование было предоставлено LT за счет гранта FIS / IMSS / PROT / GII / 922 от Fondo de Investigación en Salud (FIS), принадлежащего Instituto Mexicano del Seguro Social (IMSS). FIS-IMSS больше не участвовал в разработке исследования, написании отчета и принятии решения о представлении статьи для публикации.
Ссылки
1. Боле-Фейсот С., Гоффин В., Эдери М., Бинарт Н., Келли П.А. Пролактин (ПРЛ) и его рецепторное действие, пути передачи сигнала и фенотипы, наблюдаемые у мышей с нокаутом рецепторов ПРЛ.Endocr Rev (1998) 19: 225–68.10.1210 / edrv.19.3.0334 [PubMed] [CrossRef] [Google Scholar] 2. Freeman ME, Kanyicska B, Lerant A, Nagy G. Пролактин: структура, функция и регуляция секреции. Physiol Rev (2000) 80 (4): 1523–631. [PubMed] [Google Scholar] 3. Клапп С., Торнер Л., Гутьеррес-Оспина Г., Алькантара Е., Лопес Ф. Дж., Нагано М. и др. Ген пролактина экспрессируется в гипоталамо-нейрогипофизарной системе, и белок процессируется во фрагмент 14 кДа с активностью, подобной пролактину 16 кДа.Proc Natl Acad Sci U S A (1994) 91: 10384–8.10.1073 / pnas.91.22.10384 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 4. Торнер Л., Малумби Р., Нава Г., Аранда Дж., Клапп С., Нойманн И.Д. Высвобождение in vivo и активация генов пролактина мозга в ответ на физиологические стимулы. Eur J Neurosci (2004) 19 (6): 1601–8.10.1111 / j.1460-9568.2004.03264.x [PubMed] [CrossRef] [Google Scholar] 5. Roselli CE, Bocklandt S, Stadelman HL, Wadsworth T, Vilain E, Stormshak F. Экспрессия пролактина в головном мозге овцы.Нейроэндокринология (2008) 87: 206–15.10.1159 / 000114643 [PubMed] [CrossRef] [Google Scholar] 6. Чайсеха Ю., Нгернсунгнерн П., Сартсунноен Н., Пракобсенг Н., Эль-Халавани М.Э. Присутствие мРНК пролактина во внегипофизарных областях мозга домашней индейки. Acta Histochem (2012) 114: 116–21.10.1016 / j.acthis.2011.03.007 [PubMed] [CrossRef] [Google Scholar] 7. Якоб С., Шраут К.Г., Шмитт А.Г., Шольц С.Дж., Ортега Г., Штайнбуш Х.В. и др. Дифференциальные эффекты пренатального стресса у самок 5-HTT-дефицитных мышей: в сторону молекулярных механизмов устойчивости.Dev Neurosci (2014) 36 (6): 454–64.10.1159 / 000363695 [PubMed] [CrossRef] [Google Scholar] 8. Уолш Р.Дж., Слаби Ф.Дж., Познер Б.И. Рецептор-опосредованный механизм транспорта пролактина из крови в спинномозговую жидкость. Эндокринология (1987) 120: 1846–50.10.1210 / endo-120-5-1846 [PubMed] [CrossRef] [Google Scholar] 9. Brown RS, Wyatt AK, Herbison RE, Knowles PJ, Ladyman SR, Binart N, et al. Транспорт пролактина в мозг мыши не зависит от рецептора пролактина. FASEB J (2015) 30 (2): 1002–10.10.1096 / fj.15-276519 [PubMed] [CrossRef] [Google Scholar] 10. Felicio LF, Bridges RS. Домперидон вызывает чувствительное к пробенециду повышение иммунореактивного пролактина в церебровентрикулярных перфузатах у самок крыс. Brain Res (1992) 573 (1): 133–8.10.1016 / 0006-8993 (92)-P [PubMed] [CrossRef] [Google Scholar] 11. Николсон Дж., Грили Г. Х., младший, Хамм Дж., Янгблад В. В., Кизер Дж. С.. Пролактин в спинномозговой жидкости — вероятное место ауторегуляции пролактина. Brain Res (1980) 190: 447–57.10.1016 / 0006-8993 (80)
-5 [PubMed] [CrossRef] [Google Scholar] 12.Томпсон С.А. Локализация иммунореактивного пролактина в эпендиме и окжелудочковых органах головного мозга крыс. Cell Tissue Res (1982) 225 (1): 79–93.10.1007 / BF00216220 [PubMed] [CrossRef] [Google Scholar] 13. Das R, Vonderhaar BK. Передача сигнала роста пролактина (ПРЛ) через длинные и короткие формы рецептора ПРЛ. Mol Endocrinol (1995) 9: 1750–9.10.1210 / mend.9.12.8614411 [PubMed] [CrossRef] [Google Scholar] 14. Перро-Аппланат М., Гуалильо О, Пезет А., Винсент В., Эдери М., Келли П.А. Доминирующие негативные и кооперативные эффекты мутантных форм рецептора пролактина.Mol Endocrinol (1997) 11: 1020–32.10.1210 / исправление.11.8.9954 [PubMed] [CrossRef] [Google Scholar] 15. Gala RR. Физиология и механизмы стресс-индуцированных изменений секреции пролактина у крыс. Life Sci (1990) 46 (20): 1407–20.10.1016 / 0024-3205 (90)-U [PubMed] [CrossRef] [Google Scholar] 21.Toufexis DJ, Tesolin S, Huang N, Walker C. Измененная чувствительность гипофиза к кортикотропин-рилизинг-фактору и аргинин-вазопрессину участвует в стрессовой гипореактивности лактации у крыс. J. Neuroendocrinol (1999) 11 (10): 757–64.10.1046 / j.1365-2826.1999.00381.x [PubMed] [CrossRef] [Google Scholar] 22. Landgraf R, Wigger A, Holsboer F, Neumann ID. Гиперреактивная ось гипоталамо-гипофиз-надпочечник у крыс, разводимых для поведения, связанного с высокой тревожностью. Дж. Нейроэндокринол (1999) 11 (6): 405–7.10.1046 / j.1365-2826.1999.00342.x [PubMed] [CrossRef] [Google Scholar] 23. Стеймер Т., Дрисколл П. Дивергентные реакции на стресс и стили совладания у психогенетически отобранных римских крыс с высоким (RHA) и низким (RLA) избеганием: поведенческие, нейроэндокринные аспекты и аспекты развития. Стресс (2003) 6 (2): 87–100.10.1080 / 102538
00111320 [PubMed] [CrossRef] [Google Scholar] 24. Ривли А., Фишер А. Д., Оуэн Д., Крид Ф. Х., Дэвис-младший. Психологический стресс у пациентов с гиперпролактинемией. Clin Endocrinol (Oxf) (1997) 47 (3): 343–8.10.1046 / j.1365-2265.1997.2701073.x [PubMed] [CrossRef] [Google Scholar] 25. Драго Ф., Пульвиренти Л., Спадаро Ф., Пеннсини Дж. Эффекты ТРГ и пролактина в модели депрессии в поведенческом отчаянии (плавание) у крыс. Психонейроэндокринология (1990) 15: 349–56.10.1016 / 0306-4530 (90)
-M [PubMed] [CrossRef] [Google Scholar] 26. Oliveira MC, Pizarro CB, Golbert L, Micheletto C. Гиперпролактинемия и психологическое расстройство. Arq Neuropsiquiatr (2000) 58 (3A): 671–6.10.1590 / S0004-282X2000000400012 [PubMed] [CrossRef] [Google Scholar] 27.Mohankumar PS, Mohankumar SM, Quadri SK, Voogt JL. Хроническая гиперпролактинемия и изменения дофаминовых нейронов. Brain Res Bull (1997) 42 (6): 435–41.10.1016 / S0361-9230 (96) 00369-3 [PubMed] [CrossRef] [Google Scholar] 28. Гоффин В., Бинарт Н., Турень П., Келли П.А. Пролактин: новая биология старого гормона. Анну Рев Физиол (2002) 64: 47–67.10.1146 / annurev.physiol.64.081501.131049 [PubMed] [CrossRef] [Google Scholar] 29. Заморано М., Ледесма-Колунга М.Г., Адан Н., Вера-Массиу С., Лемини М., Мендес И. и др.Вазоингибины, производные пролактина, усиливают поведение, связанное с тревогой и депрессией. Психонейроэндокринология (2014) 44: 123–32.10.1016 / j.psyneuen.2014.03.006 [PubMed] [CrossRef] [Google Scholar] 30. О’Хара М.В., Шлехте Д.А., Льюис Д.А., Райт Э.Дж. Проспективное изучение биологических и психосоциальных факторов послеродовой хандры. Arch Gen Psychiatry (1991) 48: 801–6.10.1001 / archpsyc.1991.01810330025004 [PubMed] [CrossRef] [Google Scholar] 31. Bosch OJ, Müsch W., Bredewold R, Slattery DA, Neumann ID. Пренатальный стресс увеличивает активность оси HPA и ухудшает заботу о матери в кормящих потомках женского пола: последствия для послеродового расстройства настроения.Психонейроэндокринология (2007) 32 (3): 267–78.10.1016 / j.psyneuen.2006.12.012 [PubMed] [CrossRef] [Google Scholar] 32. Смит Дж. В., Секл Дж. Р., Эванс А. Т., Косталл Б., Смайт Дж. В.. Гестационный стресс вызывает послеродовую депрессию и изменяет материнский уход у крыс. Психонейроэндокринология (2004) 29 (2): 227–44.10.1016 / S0306-4530 (03) 00025-8 [PubMed] [CrossRef] [Google Scholar] 33. Смит М.В., Шао Л., Хауэлл Х., Лин Х., Йонкерс К.А. Перинатальная депрессия и исходы родов в проекте здорового старта. Matern Child Health J (2011) 15: 401–9.10.1007 / s10995-010-0595-6 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Гиллерер К.М., Ребер С.О., Нойманн И.Д., Слэттери Д.А. Воздействие хронического стресса во время беременности меняет послеродовую адаптацию: последствия для послеродовой тревожности и расстройств настроения. Эндокринология (2011) 152 (10): 3930–40.10.1210 / en.2011-1091 [PubMed] [CrossRef] [Google Scholar] 35. Heinrichs M, Meinlschmidt G, Neumann I, Wagner S, Kirschbaum C, Ehlert U, et al. Влияние сосания на ответы оси гипоталамус-гипофиз-надпочечники на психосоциальный стресс у кормящих женщин в послеродовом периоде.J Clin Endocrinol Metab (2001) 86: 4798–804.10.1210 / jcem.86.10.7919 [PubMed] [CrossRef] [Google Scholar] 36. Лайт К.С., Грюен К.М., Амико Дж. А., Бочча М., Браунли К. А., Джонс Дж. М.. Дефицит реакции окситоцина в плазме и усиление негативных эмоций, стресса и артериального давления у матерей, подвергшихся воздействию кокаина во время беременности. Addict Behav (2004) 29 (8): 1541–64.10.1016 / j.addbeh.2004.02.062 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 37. Skrundz M, Bolten M, Nast I, Hellhammer DH, Meinlschmidt G. Концентрация окситоцина в плазме во время беременности связана с развитием послеродовой депрессии.Нейропсихофармакология (2011) 36 (9): 1886–93.10.1038 / npp.2011.74 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 38. Sjoeholm A, Bridges RS, Grattan DR, Anderson GM. Повышение чувствительности к пролактину у репродуктивных самок крыс, специфичных для регионов, нейронов и сигнальных путей. Эндокринология (2011) 152 (5): 1979–88.10.1210 / en.2010-1220 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39. Абу-Салех М.Т., Губаш Р., Карим Л., Крымски М., Бхаи И. Гормональные аспекты послеродовой депрессии.Психонейроэндокринология (1998) 23 (5): 465–75.10.1016 / S0306-4530 (98) 00022-5 [PubMed] [CrossRef] [Google Scholar] 40. Ларсен CM, Grattan DR. Вызванный пролактином митогенез в субвентрикулярной зоне материнского мозга на ранних сроках беременности важен для нормальных послеродовых поведенческих реакций у матери. Эндокринология (2010) 151 (8): 3805–14.10.1210 / en.2009-1385 [PubMed] [CrossRef] [Google Scholar] 41. Ларсен CM, Grattan DR. Пролактин, нейрогенез и материнское поведение. Иммунное поведение мозга (2012) 26 (2): 201–9.10.1016 / j.bbi.2011.07.233 [PubMed] [CrossRef] [Google Scholar] 42. Гроер М.В., Дэвис М.В. Цитокины, инфекции, стресс и дисфорическое настроение у лиц, кормящих грудью и кормящих смесью. J Obstet Gynecol Neonatal Nurs (2006) 35 (5): 599–607.10.1111 / j.1552-6909.2006.00083.x [PubMed] [CrossRef] [Google Scholar] 43. Groër MW. Различия между исключительно кормящими грудью, кормящими смесями и контрольной группой: исследование стресса, настроения и эндокринных переменных. Биол Рес Нурс (2005) 7 (2): 106–17.10.1177 / 1099800405280936 [PubMed] [CrossRef] [Google Scholar] 44.Santarelli L, Saxe M, Gross C, Surget A, Battaglia F, Dulawa S и др. Необходимость нейрогенеза гиппокампа для поведенческих эффектов антидепрессантов. Science (2003) 301 (5634): 805–9.10.1126 / science.1083328 [PubMed] [CrossRef] [Google Scholar] 45. Ян Д., Ли Кью, Фанг Л., Ченг К., Чжан Р., Чжэн П. и др. Сниженный нейрогенез и пресинаптическая дисфункция в обонятельной луковице крысиной модели депрессии. Неврология (2011) 192: 609–18.10.1016 / j.neuroscience.2011.06.043 [PubMed] [CrossRef] [Google Scholar] 46.Ногами Х., Хосино Р., Огасавара К., Миямото С., Хисано С. Регионоспецифическая экспрессия и гормональная регуляция вариантов первого экзона мРНК рецептора пролактина крысы в головном мозге и передней доле гипофиза. J Neuroendocrinol (2007) 19: 583–93.10.1111 / j.1365-2826.2007.01565.x [PubMed] [CrossRef] [Google Scholar] 47. Шинго Т., Грегг С., Энвере Э, Фудзикава Х., Хассам Р., Гири С. и др. Стимулированный беременностью нейрогенез в переднем мозге взрослой женщины, опосредованный пролактином. Наука (2003) 299: 117–20.10.1126 / science.1076647 [PubMed] [CrossRef] [Google Scholar] 48. Мак Г.К., Вайс С. Отцовское распознавание взрослого потомства, опосредованное вновь созданными нейронами ЦНС. Nat Neurosci (2010) 13 (6): 753–8.10.1038 / nn.2550 [PubMed] [CrossRef] [Google Scholar] 49. Мак Г.К., Энвере Е.К., Грегг С., Пакарайнен Т., Поутанен М., Хухтаниеми И. и др. Стимулированный мужскими феромонами нейрогенез в мозге взрослой женщины: возможная роль в брачном поведении. Nat Neurosci (2007) 10 (8): 1003–11.10.1038 / nn1928 [PubMed] [CrossRef] [Google Scholar] 50.Ларсен CM, Kokay IC, Grattan DR. Феромоны мужского пола инициируют индуцированный пролактином нейрогенез и улучшают материнское поведение у самок мышей. Horm Behav (2008) 53 (4): 509–17.10.1016 / j.yhbeh.2007.11.020 [PubMed] [CrossRef] [Google Scholar] 51. Торнер Л., Карг С., Блюм А., Кандасами М., Кун Г. Г., Винклер Дж. И др. Пролактин предотвращает вызванное хроническим стрессом снижение нейрогенеза в гиппокампе взрослых и способствует судьбе нейронов. J Neurosci (2009) 29 (6): 1826–33.10.1523 / JNEUROSCI.3178-08.2009 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 52.Wagner K, Couillard-Despres S, Lehner B, Brockhoff G, Rivera FJ, Blume A и др. Пролактин индуцирует передачу сигналов MAPK в нейральных предшественниках без ослабления индуцированного глюкокортикоидами ингибирования нейрогенеза in vitro. Cell Physiol Biochem (2009) 24 (5-6): 397-406.10.1159 / 000257432 [PubMed] [CrossRef] [Google Scholar] 53. Уокер Т.Л., Вукович Дж., Кудийс М.М., Блэкмор Д.Г., Маккей Э.В., Сайкс А.М. и др. Пролактин стимулирует клетки-предшественники в гиппокампе взрослых мышей. PLoS One (2012) 7 (9): e44371.10.1371 / journal.pone.0044371 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 54. Ладжуд Н., Гонсалес-Запиен Р., Роке А., Тинахеро Э., Вальдес Дж. Дж., Клапп С. и др. Введение пролактина в ранний постнатальный период снижает нейрогенез гиппокампа и обонятельных луковиц и приводит к депрессивному поведению во взрослом возрасте. Horm Behav (2013) 64 (5): 781–9.10.1016 / j.yhbeh.2013.10.005 [PubMed] [CrossRef] [Google Scholar] 55. Моралес Т. Последние данные о нейропротекции против эксайтотоксичности в гиппокампе самок крыс.J. Neuroendocrinol (2011) 23 (11): 994–1001.10.1111 / j.1365-2826.2011.02141.x [PubMed] [CrossRef] [Google Scholar] 56. Техадилла Д., Цербон М., Моралес Т. Пролактин снижает повреждающие эффекты эксайтотоксичности в дорсальном гиппокампе самки крысы независимо от гормонов яичников. Неврология (2010) 169 (3): 1178–85.10.1016 / j.neuroscience.2010.05.074 [PubMed] [CrossRef] [Google Scholar] 57. Моралес Т., Лоренсон М., Уокер А.М., Рамос Э. Как пролактин (PRL), так и молекулярный имитатор фосфорилированного PRL, S179D-PRL, защищают гиппокамп самок крыс от эксайтотоксичности.Neuroscience (2014) 258: 211–7.10.1016 / j.neuroscience.2013.11.015 [PubMed] [CrossRef] [Google Scholar] 58. Ван В., Пань Ю.В., Виетеча Т., Цзоу Дж., Абель Г.М., Куо С.Т. и др. Киназа 5 (ERK5), регулируемая внеклеточными сигналами, опосредует стимулируемый пролактином нейрогенез взрослых в субвентрикулярной зоне и обонятельной луковице. J Biol Chem (2013) 288 (4): 2623–31.10.1074 / jbc.M112.401091 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 59. Havránek T, Bačová Z, Štrbák V, Lešťanová Z, Bakoš J. Пролактин увеличивает экспрессию белков цитоскелета в клетках SK-N-SH.Folia Biol (Praha) (2014) 60 (6): 281–5. [PubMed] [Google Scholar] 60. Патил М.Дж., Генри М.А., Акопян А.Н. Рецептор пролактина в регуляции возбудимости нейронов и каналов. Каналы (Остин) (2014) 8 (3): 193–202.10.4161 / chan.28946 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 61. Блюм А., Торнер Л., Лю Ю., Суббураджу С., Агилера Г., Нойманн И.Д. Пролактин активирует передачу сигналов митоген-активируемой протеинкиназы и транскрипцию рилизинг-гормона кортикотропина в нейронах гипоталамуса крыс. Эндокринология (2009) 150 (4): 1841–9.10.1210 / en.2008-1023 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 62. Блюм А., Торнер Л., Лю Ю., Суббураджу С., Агилера Г., Нойманн И.Д. Пролактин индуцирует экспрессию гена Egr-1 в культивируемых клетках гипоталамуса и в гипоталамусе крыс. Brain Res (2009) 1302: 34–41.10.1016 / j.brainres.2009.09.047 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
От физиологической адаптации к стрессу и нейрогенеза к психопатологии
Front Endocrinol ( Лозанна). 2016; 7: 25.
Лус Торнер
1 Neuroendocrinología, Departamento de Neurociencias, Centro de Investigación Biomédica de Michoacán, Instituto Mexicano del Seguro Social, Морелия, Мексика
Neología de Neología de Neología, Departamento Departament де Мичоакан, Instituto Mexicano del Seguro Social, Морелия, Мексика
Отредактировал: Дебора Сучеки, Федеральный университет Сан-Паулу, Бразилия
Рецензент: Кэрол Ф.Элиас, Мичиганский университет, США; Габор Б. Макара, Венгерская академия наук, Венгрия
Специализированный раздел: Эта статья была отправлена в раздел «Нейроэндокринная наука» журнала «Границы эндокринологии»
Поступила в редакцию 18 августа 2015 г .; Принято 14 марта 2016 г.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора (авторов) или лицензиара и ссылки на оригинальную публикацию в этом журнале в соответствии с принятой академической практикой.Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья цитируется в других статьях в PMC.Abstract
Пролактин (ПРЛ) — один из самых универсальных известных гормонов. Он считается адаптивным гормоном из-за ключевой роли, которую он играет в модуляции реакции на стресс, а также во время беременности и кормления грудью. Внутри мозга ПРЛ действует как нейропептид, стимулируя физиологические реакции, связанные с воспроизводством, адаптацией к стрессу, нейрогенезом и нейрозащитой.Действие ПРЛ на нервную систему способствует широкому спектру изменений, которые происходят в женском мозге во время беременности и приводят к ослаблению оси гипоталамус-гипофиз-надпочечники. Вместе все эти изменения способствуют поведенческой и физиологической адаптации новой матери, чтобы обеспечить репродуктивный успех. Адаптации мозга, вызванные ПРЛ, также важны для регуляции материнской эмоциональности и благополучия. ПРЛ также влияет на мужской мозг во время стрессовой реакции, но его эффекты менее изучены.ПРЛ регулирует нейрогенез как в субвентрикулярной зоне, так и в гиппокампе. Следовательно, изменения в системе ПРЛ из-за стресса или воздействия веществ, которые снижают нейрогенез или другие состояния, могут способствовать дезадаптивным реакциям и патологическим поведенческим результатам. Здесь мы рассмотрим систему ПРЛ и ее роль в модуляции реакции на стресс и регуляции эмоций. Мы обсуждаем влияние ПРЛ на нейрогенез и нейрозащиту, предполагаемые нейронные механизмы, лежащие в основе этих эффектов, и их вклад в возникновение психопатологических состояний, таких как депрессия.
Ключевые слова: тревога, депрессия, рецепторы пролактина, расстройства настроения, нейрогенез
Введение
Пролактин (ПРЛ) — плейотропный гормон гипофиза с более чем 300 известными физиологическими эффектами. Этот белковый гормон регулирует воспроизводство, иммуномодуляцию, ангиогенез, энергетический метаболизм, осмотический баланс и развитие. Помимо своих периферических функций, ПРЛ также играет много важных ролей в качестве нейропептида. ПРЛ проникает через гематоэнцефалический барьер, а локальная продукция гипоталамуса способствует достижению нескольких областей мозга, вызывающих сильные модулирующие эффекты.В частности, ПРЛ вносит вклад в регуляцию стрессовых реакций посредством ингибирования оси гипоталамус-гипофиз-надпочечники (HPA). Более того, ПРЛ модулирует тревожность и депрессивное поведение. ПРЛ также регулирует нейрогенез, генерацию новых нейронов как в субвентрикулярной зоне (SVZ), так и в гиппокампе. Уровни ПРЛ и условия окружающей среды могут вызывать изменения в нейрогенезе, потенциально влияя на эмоциональное поведение. Действительно, снижение уровня ПРЛ на ранних сроках беременности влияет на нейрогенез обонятельной луковицы и увеличивает послеродовую тревогу у самок крыс.Кроме того, ПРЛ может оказывать нейропротекторное действие в гиппокампе взрослых животных, подвергшихся хроническому стрессу или подвергнутых инфузии каиновой кислоты в гиппокамп. Однако ПРЛ снижает нейрогенез при введении на ранних стадиях развития и способствует депрессивному поведению во взрослом возрасте. Некоторые из этих эффектов опосредованы активацией различных нейрональных сигнальных систем и ионных каналов. Здесь мы суммируем некоторые аспекты действий ПРЛ в головном мозге и их вклад в возникновение психопатологических состояний, таких как депрессия.
Система пролактина
Синтез ПРЛ
Пролактин вырабатывается в основном лактотрофными клетками передней доли гипофиза. ПРЛ находится под ингибирующим контролем дофамина, высвобождаемого тубероинфундибулярными дофаминергическими (TIDA) нейронами (1). Несмотря на многочисленные попытки картировать ПРЛ в церебральных областях с использованием нескольких методов, синтез ПРЛ в головном мозге оказался под вопросом. PRL-положительные нейроны были локализованы методом иммуноцитохимии у самцов и самок разных видов (2).МРНК ПРЛ была обнаружена с помощью ПЦР в паравентрикулярном ядре (ПВЯ) и супраоптическом ядре (3) и с помощью кПЦР в гипоталамусе самок крыс (4). In situ гибридизация показала экспрессию ПРЛ в медиальной преоптической области (MPOA), перивентрикулярном преоптическом ядре, ядре ложа концевой полоски, PVN и латеральной перегородке у домашней индейки, а также у эмбрионов и взрослых овец (5 , 6). Недавние исследования с использованием методов микроматрицы обнаружили экспрессию ПРЛ в гиппокампе устойчивых мышей (7).
Периферический ПРЛ считается основным эффектором в головном мозге. Было высказано предположение, что ПРЛ может пересекать гематоэнцефалический барьер посредством рецепторно-опосредованного механизма, происходящего в клетках сосудистого сплетения (8). Однако недавние исследования с использованием мышей с нокаутом рецептора PRL (PRL-R) показали, что транспорт PRL зависит не от PRL-R, а от другого, еще не идентифицированного механизма (9). Через 30 минут после периферического введения ПРЛ активирует нейроны мозга за счет индукции фосфорилирования сигнального преобразователя и активатора транскрипции 5 [pSTAT5 (9)].Пики ПРЛ в спинномозговой жидкости (ЦСЖ) через 30 мин (10) или 90 мин (9) после его периферического введения. Эти последние исследования также предполагают, что ПРЛ не попадает в мозг после попадания в спинномозговую жидкость (9). Поскольку иммунореактивный ПРЛ наблюдался в сосудистом сплетении и эпендимных клетках желудочков головного мозга, было высказано предположение, что ПРЛ может транспортироваться из этих участков для достижения своих целевых областей (11, 12). Однако до сих пор неизвестно, как ПРЛ получает доступ к своим отдаленным целевым областям в головном мозге.Принимают ли эпендимные клетки или нейроны ПРЛ и высвобождают его в непосредственной близости от своих клеток-мишеней, или если ПРЛ высвобождается во внеклеточное пространство, чтобы диффундировать, пока не достигнет его рецепторов, все еще остается предметом споров.
Рецепторы ПРЛ
Рецепторы пролактина относятся к суперсемейству цитокиновых рецепторов класса 1 (1). PRL-R кодируется одним геном, но альтернативный сплайсинг дает несколько изоформ PRL-R. И у человека, и у крыс три изоформы (длинная, промежуточная и короткая — e.g., размер внутриклеточного домена). Ответ запускается после димеризации рецепторов с образованием гомодимеров. Длинно-длинные димеры способны активировать пути вторичных мессенджеров, в частности, сигнальный каскад преобразователя JAK-сигнала и активатора транскрипции (JAK-STAT) посредством активации STAT3 и STAT5. Короткая изоформа PRL-R активирует путь митоген-активируемой протеинкиназы (MAPK) (13). И длинные, и короткие гетеродимеры рецепторов ингибируют передачу сигналов ПРЛ (14) и способствуют модуляции действий ПРЛ.
Реакция на стресс и ПРЛ
Стресс — критический фактор, который может привести к депрессивным расстройствам. Воздействие стресса активирует ось HPA, вызывая высвобождение кортикотропин-рилизинг-гормона (CRH) в PVN, который способствует секреции адренокортикотропина (ACTH) из гипофиза. В свою очередь, АКТГ запускает выброс глюкокортикоидов из надпочечников. ПРЛ также секретируется гипофизом в ответ на ряд стрессорных факторов. Первоначальные исследования показали, что ПРЛ может противодействовать воздействию глюкокортикоидов на иммунную систему во время стрессовой реакции (15).Однако более поздние исследования показали, что предотвращение экспрессии PRL-R в мозге с помощью антисмыслового зонда сильно увеличивает вызванную стрессом секрецию АКТГ у девственных и кормящих крыс, предполагая, что ПРЛ играет ингибирующую роль в реактивности оси HPA (16, 17 ). Была выдвинута гипотеза, что ПРЛ модулирует активность оси HPA за счет уменьшения нервных входов в PVN. Как острые, так и хронические интрацеребровентрикулярные введения ПРЛ у девственных самок крыс снижают активацию нейронов миндалины и экспрессию гипоталамуса CRH в ответ на стресс (18).Кроме того, ПРЛ локально высвобождается из PVN и MPOA в ответ на физиологические стимулы, включая стресс (4).
Пролактин недавно был связан с устойчивостью в модели хронического легкого стресса (CMS). Взрослые крысы, ранее подвергавшиеся CMS, были выбраны как отвечающие и не отвечающие на лечение в соответствии с их реакцией на стресс. Устойчивые животные (т. Е. Не отвечающие) имели более высокие уровни ПРЛ в плазме и более высокие уровни мРНК ПРЛ-Р в сосудистом сплетении, чем у их уязвимых (т.е., респонденты) аналог (19). Соответственно, исследование микроматрицы, проведенное на гетерозиготных 5-Htt-дефицитных потомках, подвергшихся пренатальному стрессу, показало, что ПРЛ, гормон роста и рецептор галанина 3 по-разному экспрессируются в гиппокампе устойчивых мышей по сравнению с контролем (7). Эти результаты предполагают роль ПРЛ в регуляции стресса на уровне гиппокампа.
ПРЛ и эмоциональная реакция
Эффекты ПРЛ на тревожность и депрессивное поведение были изучены, но они различаются в зависимости от используемых видов и физиологического состояния.
ПРЛ и тревога
Внутрицеребровентрикулярное или внутривенное введение ПРЛ оказывает дозозависимый анксиолитический эффект как у самцов, так и у девственных самок крыс (16). Уровень тревожности у беременных и кормящих крыс постепенно снижается (20, 21). Эти эффекты, вероятно, опосредуются ПРЛ, о чем свидетельствует повышенная тревожность, проявляемая кормящими самками крыс в приподнятом крестообразном лабиринте после блокады экспрессии ПРЛ-Р в головном мозге (17). Было показано, что хроническое ICV-введение ПРЛ крысам-самкам с удаленной овариэктомией (используемым для моделирования эндокринного статуса во время беременности) снижает уровень тревожности в приподнятом крестообразном лабиринте (18).Взятые вместе, эти результаты убедительно свидетельствуют о том, что ПРЛ оказывает анксиолитическое действие на грызунов.
Исследования инбредных линий грызунов показали связь между повышенным уровнем ПРЛ и повышенной тревожностью. Сообщалось о повышенных базальных и стресс-индуцированных уровнях ПРЛ у крыс-самцов, разводимых с высоким тревожным поведением (HAB), по сравнению с крысами с низким тревожным поведением (LAB) (22). Римская линия крыс с низким уровнем избегания (RLA / Verh) (т. Е. Крысы, отобранные для низкой производительности в двустороннем тесте активного избегания) демонстрирует повышенные реакции на стресс, более высокие уровни ПРЛ и пассивный стиль совладания по сравнению с римскими высокими. линия крыс-избегание (RHA / Verh) (i.е., крысы, отобранные для достижения высоких результатов в тесте двустороннего активного избегания) аналог (23). Повышенные уровни ПРЛ, обнаруженные в этой линии животных, могут быть результатом дисбаланса одного или нескольких стимуляторов секреции ПРЛ (серотонина, ГАМК и т. Д.). В качестве альтернативы, высокие концентрации ПРЛ могут помочь улучшить избыточную реактивность оси HPA, наблюдаемую у этих животных. Напротив, клинические исследования на людях показали корреляцию между высокими уровнями ПРЛ и психологическим стрессом. Пациенты женского пола с гиперпролактинемией обычно сообщают о большем количестве симптомов тревоги и враждебности, чем женщины контрольной группы (24).
ПРЛ и депрессивные состояния
Было показано, что искусственное индуцирование гиперпролактинемии у взрослых самцов крыс путем помещения трансплантатов гипофиза крысы-донора в почку животного-рецептора оказывает антидепрессивный эффект в тесте принудительного плавания (25).
У людей некоторые пациенты с гиперпролактинемией проявляют симптомы депрессии. Однако различий в распространенности депрессии у пациентов с гиперпролактинемией по сравнению с контрольной группой не наблюдалось (24, 26).Примечательно, что в нескольких исследованиях проводилось различие между происхождением гиперпролактинемии (например, опухоль гипофиза или нарушение регуляции нервных путей из-за изменений нейротрансмиттеров) и ее связь с тревогой и депрессией. Поскольку ПРЛ модулирует экспрессию собственных рецепторов, было высказано предположение, что пациенты с гиперпролактинемией могут экспрессировать больше ПРЛ-Р в головном мозге. Однако неизвестно, активированы ли рецепторы функционально. Избыточные уровни ПРЛ могут препятствовать образованию гомодимеров, необходимых для физиологических функций ПРЛ.Кроме того, длительная гиперпролактинемия снижает способность тубероинфундибулярных нейронов синтезировать дофамин (27). Высокие концентрации ПРЛ вызывают повышенные уровни фрагмента ПРЛ 16К, называемого вазоингибином. Этот фрагмент оказывает действие, противоположное действию нативного гормона (28, 29).
Депрессивно-подобные состояния и материнство
В нескольких исследованиях на животных сообщается о причинной связи между снижением материнской заботы и депрессивно-подобным состоянием или изменениями эмоционального поведения у потомства.Воздействие стресса во время беременности изменяет нейронные механизмы, которые подготавливают женщину к ее материнской роли, и способствует развитию психических заболеваний, таких как депрессия или тревога (30, 31). Самки крыс, подвергшиеся хроническому психосоциальному стрессу во время беременности, демонстрируют послеродовое депрессивное состояние (32–34). Активация систем окситоцина и ПРЛ во время лактации способствует ослаблению активации оси HPA и вызывает позитивное настроение (35). Следовательно, изменения в этих системах могут способствовать развитию аффективных расстройств, наблюдаемых в послеродовом периоде.Действительно, экспрессия окситоцина снижена в гипоталамусе послеродовых самок крыс, подвергшихся хроническому стрессу во время беременности (34). Послеродовой уровень циркулирующего окситоцина снижается у женщин, проявляющих депрессивные симптомы во время беременности (36). Низкие концентрации окситоцина могут увеличить риск развития послеродовой депрессии (37).
Нарушение регуляции реакции PRL-R может быть связано с послеродовыми расстройствами (38). Действительно, низкие уровни ПРЛ были обнаружены у женщин, страдающих послеродовым депрессивным расстройством (39).Введение бромокриптина на ранних стадиях беременности снижает уровень ПРЛ, вызывает депрессивное состояние и ухудшает материнское поведение у самок крыс, что позволяет предположить, что ПРЛ может играть ключевую роль в возникновении послеродовой депрессии (40, 41). Более того, повышение уровня ПРЛ, вызванное грудным вскармливанием, оказывает положительное влияние как на здоровье матери, так и на связь между матерью и младенцем. Была обнаружена корреляция между стрессом, дисфорическим настроением и сниженным уровнем гамма-интерферона у матерей, кормящих из бутылочки (42).Напротив, кормящие матери получили меньше баллов в тестах на тревожность, депрессию и гнев (43).
Нейрогенез и нейропротекция
Известно, что хроническое стрессовое воздействие и депрессивные состояния влияют на нейрогенез. Нейрогенез — это процесс, который производит новые нейроны на протяжении всей жизни. Считается, что новые нейроны временно улучшают нейронную связь. Во взрослом мозге обнаружены две нейрогенные ниши: гиппокамп и SVZ. Гиппокамп отрицательно контролирует активность оси HPA и участвует в эмоциональной модуляции.Антидепрессивные препараты усиливают нейрогенез в гиппокампе и показывают корреляцию с улучшением настроения (44). Нейрогенез обонятельной луковицы и обонятельная дисфункция также снижаются при воздействии CMS — процедуры, которая, как известно, вызывает депрессивные состояния (45).
Пролактин — регулятор нейрогенеза. Рецепторы ПРЛ экспрессируются в СВЗ и гиппокампе (46–48). Первоначальные доказательства взаимосвязи между ПРЛ и нейрогенезом были получены в исследованиях, показывающих усиление нейрогенеза в СВЗ беременных женщин.Было обнаружено, что это увеличение опосредовано ПРЛ (47), и была выдвинута гипотеза, что обонятельная дискриминация запахов, связанных с детенышами, имеет решающее значение для материнского успеха. Другие обонятельные сигналы являются важными сигналами, которые также вызывают нейрогенез в SVZ и в гиппокампе. Воздействие феромонов доминирующего самца вызывает пролиферацию клеток как в обонятельной луковице, так и в гиппокампе самок мышей. Эти эффекты опосредуются ПРЛ в обонятельной луковице и лютеинизирующим гормоном в гиппокампе, и оба гормона вносят вклад в регуляцию женского воспроизводства (49).Воздействие мужских феромонов увеличивает нейрогенез SVZ и способствует материнскому поведению у девственных и послеродовых женщин (50). Инъекции бромокриптина, агониста дофамина, самкам крыс в первые дни беременности для снижения уровня ПРЛ, снижают обонятельный нейрогенез и вызывают послеродовые изменения поведения (41). Эти сообщения ясно указывают на то, что ПРЛ может регулировать нейрогенез SVZ и играть ключевую роль в регуляции настроения.
Уменьшение нейрогенеза гиппокампа из-за воздействия хронического стресса предотвращалось ежедневным введением ПРЛ самцам мышей.Было показано, что ПРЛ способствует судьбе нейронов и оказывает нейропротекторное действие в гиппокампе (51). Первоначально считалось, что эффекты ПРЛ противодействуют глюкокортикоидному снижению пролиферации и выживаемости нейросферы. Однако инкубация ПРЛ вместе с дексаметазоном не могла подавить эффекты дексаметазона на нейросферы, несмотря на индукцию ERK1 / 2. Таким образом, было высказано предположение, что ПРЛ может влиять на нейрогенез гиппокампа через косвенный механизм (52). Следующие исследования показали как in vitro (в первичных клетках взрослого гиппокампа), так и in vivo (прямая инъекция в зубчатую извилину взрослых мышей), что введение ПРЛ увеличивает число нейросфер, что предполагает прямое влияние этого нейропептида на гиппокамп ( 53).Кроме того, эти авторы сообщили о поведенческих дефицитах у мышей с нулевым ПРЛ, обученных задачам обучения, зависящим от гиппокампа, и предположили роль ПРЛ в процессах обучения и памяти (53). Напротив, ежедневные инъекции ПРЛ крысам в течение первых двух постнатальных недель снижают нейрогенез как в зубчатой извилине, так и в обонятельной луковице и вызывают депрессивное состояние как у взрослых самцов, так и у самок крыс (54). Эти результаты предполагают, что ПРЛ по-разному влияет на нейрогенез в зависимости от возраста животных, и это может быть связано с эмоциональной регуляцией.
Во время беременности и кормления грудью ПРЛ защищает гиппокамп от высоких концентраций глюкокортикоидов (55). Введение овечьего ПРЛ в желудочек головного мозга девственных самок с удаленными яичниками буферизует нейродегенеративный процесс, вызванный инфузией каиновой кислоты в областях СА1, СА3 и СА4 гиппокампа (56, 57). Эти результаты предполагают нейрозащитную роль ПРЛ в гиппокампе.
Нейронные механизмы действия ПРЛ
Действие пролактина на нейрогенез опосредуется его активацией киназы 5 (ERK5), регулируемой внеклеточными сигналами.ERK5 экспрессируется в нейрогенных нишах мозга (58). Более того, ПРЛ увеличивает как экспрессию, так и уровни белка нестина и связанного с микротрубочками белка 2 (MAP2) в клетках нейробластомы (SK-N-SH). Это предполагает, что ПРЛ регулирует синтез белка цитоскелета и, следовательно, способствует дифференцировке нейронов (59). Кроме того, ПРЛ модулирует Ca 2+ -зависимые каналы K + , которые могут влиять на высвобождение нейротрансмиттеров в различных областях мозга (60).В гипоталамусе ПРЛ стимулирует путь ERK / MAPK в нейронах CRH, вазопрессина и окситоцина (61) и способствует экспрессии EGR-1 в магноцеллюлярных нейронах (62). Активация этих путей ПРЛ может способствовать пластическим изменениям, наблюдаемым в головном мозге во время беременности. Стимуляция ПРЛ транскрипции CRH в культивируемых клетках гипоталамуса интерпретируется как косвенный ингибирующий контроль ПРЛ на активность оси HPA (62). Однако до сих пор неизвестно, как PRL влияет на ось HPA.
Заключительные замечания и направления на будущее
Пролактин изменяет нейронные цепи, чтобы помочь человеку справиться со стрессом.Сниженная активация нервных входов, активация ионных каналов или модуляция нескольких сигнальных путей — вот некоторые из предполагаемых механизмов действия, лежащих в основе эффектов ПРЛ на мозговые цепи. Неизвестно, как ПРЛ регулирует функцию оси HPA во время стрессовой реакции. ПРЛ может влиять на активность гипоталамуса и / или гиппокампа, регулируя эмоциональность. Вклад ПРЛ в послеродовую депрессию до сих пор неизвестен. Низкий уровень ПРЛ у кормящих женщин был связан с послеродовой депрессией.Ингибирование ПРЛ снижает нейрогенез в обонятельной луковице, но механизмы, которые приводят к послеродовому депрессивному состоянию, неизвестны. Кроме того, пути, на которые влияет ПРЛ на регуляцию тревожности, еще не известны, и остается неясным, вносят ли эффекты ПРЛ на нейрогенез гиппокампа в модулирование тревожности. Введение ПРЛ на ранних постнатальных стадиях снижает нейрогенез в гиппокампе и обонятельной луковице и способствует депрессивному состоянию во взрослом возрасте. Это говорит о том, что ПРЛ влияет на критическое окно во время развития мозга и что действия ПРЛ зависят от возраста, в течение которого он применяется.Необходимы дальнейшие исследования, чтобы понять механизмы действия ПРЛ в головном мозге и то, как этот гормон модулирует эмоциональность и тревогу на разных этапах развития.
Вклад авторов
Автор подтверждает, что является единственным соавтором этой работы, и одобряет ее к публикации.
Заявление о конфликте интересов
Автор заявляет, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы рассматриваться как потенциальный конфликт интересов.
Финансирование
Финансирование было предоставлено LT за счет гранта FIS / IMSS / PROT / GII / 922 от Fondo de Investigación en Salud (FIS), принадлежащего Instituto Mexicano del Seguro Social (IMSS). FIS-IMSS больше не участвовал в разработке исследования, написании отчета и принятии решения о представлении статьи для публикации.
Ссылки
1. Боле-Фейсот С., Гоффин В., Эдери М., Бинарт Н., Келли П.А. Пролактин (ПРЛ) и его рецепторное действие, пути передачи сигнала и фенотипы, наблюдаемые у мышей с нокаутом рецепторов ПРЛ.Endocr Rev (1998) 19: 225–68.10.1210 / edrv.19.3.0334 [PubMed] [CrossRef] [Google Scholar] 2. Freeman ME, Kanyicska B, Lerant A, Nagy G. Пролактин: структура, функция и регуляция секреции. Physiol Rev (2000) 80 (4): 1523–631. [PubMed] [Google Scholar] 3. Клапп С., Торнер Л., Гутьеррес-Оспина Г., Алькантара Е., Лопес Ф. Дж., Нагано М. и др. Ген пролактина экспрессируется в гипоталамо-нейрогипофизарной системе, и белок процессируется во фрагмент 14 кДа с активностью, подобной пролактину 16 кДа.Proc Natl Acad Sci U S A (1994) 91: 10384–8.10.1073 / pnas.91.22.10384 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 4. Торнер Л., Малумби Р., Нава Г., Аранда Дж., Клапп С., Нойманн И.Д. Высвобождение in vivo и активация генов пролактина мозга в ответ на физиологические стимулы. Eur J Neurosci (2004) 19 (6): 1601–8.10.1111 / j.1460-9568.2004.03264.x [PubMed] [CrossRef] [Google Scholar] 5. Roselli CE, Bocklandt S, Stadelman HL, Wadsworth T, Vilain E, Stormshak F. Экспрессия пролактина в головном мозге овцы.Нейроэндокринология (2008) 87: 206–15.10.1159 / 000114643 [PubMed] [CrossRef] [Google Scholar] 6. Чайсеха Ю., Нгернсунгнерн П., Сартсунноен Н., Пракобсенг Н., Эль-Халавани М.Э. Присутствие мРНК пролактина во внегипофизарных областях мозга домашней индейки. Acta Histochem (2012) 114: 116–21.10.1016 / j.acthis.2011.03.007 [PubMed] [CrossRef] [Google Scholar] 7. Якоб С., Шраут К.Г., Шмитт А.Г., Шольц С.Дж., Ортега Г., Штайнбуш Х.В. и др. Дифференциальные эффекты пренатального стресса у самок 5-HTT-дефицитных мышей: в сторону молекулярных механизмов устойчивости.Dev Neurosci (2014) 36 (6): 454–64.10.1159 / 000363695 [PubMed] [CrossRef] [Google Scholar] 8. Уолш Р.Дж., Слаби Ф.Дж., Познер Б.И. Рецептор-опосредованный механизм транспорта пролактина из крови в спинномозговую жидкость. Эндокринология (1987) 120: 1846–50.10.1210 / endo-120-5-1846 [PubMed] [CrossRef] [Google Scholar] 9. Brown RS, Wyatt AK, Herbison RE, Knowles PJ, Ladyman SR, Binart N, et al. Транспорт пролактина в мозг мыши не зависит от рецептора пролактина. FASEB J (2015) 30 (2): 1002–10.10.1096 / fj.15-276519 [PubMed] [CrossRef] [Google Scholar] 10. Felicio LF, Bridges RS. Домперидон вызывает чувствительное к пробенециду повышение иммунореактивного пролактина в церебровентрикулярных перфузатах у самок крыс. Brain Res (1992) 573 (1): 133–8.10.1016 / 0006-8993 (92)-P [PubMed] [CrossRef] [Google Scholar] 11. Николсон Дж., Грили Г. Х., младший, Хамм Дж., Янгблад В. В., Кизер Дж. С.. Пролактин в спинномозговой жидкости — вероятное место ауторегуляции пролактина. Brain Res (1980) 190: 447–57.10.1016 / 0006-8993 (80)
-5 [PubMed] [CrossRef] [Google Scholar] 12.Томпсон С.А. Локализация иммунореактивного пролактина в эпендиме и окжелудочковых органах головного мозга крыс. Cell Tissue Res (1982) 225 (1): 79–93.10.1007 / BF00216220 [PubMed] [CrossRef] [Google Scholar] 13. Das R, Vonderhaar BK. Передача сигнала роста пролактина (ПРЛ) через длинные и короткие формы рецептора ПРЛ. Mol Endocrinol (1995) 9: 1750–9.10.1210 / mend.9.12.8614411 [PubMed] [CrossRef] [Google Scholar] 14. Перро-Аппланат М., Гуалильо О, Пезет А., Винсент В., Эдери М., Келли П.А. Доминирующие негативные и кооперативные эффекты мутантных форм рецептора пролактина.Mol Endocrinol (1997) 11: 1020–32.10.1210 / исправление.11.8.9954 [PubMed] [CrossRef] [Google Scholar] 15. Gala RR. Физиология и механизмы стресс-индуцированных изменений секреции пролактина у крыс. Life Sci (1990) 46 (20): 1407–20.10.1016 / 0024-3205 (90)-U [PubMed] [CrossRef] [Google Scholar] 21.Toufexis DJ, Tesolin S, Huang N, Walker C. Измененная чувствительность гипофиза к кортикотропин-рилизинг-фактору и аргинин-вазопрессину участвует в стрессовой гипореактивности лактации у крыс. J. Neuroendocrinol (1999) 11 (10): 757–64.10.1046 / j.1365-2826.1999.00381.x [PubMed] [CrossRef] [Google Scholar] 22. Landgraf R, Wigger A, Holsboer F, Neumann ID. Гиперреактивная ось гипоталамо-гипофиз-надпочечник у крыс, разводимых для поведения, связанного с высокой тревожностью. Дж. Нейроэндокринол (1999) 11 (6): 405–7.10.1046 / j.1365-2826.1999.00342.x [PubMed] [CrossRef] [Google Scholar] 23. Стеймер Т., Дрисколл П. Дивергентные реакции на стресс и стили совладания у психогенетически отобранных римских крыс с высоким (RHA) и низким (RLA) избеганием: поведенческие, нейроэндокринные аспекты и аспекты развития. Стресс (2003) 6 (2): 87–100.10.1080 / 102538
00111320 [PubMed] [CrossRef] [Google Scholar] 24. Ривли А., Фишер А. Д., Оуэн Д., Крид Ф. Х., Дэвис-младший. Психологический стресс у пациентов с гиперпролактинемией. Clin Endocrinol (Oxf) (1997) 47 (3): 343–8.10.1046 / j.1365-2265.1997.2701073.x [PubMed] [CrossRef] [Google Scholar] 25. Драго Ф., Пульвиренти Л., Спадаро Ф., Пеннсини Дж. Эффекты ТРГ и пролактина в модели депрессии в поведенческом отчаянии (плавание) у крыс. Психонейроэндокринология (1990) 15: 349–56.10.1016 / 0306-4530 (90)
-M [PubMed] [CrossRef] [Google Scholar] 26. Oliveira MC, Pizarro CB, Golbert L, Micheletto C. Гиперпролактинемия и психологическое расстройство. Arq Neuropsiquiatr (2000) 58 (3A): 671–6.10.1590 / S0004-282X2000000400012 [PubMed] [CrossRef] [Google Scholar] 27.Mohankumar PS, Mohankumar SM, Quadri SK, Voogt JL. Хроническая гиперпролактинемия и изменения дофаминовых нейронов. Brain Res Bull (1997) 42 (6): 435–41.10.1016 / S0361-9230 (96) 00369-3 [PubMed] [CrossRef] [Google Scholar] 28. Гоффин В., Бинарт Н., Турень П., Келли П.А. Пролактин: новая биология старого гормона. Анну Рев Физиол (2002) 64: 47–67.10.1146 / annurev.physiol.64.081501.131049 [PubMed] [CrossRef] [Google Scholar] 29. Заморано М., Ледесма-Колунга М.Г., Адан Н., Вера-Массиу С., Лемини М., Мендес И. и др.Вазоингибины, производные пролактина, усиливают поведение, связанное с тревогой и депрессией. Психонейроэндокринология (2014) 44: 123–32.10.1016 / j.psyneuen.2014.03.006 [PubMed] [CrossRef] [Google Scholar] 30. О’Хара М.В., Шлехте Д.А., Льюис Д.А., Райт Э.Дж. Проспективное изучение биологических и психосоциальных факторов послеродовой хандры. Arch Gen Psychiatry (1991) 48: 801–6.10.1001 / archpsyc.1991.01810330025004 [PubMed] [CrossRef] [Google Scholar] 31. Bosch OJ, Müsch W., Bredewold R, Slattery DA, Neumann ID. Пренатальный стресс увеличивает активность оси HPA и ухудшает заботу о матери в кормящих потомках женского пола: последствия для послеродового расстройства настроения.Психонейроэндокринология (2007) 32 (3): 267–78.10.1016 / j.psyneuen.2006.12.012 [PubMed] [CrossRef] [Google Scholar] 32. Смит Дж. В., Секл Дж. Р., Эванс А. Т., Косталл Б., Смайт Дж. В.. Гестационный стресс вызывает послеродовую депрессию и изменяет материнский уход у крыс. Психонейроэндокринология (2004) 29 (2): 227–44.10.1016 / S0306-4530 (03) 00025-8 [PubMed] [CrossRef] [Google Scholar] 33. Смит М.В., Шао Л., Хауэлл Х., Лин Х., Йонкерс К.А. Перинатальная депрессия и исходы родов в проекте здорового старта. Matern Child Health J (2011) 15: 401–9.10.1007 / s10995-010-0595-6 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Гиллерер К.М., Ребер С.О., Нойманн И.Д., Слэттери Д.А. Воздействие хронического стресса во время беременности меняет послеродовую адаптацию: последствия для послеродовой тревожности и расстройств настроения. Эндокринология (2011) 152 (10): 3930–40.10.1210 / en.2011-1091 [PubMed] [CrossRef] [Google Scholar] 35. Heinrichs M, Meinlschmidt G, Neumann I, Wagner S, Kirschbaum C, Ehlert U, et al. Влияние сосания на ответы оси гипоталамус-гипофиз-надпочечники на психосоциальный стресс у кормящих женщин в послеродовом периоде.J Clin Endocrinol Metab (2001) 86: 4798–804.10.1210 / jcem.86.10.7919 [PubMed] [CrossRef] [Google Scholar] 36. Лайт К.С., Грюен К.М., Амико Дж. А., Бочча М., Браунли К. А., Джонс Дж. М.. Дефицит реакции окситоцина в плазме и усиление негативных эмоций, стресса и артериального давления у матерей, подвергшихся воздействию кокаина во время беременности. Addict Behav (2004) 29 (8): 1541–64.10.1016 / j.addbeh.2004.02.062 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 37. Skrundz M, Bolten M, Nast I, Hellhammer DH, Meinlschmidt G. Концентрация окситоцина в плазме во время беременности связана с развитием послеродовой депрессии.Нейропсихофармакология (2011) 36 (9): 1886–93.10.1038 / npp.2011.74 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 38. Sjoeholm A, Bridges RS, Grattan DR, Anderson GM. Повышение чувствительности к пролактину у репродуктивных самок крыс, специфичных для регионов, нейронов и сигнальных путей. Эндокринология (2011) 152 (5): 1979–88.10.1210 / en.2010-1220 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39. Абу-Салех М.Т., Губаш Р., Карим Л., Крымски М., Бхаи И. Гормональные аспекты послеродовой депрессии.Психонейроэндокринология (1998) 23 (5): 465–75.10.1016 / S0306-4530 (98) 00022-5 [PubMed] [CrossRef] [Google Scholar] 40. Ларсен CM, Grattan DR. Вызванный пролактином митогенез в субвентрикулярной зоне материнского мозга на ранних сроках беременности важен для нормальных послеродовых поведенческих реакций у матери. Эндокринология (2010) 151 (8): 3805–14.10.1210 / en.2009-1385 [PubMed] [CrossRef] [Google Scholar] 41. Ларсен CM, Grattan DR. Пролактин, нейрогенез и материнское поведение. Иммунное поведение мозга (2012) 26 (2): 201–9.10.1016 / j.bbi.2011.07.233 [PubMed] [CrossRef] [Google Scholar] 42. Гроер М.В., Дэвис М.В. Цитокины, инфекции, стресс и дисфорическое настроение у лиц, кормящих грудью и кормящих смесью. J Obstet Gynecol Neonatal Nurs (2006) 35 (5): 599–607.10.1111 / j.1552-6909.2006.00083.x [PubMed] [CrossRef] [Google Scholar] 43. Groër MW. Различия между исключительно кормящими грудью, кормящими смесями и контрольной группой: исследование стресса, настроения и эндокринных переменных. Биол Рес Нурс (2005) 7 (2): 106–17.10.1177 / 1099800405280936 [PubMed] [CrossRef] [Google Scholar] 44.Santarelli L, Saxe M, Gross C, Surget A, Battaglia F, Dulawa S и др. Необходимость нейрогенеза гиппокампа для поведенческих эффектов антидепрессантов. Science (2003) 301 (5634): 805–9.10.1126 / science.1083328 [PubMed] [CrossRef] [Google Scholar] 45. Ян Д., Ли Кью, Фанг Л., Ченг К., Чжан Р., Чжэн П. и др. Сниженный нейрогенез и пресинаптическая дисфункция в обонятельной луковице крысиной модели депрессии. Неврология (2011) 192: 609–18.10.1016 / j.neuroscience.2011.06.043 [PubMed] [CrossRef] [Google Scholar] 46.Ногами Х., Хосино Р., Огасавара К., Миямото С., Хисано С. Регионоспецифическая экспрессия и гормональная регуляция вариантов первого экзона мРНК рецептора пролактина крысы в головном мозге и передней доле гипофиза. J Neuroendocrinol (2007) 19: 583–93.10.1111 / j.1365-2826.2007.01565.x [PubMed] [CrossRef] [Google Scholar] 47. Шинго Т., Грегг С., Энвере Э, Фудзикава Х., Хассам Р., Гири С. и др. Стимулированный беременностью нейрогенез в переднем мозге взрослой женщины, опосредованный пролактином. Наука (2003) 299: 117–20.10.1126 / science.1076647 [PubMed] [CrossRef] [Google Scholar] 48. Мак Г.К., Вайс С. Отцовское распознавание взрослого потомства, опосредованное вновь созданными нейронами ЦНС. Nat Neurosci (2010) 13 (6): 753–8.10.1038 / nn.2550 [PubMed] [CrossRef] [Google Scholar] 49. Мак Г.К., Энвере Е.К., Грегг С., Пакарайнен Т., Поутанен М., Хухтаниеми И. и др. Стимулированный мужскими феромонами нейрогенез в мозге взрослой женщины: возможная роль в брачном поведении. Nat Neurosci (2007) 10 (8): 1003–11.10.1038 / nn1928 [PubMed] [CrossRef] [Google Scholar] 50.Ларсен CM, Kokay IC, Grattan DR. Феромоны мужского пола инициируют индуцированный пролактином нейрогенез и улучшают материнское поведение у самок мышей. Horm Behav (2008) 53 (4): 509–17.10.1016 / j.yhbeh.2007.11.020 [PubMed] [CrossRef] [Google Scholar] 51. Торнер Л., Карг С., Блюм А., Кандасами М., Кун Г. Г., Винклер Дж. И др. Пролактин предотвращает вызванное хроническим стрессом снижение нейрогенеза в гиппокампе взрослых и способствует судьбе нейронов. J Neurosci (2009) 29 (6): 1826–33.10.1523 / JNEUROSCI.3178-08.2009 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 52.Wagner K, Couillard-Despres S, Lehner B, Brockhoff G, Rivera FJ, Blume A и др. Пролактин индуцирует передачу сигналов MAPK в нейральных предшественниках без ослабления индуцированного глюкокортикоидами ингибирования нейрогенеза in vitro. Cell Physiol Biochem (2009) 24 (5-6): 397-406.10.1159 / 000257432 [PubMed] [CrossRef] [Google Scholar] 53. Уокер Т.Л., Вукович Дж., Кудийс М.М., Блэкмор Д.Г., Маккей Э.В., Сайкс А.М. и др. Пролактин стимулирует клетки-предшественники в гиппокампе взрослых мышей. PLoS One (2012) 7 (9): e44371.10.1371 / journal.pone.0044371 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 54. Ладжуд Н., Гонсалес-Запиен Р., Роке А., Тинахеро Э., Вальдес Дж. Дж., Клапп С. и др. Введение пролактина в ранний постнатальный период снижает нейрогенез гиппокампа и обонятельных луковиц и приводит к депрессивному поведению во взрослом возрасте. Horm Behav (2013) 64 (5): 781–9.10.1016 / j.yhbeh.2013.10.005 [PubMed] [CrossRef] [Google Scholar] 55. Моралес Т. Последние данные о нейропротекции против эксайтотоксичности в гиппокампе самок крыс.J. Neuroendocrinol (2011) 23 (11): 994–1001.10.1111 / j.1365-2826.2011.02141.x [PubMed] [CrossRef] [Google Scholar] 56. Техадилла Д., Цербон М., Моралес Т. Пролактин снижает повреждающие эффекты эксайтотоксичности в дорсальном гиппокампе самки крысы независимо от гормонов яичников. Неврология (2010) 169 (3): 1178–85.10.1016 / j.neuroscience.2010.05.074 [PubMed] [CrossRef] [Google Scholar] 57. Моралес Т., Лоренсон М., Уокер А.М., Рамос Э. Как пролактин (PRL), так и молекулярный имитатор фосфорилированного PRL, S179D-PRL, защищают гиппокамп самок крыс от эксайтотоксичности.Neuroscience (2014) 258: 211–7.10.1016 / j.neuroscience.2013.11.015 [PubMed] [CrossRef] [Google Scholar] 58. Ван В., Пань Ю.В., Виетеча Т., Цзоу Дж., Абель Г.М., Куо С.Т. и др. Киназа 5 (ERK5), регулируемая внеклеточными сигналами, опосредует стимулируемый пролактином нейрогенез взрослых в субвентрикулярной зоне и обонятельной луковице. J Biol Chem (2013) 288 (4): 2623–31.10.1074 / jbc.M112.401091 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 59. Havránek T, Bačová Z, Štrbák V, Lešťanová Z, Bakoš J. Пролактин увеличивает экспрессию белков цитоскелета в клетках SK-N-SH.Folia Biol (Praha) (2014) 60 (6): 281–5. [PubMed] [Google Scholar] 60. Патил М.Дж., Генри М.А., Акопян А.Н. Рецептор пролактина в регуляции возбудимости нейронов и каналов. Каналы (Остин) (2014) 8 (3): 193–202.10.4161 / chan.28946 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 61. Блюм А., Торнер Л., Лю Ю., Суббураджу С., Агилера Г., Нойманн И.Д. Пролактин активирует передачу сигналов митоген-активируемой протеинкиназы и транскрипцию рилизинг-гормона кортикотропина в нейронах гипоталамуса крыс. Эндокринология (2009) 150 (4): 1841–9.10.1210 / en.2008-1023 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 62. Блюм А., Торнер Л., Лю Ю., Суббураджу С., Агилера Г., Нойманн И.Д. Пролактин индуцирует экспрессию гена Egr-1 в культивируемых клетках гипоталамуса и в гипоталамусе крыс. Brain Res (2009) 1302: 34–41.10.1016 / j.brainres.2009.09.047 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
(PDF) Гиперпролактинемия, вызванная стрессом: патофизиология и клинический подход
[18] К. Бриет, М. Сараваль, С. Лорик, Х. Тополински-Дуйм, С.Fendri,
и R. Desailloud, «Использование внутривенной катетеризации
с периодом покоя полезно для определения уровней кортизола в плазме
, но не уровней пролактина в плазме», Annales
d’Endocrinologie, vol. 68, нет. 1, pp. 34–38, 2007.
[19] M. Me, «Prolactinoma», in ine Pituitary, pp. 455–495, Wiley-
Blackwell, Malden, MA, USA, 2002.
[20] PJ Newey, CM Gorvin и RV akker, «Мутантный рецептор пролактина
и семейная гиперпролактинемия», New
England Journal of Medicine, vol.370, нет. 10, pp. 977-978,
2014.
[21] Д. Шоуп, «Учебник Мишелла по бесплодию, контрацепции
и репродуктивной эндокринологии», в HDA Treatment,
Blackwell Scienti ‑ Publications, Кембридж, Массачусетс, США. , 1997.
[22] Ф. Кокер и Д. Тейлор, «Вызванная антидепрессантами гипер-
пролактинемия: частота, механизмы и лечение»,
Препараты для ЦНС, том. 24, вып. 7, pp. 563–574, 2010.
[23] М. Е. Молитч, «Гиперпролактинемия, вызванная лекарствами»,
Mayo Clinic Proceedings, vol.80, нет. 8, pp. 1050–1057, 2005.
[24] М. Э. Молич, «Лекарства и пролактин», Гипофиз, т. 8, с. 11, вып. 2,
pp. 209–218, 2008.
[25] PC Yang, J. Jury, JD S¨
oderholm, PM Sherman,
DM McKay, и MH Perdue, «Хронический психологический стресс
в крысы индуцируют сенсибилизацию кишечника к an-
тигенам в просвете кишечника », American Journal of Pathology, vol. 168, нет. 1,
pp. 104–114, 2006.
[26] Х. Акияма, Х.Амано и Дж. Биненсток, «Эпителиальные реакции трахеи
икрыс на стресс избегания воды», Журнал
Аллергия и клиническая иммунология, вып. 116, нет. 2, pp. 318–324,
2005.
[27] К. Слива, Дж. Фетт и У. Элькаям, «Перипартальный кардиомиоп-
athy», Lancet, vol. 368, нет. 9536, pp. 687–693, 2006.
[28] Дж. Сонг, М. Ван, X. Чен и др., «Пролактин опосредует эффекты хронического психологического стресса
на индукцию жировых клеток в
сердце. , ”Американский журнал трансляционных исследований, т.8,
нет. 2, pp. 644–652, 2016.
[29] С. Джароенпорн, К. Нагаока, К. Касахара, Р. Охта,
Г. Ватанабе и К. Тайя, «Физиологическая роль пролактина в
. адренокортикальный ответ на острый ограничивающий стресс », Endo-
crine Journal, vol. 54, нет. 5, pp. 703–711, 2007.
[30] Р. Ф. Вебер и А. Э. Калоджеро, «Пролактин стимулирует крыс
гипоталамический кортикотропин-рилизинг-гормон и гипофиз
секреция адренокортикотропина in vitro», Нейроэндокринология,
0002.54, нет. 3, pp. 248–253, 1991.[31] A. Kooy, WJ de Greef, JTM Vreeburg et al., «Доказательства
участия фактора высвобождения кортикотропина в ингибировании гонадотропина». высвобождение, вызванное пролактинемией гипер-
, Нейроэндокринология, т. 51, нет. 3,
pp. 261–266, 1990.
[32] К. Хигучи, Х. Навата, Т. Маки, М. Хигашизима, К.И. Като,
и Х. Ибаяси, «Пролактин оказывает прямое действие на надпочечники
секреция андрогенов », Журнал клинической эндокринологии и метаболизма
, вып.59, нет. 4, pp. 714–718, 1984.
[33] A. Glasow, M. Breidert, A. Haidan, U. Anderegg, PA Kelly,
и SR Bornstein, «Функциональные аспекты действия пролактина
. (PRL) о стероидогенезе надпочечников и распределении рецептора PRL
в надпочечниках человека », Journal of
Clinical Endocrinology and Metabolism, vol. 81, нет. 8,
pp. 3103–3111, 1996.
[34] LL Chang, MJ Lo, SF Kan et al., «Прямое влияние пролактина
на высвобождение кортикостерона zona fasciculata-
ретикулярных клеток самцов крыс. , ”Journal of Cellular Bio-
Chemistry, vol.73, нет. 4, pp. 563–572, 1999.
[35] Н. Сонино, К. Наваррини, К. Руини, Ф. Фалло, М. Боскаро и
Г. Фава, «Жизненные события в патогенезе гипер —
пролактинемия », Европейский журнал эндокринологии, вып. 151,
нет. 1, pp. 61–65, 2004.
[36] RB Machado, MR Rocha и D. Suchecki, «Brain pro-
лактин участвует в индуцированном стрессом восстановлении быстрого сна»,
Hormones and Behavior. т. 89, стр. 38–47, 2017.
[37] T.Фудзикава, Х. Соя, К. Л. К. Тамаширо и др., «Пролактин
предотвращает острую вызванную стрессом гипокальциемию и язвенный генез
, воздействуя на мозг крысы», Эндокринология, том. 145,
нет. 4, pp. 2006–2013, 2004.
[38] SE Kirk, T.Y Xie, FJ Steyn, DR Grattan, and SJ Bunn,
«Сдерживающий стресс увеличивает опосредованное пролактином фосфорилирование —
сигнального преобразователя и активатора. транскрипции 5 в гипоталамусе и коре надпочечников
у самцов мышей », Journal
of Neuroendocrinology, vol.29, нет. 6, 2017.
[39] Б. И. Перри, К. Дж. Голдринг и С. Дж. Менон, «Мониторинг пролактина
в условиях острой психиатрии», Psychiatry Re-
search, vol. 235, pp. 104–109, 2016.
[40] A. Riecher-Rossler, JK Rybakowski, MO Püeger et al.,
«Гиперпролактинемия у пациентов, ранее не получавших антипсихотики, с
первого эпизода психоза», Психологическая медицина. , т. 43,
нет. 12, pp. 2571–2582, 2013.
[41] M.C. Nunes, L.G. Sobrinho, C. Calhaz-Jorge, M. A. Santos,
J. C. Mauricio и M. F. Sousa, «Психосоматические факторы у
пациентов с гиперпролактинемией и / или галактореей», Ob-
stetrics and Gynecology, vol. 55, нет. 5, pp. 591–595, 1980.
[42] Л. Г. Собринью, «Пролактин, психологический стресс и окружающая среда: адаптация и дезадаптация», Pitui-
tary, vol. 6, вып. 1, pp. 35–39, 2003.
[43] Q. J. Bo, Z. M. Wang, X.B. Li, X. Ma, C. Y. Wang и
J. de Leon, «Дополнительный метформин для гиперпролактинемии, вызванной нейролептиками
: систематический обзор», Psychiatry Re-
search, vol. 237, pp. 257–263, 2016.
[44] Р. Крысяк, В. Шкробка и Б. Окопиен, «Альтернативные стратегии лечения
у женщин, плохо переносящих умеренные дозы
бромокриптина», Экспериментальная и клиническая эндоскопия. —
Кринология и диабет, т. 125, нет. 6. С. 360–364, 2017.
[45] М. Помпили, Г. Серафини, М. Палермо и др., «Гипоталамическая
ось гипофиза и надпочечники и аномалии пролактина при суицидальном поведении
», ЦНС и неврологические расстройства — мишени для лекарств,
тома. 12, вып. 7, pp. 954–970, 2013.
6Abstetrics and Gynecology International
Связь между самовоспринимаемым стрессом, психопатологическими симптомами и гормоном стресса пролактином при зарождающемся психозе
Abstract
Общие сведения
Психосоциальный стресс и гормон стресса пролактин Предполагается, что они играют важную роль в патогенезе шизофрении и связанных с ней психозов, и часто наблюдается повышение у пациентов, ранее не принимавших антипсихотики, с клиническим высоким риском психоза (CHR-P) или первого эпизода психоза (FEP).Целью этого исследования было дальнейшее выяснение взаимосвязи между самооценкой стресса, психопатологическими симптомами и уровнями пролактина у этих пациентов.
Методы
В этом поперечном исследовании 45 здоровых людей из контрольной группы, 31 пациент CHR-P и 87 пациентов FEP были набраны из двух разных исследовательских центров. Пролактин измеряли в стандартных условиях между 8 и 10 часами утра. Все пациенты не получали антипсихотические препараты и не принимали никаких препаратов, влияющих на пролактин.Самостоятельно воспринимаемый стресс в течение последнего месяца измерялся по шкале воспринимаемого стресса (PSS-10) непосредственно перед взятием крови.
Результаты
Пациенты с CHR-P и FEP показали значительно более высокие уровни стресса и пролактина, чем в контрольной группе. Гиперпролактинемия (то есть уровни пролактина выше нормального диапазона) наблюдалась у 26% пациентов с CHR-P и 45% пациентов с FEP. Самооценка стресса была достоверно положительно связана с аффективными симптомами, но не с другими симптомами.Не было значимой связи между самооценкой стресса и уровнем пролактина.
Заключение
Наши результаты подтверждают, что пациенты с CHR-P и FEP имеют более высокий уровень стресса, чем здоровые люди в контрольной группе, и часто имеют гиперпролактинемию, независимо от приема антипсихотических препаратов. Однако, хотя хорошо известно, что уровень пролактина повышается в ответ на стресс, наши результаты не подтверждают мнение о том, что повышенный уровень пролактина у этих пациентов вызван стрессом.
Ключевые слова
Шизофрения
Стресс
Психическое состояние, подверженное риску
Пролактин
Клинический высокий риск
Психоз
Рекомендуемые статьиЦитирующие статьи (0)
Просмотр аннотации© 2020 Автор (ы).Опубликовано Elsevier Ltd.
Рекомендуемые статьи
Цитирующие статьи
Животные | Бесплатный полнотекстовый | Исследование роли пролактина как потенциального биомаркера стресса у кастрированных домашних собак-самцов
1. Введение
Хотя гормон пролактин известен своей функцией в стимуляции роста молочной железы и процессов лактации, он имеет более 300 различная биологическая активность, гомеостатические роли и физиологические функции в организме, e.g., электролитный баланс, лютеиновая функция, регуляция иммунной системы, осморегуляция, ангиогенез и поддержание межэстового промежутка [1]. Фактически, важная генетическая роль рецептора пролактина (PRL-R) в энергетическом балансе и метаболической адаптации была недавно доказана у грызунов, доказывая, что пролактин играет важную роль в метаболизме глюкозы, инсулина и липидов, а также в стимулировании положительный энергетический баланс [2]. Кроме того, было обнаружено, что пролактин является показателем острого стресса у некоторых видов животных, кроме человека, таких как крысы [3,4,5], домашние жвачные животные [6], ослы [7], крупный рогатый скот [8] и овцы. [9]; также были продемонстрированы различные специфические функции пролактина во время реакции на стресс [2], такие как посредничество в адаптации эпидермиса к стрессу окружающей среды у рыб [10].Недавно было обнаружено, что передача сигналов пролактина в нейронах тубероинфундибулярного дофамина (TIDA) снижена у мышей, подвергшихся острому стрессу, с последующим потенциальным снижением их ингибирующего влияния на секрецию пролактина [11]. Это предполагает, что пролактин, секретируемый в ответ на острый стресс, может активировать рецепторы пролактина в определенных тканях, участвующих в физиологической адаптации к стрессу [11]. У людей пролактин стимулируется сосанием, восприятием визуальных, акустических и обонятельных стимулов, а также стрессом [12], включая психологические и психосоциальные стрессы [13], и экспериментальными стрессовыми состояниями, такими как гипогликемия [14], хирургия [14], прыжки с парашютом у призывников [15] и обязательное плавание у не умеющих плавать [16].Фактически, кортизол, пролактин и ежедневные изменения индексов тревожности, измеренные с помощью анкет, были значительно коррелированы [17]. Однако в научной литературе сообщается о различных результатах как с неизменным [18,19], так и с пониженным уровнем пролактина [ 20,21,22] в ответ на стресс, ставя под сомнение веру в то, что стресс стимулирует секрецию пролактина [23]. Кроме того, хотя было обнаружено, что уровни кортизола коррелируют с уровнями тревожности за день до хирургического вмешательства, никакой существенной корреляции между пролактином и тревогой обнаружено не было [24].Что касается домашней собаки (Canis familis), насколько нам известно, потенциальная связь между стрессом и уровнем пролактина практически не исследована. Одно исследование, посвященное оценке связанного с хирургическим вмешательством стресса у собак, показало, что кортизол повышался, а пролактин снижался в послеоперационный период по сравнению с базовыми уровнями [25], причем последнее контрастировало с повышенным послеоперационным ответом пролактина, обнаруженным у людей после операции [26]. . Авторы предположили, что этот контраст может показывать, что разные виды могут проявлять различия в активации систем регуляции обратной связи пролактина [25].В нескольких исследованиях сообщалось, что у собак с генерализованной тревогой была гиперпролактинемия, а у собак с фобиями или легкой тревожностью — нет [27,28]. Уровни пролактина в крови положительно коррелировали с оценкой, полученной по индивидуальной шкале для количественной оценки наличия поведения, связанного с тревогой, посредством физической и поведенческой оценки [28]. Фактически, у собак, страдающих различными видами генерализованной тревоги, наблюдалось значительное снижение уровня дофамина в крови [29], что может служить основанием для измерения пролактина, поскольку его секреция в основном контролируется дофаминергическими нейронами [28].Однако участие пролактина в эмоциональных реакциях у собак кажется более сложным, поскольку было показано, что его циркулирующие концентрации увеличиваются также во время позитивного взаимодействия с людьми [30]. Кортизол обычно считается «гормоном стресса»; Фактически, кортизол и его метаболиты были количественно определены в различных матрицах образцов, таких как кровь, слюна, моча и фекалии [31], а недавно и в волосах [32,33,34], как эндокринная реакция на стресс. Было показано, что уровень кортизола увеличивается в неблагоприятных условиях, таких как изоляция, ограничение передвижения, перегруппировка или транспортировка [35].Фактически, кортизол секретируется после активации оси гипоталамус-гипофиз-надпочечники (HPA), одной из основных систем реакции на стресс [36]. Тем не менее, повышенная активность HPA не является специфической для стресса, поскольку она также может быть вызвана метаболическими процессами, положительными аффективными состояниями, поведением матери и физической активностью [37,38,39,40]. По этой причине некоторые авторы предполагают, что повышение уровня кортизола следует рассматривать как индикатор возбуждения [37], а не стресса. Надежность кортизола при оценке стресса дополнительно подвергается сомнению из-за многих факторов, которые могут влиять на интерпретация уровней кортизола, таких как индивидуальная вариабельность реакции на стрессовое воздействие [41,42], высокая межиндивидуальная вариабельность исходного уровня кортизола между собаками [43], затруднения при заборе крови [44] и возможные вариации из-за циркадный ритм [44], причем последний четко не идентифицирован у домашних собак: на самом деле, у лабораторных [45] и рабочих собак [46,47] с интервалами 24–28 часов не сообщалось о циркадном ритме кортизола.Все эти факторы требуют осторожности при сравнении уровней кортизола в группах разных собак, а также при оценке долгосрочной секреции кортизола из жидкостей, таких как кровь, моча и слюна [44]. Оценка уровня кортизола может дополнительно осложняться изменениями в зависимости от продолжительности стресса. В то время как в присутствии сыворотки, вызывающей острый стрессор, кортизол быстро увеличивается, а затем возвращается к базовым уровням, в ситуации хронического стресса длительное воздействие стрессора может привести к подавлению и дерегулированию оси HPA [48], что обычно не означает нормализации уровня циркулирующего кортизола, и, таким образом, они являются очень полезным показателем хронического стресса [49].В последние годы анализ кортизола волос был также подтвержден как надежное отражение долгосрочной секреции кортизола [50,51]. Кортизол и пролактин, по-видимому, оба участвуют в реакции на стресс, и их уровни, вероятно, каким-то образом связаны. Например, эксперименты in vitro показали более высокие базальные уровни кортикостерона у гиперпролактинемических крыс, чем у нормальных и гипопролактинемических крыс; пролактин оказывает стимулирующее действие на АКТГ-индуцированную секрецию кортикостерона при остром ограничительном стрессе [52].Тем не менее, реакция гормонов пролактина и кортизола на стрессовую ситуацию может быть различной, и некоторые авторы предполагают, что высвобождение пролактина может выступать в качестве альтернативной формы реакции кортизола на стресс [22]. У собак оценка стресса часто бывает сочетание физиологических и поведенческих параметров, последний обычно считается надежным индикатором [53,54]. Например, после индукции хронического стресса с помощью модели социальных и пространственных ограничений собаки, живущие в небольших комнатных вольерах, демонстрировали значительно более низкие позы [55], а также повышение уровня кортизола [56] по сравнению с собаками, живущими в обогащенных просторных помещениях. уличное жилье группами.В условиях короткого питомника собаки, как правило, были более активными [36,57], а их соотношение кортизол: креатинин (C / Cr) было значительно выше по сравнению с тем, когда они находились в домашних условиях [36].Целью этого оппортунистического исследования было оценить, существует ли корреляция между концентрациями кортизола и пролактина в сыворотке и между ними и поведенческими индикаторами стресса и страха у домашних собак. Чтобы уменьшить влияние возможных влияющих факторов, таких как пол, состояние стерилизации, порода и условия содержания, это исследование было проведено на однородной выборке кастрированных самцов испанских борзых, содержавшихся более 155 дней в приюте для собак.У этой породы сложный социальный контекст на юге Испании, где проводилось это исследование, с частыми сообщениями о жестоком обращении и пренебрежении. Следовательно, они могли испытать предыдущий общий неблагоприятный опыт до того, как их спасли, что могло усилить однородность образца.
Гипотеза этого исследования заключалась в том, что, как ранее предполагали другие авторы, пролактин мог использоваться в качестве биомаркера стресса у домашних собак и по этой причине он коррелировал с другими показателями, связанными со стрессом, такими как уровень кортизола в сыворотке крови, наличие страха или частота поведения, связанного со стрессом, у собак.Секреция пролактина гипофизом используется в качестве маркера активации лактотропной оси [58], было обнаружено, что он является показателем острого стресса у некоторых видов и выполняет определенные функции во время стрессовой реакции [2]. Однако из-за противоречивых результатов в литературе мы не делали никаких прогнозов относительно возможного повышения или снижения уровня пролактина в стрессовом состоянии.Это исследование включает в себя некоторые элементы новизны, такие как, насколько нам известно, первое, включающее несколько показателей стресса, как гормонального, так и поведенческого (пролактин, кортизол и поведение, связанное со стрессом и страхом), изучение их возможной корреляции и включение таких однородная выборка домашних собак, все из которых принадлежат к одной породе, являются кастрированными самцами и живут в одной среде.
2. Материалы и методы
Процедура была доведена до сведения Этического комитета Пизанского университета, Италия, и получила положительное заключение Решением № 09/2018.
2.1. Субъекты и место
Образцы были собраны в период с 3 сентября 8 сентября по 26 ноября ноября 2018 у 40 кастрированных взрослых самцов испанских борзых собак (средний возраст ± стандартное отклонение = 46,5 ± 20,8 месяцев; мин. = 19; макс. = 112 месяцев). Собак разместили в Fundación Benjamin Mehnert (Севилья, Испания).
Собаки, вошедшие в приют, либо бродили в одиночестве, вероятно, после того, как их бросили, иногда сбивали машиной, либо пришли прямо из отходов охотников или сообщений о жестоком обращении и жестоком обращении. Все они находились в приюте на срок более 155 дней (270,9 ± 115,6 дней), были здоровы и регулярно проверялись ветеринаром.
Укрытие включает крытое пространство 2000 м 2 , разделенное на 2 ряда и 3 основных коридора, в общей сложности 60 ящиков, в каждом из которых есть 1-3 пластиковые кровати (88 × 58 × 28 см), в зависимости от количества собак, разделяющих бокс.Кроме кормушки и ведра с водой, в ящиках не было других предметов, например игрушек. Собаки выходили на внешние дворы небольшими группами два раза в день.
Собаки обычно жили в группе из 3–4 собак (92,5% случаев), все испанские борзые, делили одну будку в течение нескольких дней или недель; в нескольких случаях (n = 3) пять собак содержались вместе. Персонал приюта организовал собак в группы, которые обеспечивали максимально возможную социальную стабильность, частично уравновешивая риск стресса из-за перенаселенности или конфликтов.
2.2. Видеоанализ
Каждую собаку записывали 10-минутное видео с помощью видеокамеры (JVC GZ-MG130E, Йокогама, Япония), расположенной примерно в одном метре от ограждения бокса (максимально возможное расстояние для покрытия всего бокса) и на стабильная высота 100 см. Видео записывались с 8:30 до 15:00. Чтобы облегчить распознавание каждой собаки на видео, были зарегистрированы их наиболее характерные физические характеристики и был сделан снимок.
Видео были проанализированы с использованием BORIS (интерактивное программное обеспечение для исследования поведенческих наблюдений, Туринский университет, Турин, Италия) [59].Был составлен список из 18 возможных признаков стресса у собак [54,60,61,62,63], и для каждого из них регистрировалось количество проявлений (наблюдений). Оценка стресса была рассчитана для каждой собаки путем суммирования общего количества проявлений каждого из следующих связанных со стрессом поведений: зевота, тряска, поднятие лапы, высунутый язык, устранение, рычание, поворот головы, подгибание хвоста, съеживание, дрожь, кружение, хождение, прятание, тяжёлое дыхание, слюноотделение, вой, нытье и поведение против ограды (любое поведение, при котором собака физически контактировала с забором, например, прыжки на забор или вставание против него).Видео было проанализировано наблюдателем, имеющим опыт видеоанализа поведения собак. Чтобы измерить точность наблюдений, второй наблюдатель, также имеющий предыдущий опыт поведенческого анализа видео, проанализировал 3 видео с использованием того же программного обеспечения (BORIS), и было вычислено согласие между наблюдателями.
2.3. Присутствие страха в комнате сбора
После записи видео 2–3 собаки одновременно были приведены на поводке в комнату в приюте, отсюда называемую комнатой сбора.Это движение заняло около двух минут. В комнате для сбора собак держали на поводке, привязанном к столу.
Наличие страха во время забора крови оценивалось качественно (да / нет) в результате глобального рассмотрения поведения собаки в течение времени, проведенного в комнате для забора крови (20,6 ± 7,0 мин). Страх оценивался как «да» тем собакам, которые проявляли по крайней мере одно из поведений, связанных со страхом [64], например, поднятый хвост, дрожание, съеживание и прятание за предметами или в углу, избегание зрительного контакта и приближения. , и замораживание.2.4. Сбор и хранение образцов сыворотки
Кровь (3–4 мл) была взята из головной вены в комнате для сбора ветеринаром, входящим в состав персонала приюта и знакомым всем собакам, что позволило максимально избежать стресса для собаки. Только ветеринар принимал участие как в удерживании собаки во время забора, так и в заборе крови.
На основании предыдущей литературы о времени, в которое пролактин и кортизол достигают своих максимальных значений и уменьшаются в крови после стрессовой ситуации у людей [65,66], образцы были собраны примерно через 10 минут (в диапазоне от 5 до 15 минут) после попадания в комната для сбора.Когда процедура (идентификация, забор крови и клиническое обследование) была завершена для всех собак в комнате, их вместе поместили в их бокс.Пробирки с кровью хранили в холодильнике (4 ° C) в вертикальном положении в мягком ящике. Через 50–90 мин кровь центрифугировали при 3000 об / мин в течение 20 мин (с использованием Nahita 2615 Auxilab SL, Бериан, Испания). Образцы сыворотки хранили в пробирках Эппендорфа, которые держали вертикально в морозильной камере (-18 ° C) и поддерживали замороженными до анализа.
2.5. ELISA Kit
Концентрации пролактина и кортизола в собачьей сыворотке измеряли с помощью набора EIA (иммуноферментный анализ) (Demeditec Diagnostics ® , Киль, Германия для пролактина; Diametra ® , Segrate, Италия для кортизола), согласно инструкции производителя.
2.6. Статистический анализ
Тест Шапиро-Уилка (p <0,05) был применен к трем параметрам (пролактин, кортизол и оценка стресса) для исследования нормальности данных.Ни у одного из них не было обнаружено нормального распределения; поэтому дальнейший анализ проводился с использованием непараметрической статистики.
Сравнение между собаками, показывающими страх, и собаками, не показывающими страха в помещении для сбора, было выполнено для каждого параметра с помощью U-критерия Манна-Уитни (p <0,05).
Возможная корреляция между уровнями пролактина в сыворотке (нг / мл), уровнями кортизола в сыворотке (нг / мл) и показателем стресса исследовалась с использованием коэффициента ранговой корреляции Спирмена (p <0.05).
4. Обсуждение
Научной литературы о нормальных диапазонах пролактина у собак относительно мало. Хорошо задокументировано, учитывая его роль в лактации, что пролактин увеличивается у беременных и, прежде всего, у кормящих сук, а также у псевдобеременных сук [67,68] со значениями в диапазоне от 0 до примерно 40 нг / мл через 10 недель после эструс [67,69]. Что касается здоровых собак-самцов, исследования, проведенные на интактных самцах, выявили разные, но схожие диапазоны [70,71,72], которые можно суммировать как нормальный диапазон у интактных самцов в диапазоне от неопределяемого до 6 нг / мл [71] .Некоторые факторы, такие как порода, по-видимому, ответственны за различия в секреции пролактина у интактных кобелей [71,72], тогда как возраст не имеет значения [71]. Результаты настоящего исследования относятся к кастрированным самцам, собакам, размещенным в приюте, и к породе собак, ранее не участвовавшей в исследованиях пролактина, поэтому их интерпретацию следует проводить осторожно. Однако данные, представленные на Рисунке 1, а также среднее значение показывают, что у большинства задействованных собак концентрации пролактина превышали пороговое значение, указанное Corrada et al.[71], а у некоторых собак значения были ближе или выше, чем у Pageat et al. [28] для тревожных собак, получавших флуоксетин или селегилин (около 13 нг / мл). Результаты этого исследования по концентрации кортизола в сыворотке показали высокую индивидуальную вариабельность в соответствии с Bennett и Hayssen [43]. Полученные здесь значения включены в широкий диапазон (5–100 нг / мл) для исходного уровня кортизола, измеренного с помощью набора для ELISA в сыворотке собак, принадлежащих клиенту [73]. Однако в других исследованиях сообщается о более узком диапазоне, варьирующемся в зависимости от физиологического состояния собак и используемых аналитических методов [74,75,76,77], что затрудняет сравнение и определение значений, найденных в текущем исследовании.Вообще говоря, среднее значение кортизола в сыворотке, полученное в этом исследовании, было выше, чем ожидалось для здоровых домашних собак. Высокие значения кортизола могут быть связаны со многими факторами, включая потенциальное хроническое стрессовое состояние, в котором живут собаки в приюте, с последующим нарушением регуляции оси HPA [48,56]. Это будет обсуждено позже. Если посмотреть на взаимосвязь между исследуемыми параметрами, значения сывороточного пролактина не коррелировали со шкалой стресса, и они слабо отрицательно коррелировали с уровнями кортизола в сыворотке.Несколько авторов сообщили, что стрессовые ситуации могут привести к более высокому уровню циркулирующего пролактина у различных видов [3,4,5,6,7,8,9,11,12,13,14,15,16], предполагая, что пролактин может быть хороший биомаркер острого стресса. Результаты настоящего исследования не подтверждают эту гипотезу. Однако другие исследования показали, что связанные со стрессом изменения кортизола не влияют на уровень пролактина [19,78,79] или даже сообщают об отрицательной корреляции между уровнями кортизола и пролактина [21,22,30,80,81].Собриньо и др. [22] предположили, что эта отрицательная корреляция может быть связана с тем фактом, что высвобождение пролактина действует как альтернативная форма, а не как продолжение более распространенной реакции кортизола, таким образом, каждый гормон может высвобождаться в ответ на определенные эмоции [22]. Фактически, нервные пути, ответственные за реакцию кортизола и пролактина на стресс, различны у грызунов [82], которые часто выделяют пролактин в ответ на острый психологический стресс [83]. Аналогичным образом, у собак, находящихся в приюте, в то время как уровни пролактина в сыворотке крови снижались в ответ на стресс, не наблюдалось изменений концентрации кортизола в сыворотке [58].Пролактин имеет прямое влияние на секрецию окситоцина, и оба гормона модулируют нейроэндокринную реакцию на острый стресс во время материнского поведения, оказывая анксиолитический эффект у беременных и кормящих крыс [84,85]. Тем не менее, реакция пролактина на стресс, по-видимому, не ограничивается самками: в исследовании Siracusa et al. Не было значительного взаимодействия между полом и изменением концентрации пролактина в сыворотке между временными точками у собак, подвергшихся воздействию синтетического, успокаивающего собак феромон как до, так и после операции [58].Следует отметить, что то, как люди реагируют на стресс и страх, может зависеть от их индивидуального прошлого. Собаки, участвовавшие в текущем исследовании, сталкивались с ситуациями жестокого обращения, безнадзорности и / или покинутости до того, как попали в приют, что можно рассматривать как стрессовые ситуации. Можно предположить, что их индивидуальная история могла существенно повлиять на их способ реагирования на острую стрессовую ситуацию. Фактически, было показано, что высвобождение дофамина увеличивается в ответ на острый стресс у крыс, если они ранее подвергались хроническому стрессу [86].Это согласуется со снижением концентрации пролактина у собак в приюте с предполагаемым хроническим стрессом, которые подвергались острому стрессу [25]. В текущем исследовании концентрации пролактина не коррелировали ни с показателем стресса, ни с поведением страха в помещении для сбора. . Этот результат, вместе с нехваткой публикаций о реакции пролактина на стресс у собак [58], убедительно свидетельствует о необходимости будущих исследований, посвященных острым стрессовым факторам, которые могут предоставить дополнительную информацию о возможном использовании пролактина в качестве биомаркера острого стресса у собак. домашние собаки.Следует отметить, что большинство собак не проявляли испуганного поведения в помещении для сбора. Это не могло быть следствием их знакомства с этим местом, поскольку посещение ветеринарных учреждений происходило только для ветеринарной помощи и хирургических вмешательств. Тем не менее, присутствие как знакомых людей (персонал приюта), так и знакомых собак (товарищей по боксу), вероятно, уменьшило стресс от новизны и забора крови в комнате для сбора. Возможное объяснение результатов текущего исследования по кортизолу заключается в том, что некоторые собаки, принадлежащие к группе В выборке могут находиться хронические стрессы, и их уровень кортизола отражает такое состояние: фактически, собаки из приюта часто подвергаются стрессовым условиям [87], а собаки из текущей выборки переживали отказ, жестокое обращение и / или пренебрежение.Другими словами, отсутствие корреляции, обнаруженной между уровнями кортизола, показателем стресса и поведением страха в комнате для сбора, как ранее сообщалось о взаимосвязи между уровнями кортизола и пролактина, может быть объяснено тем фактом, что на значения кортизола влияли факторы, помимо те, которые проанализированы в этом исследовании. Например, длительное пребывание в приюте, в котором жили собаки в нашей выборке, могло привести к хроническому стрессу, что привело к подавлению и дерегулированию оси HPA [48].Фактически, в нескольких исследованиях сообщалось о вариациях кортизола в зависимости от того, как долго собаки находились в приюте [88,89,90,91,92]. Этот момент, вместе с другими недостатками, о которых ранее сообщалось для кортизола, делает еще более актуальным потребность в альтернативных легко измеримых биомаркерах стресса. Можно утверждать, что если уровень пролактина остается постоянно повышенным в течение длительного периода стресса, то этот гормон может быть хорошим биомаркером хронического стресса у собаки. Если уровень пролактина у длительно проживающих в приюте собак был повышен, а уровень кортизола варьировался в зависимости от благополучия собаки, e.g., уменьшаясь вместе со временем пребывания в приюте [90,91,92], то можно ожидать отрицательной корреляции между пролактином и кортизолом, как частично сообщалось в текущем исследовании. Желательно, чтобы дальнейшие исследования выяснили, является ли пролактин хорошим кандидатом на роль биомаркера хронического стресса у собак. Для этого необходимо принять во внимание, что в настоящее время использование других биологических матриц, кроме крови, для измерения пролактина у собак не рекомендуется [93].В этом исследовании представлены некоторые слабые стороны и ограничения. Одним из ограничений является то, что это исследование было сосредоточено на оценке возможной связи между пролактином и другими показателями стресса, но не проводился анализ для изучения возможного влияния таких факторов, как количество собак в боксе, вариабельность предыдущего индивидуального опыта и т. Д. Кроме того, общий опыт, например, проживание в одной клетке, может иметь влияние и приводить к эффекту клетки, который не исследовался в текущем исследовании.В будущих исследованиях, включающих более широкую выборку, следует учитывать эти факторы. Еще одно ограничение заключается в том, что, хотя, с одной стороны, однородность выборки может снизить вариабельность данных, конкретные характеристики собак (порода, пол, половой статус, предыдущий опыт и менеджмент) требуют осторожности при обобщении результатов на всех собак. популяции, в частности домашних собак, чей предыдущий опыт может заставить их по-разному реагировать на стресс. Потенциальная слабость этого исследования связана с отсутствием знаний о времени высвобождения пролактина и его снижения после стрессового события, особенно у собак.Дальнейшие исследования должны лучше изучить этот момент.
Гормональная реакция на стресс не изменяется из-за резкого снижения концентрации пролактина в плазме во время операции по поводу микропролактиномы
Эндокринная реакция на стресс широко изучается с начала 1950-х годов.1-3 Большинство исследований, однако, проводились на людях. проводились у пациентов, разнородных по патологии, типу операции или протоколу анестезии1. 4-7 Эндокринная реакция на хирургический стресс недавно изучалась с участием более однородных групп пациентов, а именно, недоношенных детей, 8 новорожденных, 9 детей, 10 или взрослых 11, но данные об операции на гипофизе немногочисленны.12 Основываясь на вышеизложенных результатах, настоящая работа преследовала тройную цель: (1) изучить гормональный ответ, в частности ответ передней доли гипофиза, и хирургический стресс в популяции, очень однородной с точки зрения пола и патологии (женщины с микропролактиномами ) и протокол анестезии; (2) оценить непосредственный эффект снижения концентрации пролактина на концентрацию других гормонов, участвующих в стрессовой реакции, таких как кортизол, АКТГ, GH и β-эндорфин, путем частого отбора проб до, во время и после операции.Хотя было установлено, что эндогенные опиоиды, в частности β-эндорфин, стимулируют секрецию пролактина, 13 мало что известно о влиянии пролактина на секрецию β-эндорфина у людей; (3) из-за предыдущих сообщений о том, что опиаты могут индуцировать высвобождение как гликозилированных, так и негликозилированных форм пролактина неаденомными клетками14, мы также исследовали in vivo действие экзогенных опиатов на секрецию пролактина аденомными клетками у этих пациентов.
Пациенты и методы
Тридцать шесть женщин в возрасте от 18 до 44 (средний 29) лет с микропролактиномой, а также 10 здоровых женщин (без эндокринных аномалий и без лечения) в возрасте от 21 до 39 (средний 31) год были включены в исследование.Диагностическими критериями микропролактиномы были: (1) синдром аменореи или аменореи-галактореи; (2) опухоль гипофиза, видимая на МРТ, не более 10 мм в самом большом диаметре; и (3) базальные концентрации ПРЛ выше 20 мкг / л и не более 250 мкг / л, не стимулируемые TRH или метоклопрамидом. Все пациенты и контрольная группа были проинформированы о целях и методах исследования в соответствии с Хельсинкской конвенцией, и мы получили согласие этического комитета клиники Timone Teaching Hospital.Критериями исключения были пациенты со смешанной аденомой, пациенты с хронической болью и пациенты с противопоказаниями к анестезии или хирургическому вмешательству. Пациенты, перенесшие трансфеноидальную резекцию по поводу аденомы, секретирующей пролактин, также были исключены. Из 36 пациентов 12 принимали бромокриптин (2,5–5 мг / кг) в течение 1–60 (в среднем 17) месяцев до операции. Лечение было прекращено за 1-10 месяцев до операции. Двадцать четыре были прооперированы без промедления.
ХИРУРГИЯ
Все пациенты были прооперированы одним и тем же хирургом риносептальным путем.Операция началась в 8:30 ± 5 минут, а продолжительность, измеренная между разрезом кожи и окончанием резекции, составила 50 ± 5 минут.
АНЕСТЕЗИЯ
Анестезию проводил тот же анестезиолог. Премедикация проводилась за 30 минут до индукции и включала 10 мг / кг морнифлумата (суппозиторий) и 20 мкг / кг лоразепама (внутримышечно). Индукция проводилась пропофолом (2,5 мг / кг) и бромидом панкурония (8 мг / кг). После интубации обезболивание получали феноперидином 20 мкг / кг и поддерживали N 2 O / O 2 (60% / 40%).При установке транспалатиновых ретракторов вводили 20 мкг / кг альфентанила.
ОБРАЗЦЫ
Всего 23 образца (каждый по 3 мл) венозной крови были взяты в ЭДТА от каждого пациента с помощью небольшого катетера. Первый образец брали перед премедикацией (за 30 минут до индукции), затем каждые 10 минут, начиная за 20 минут до индукции анестезии и до 80 минут после экстубации. Последний образец был взят через 24 часа после экстубации. В контрольной группе брали только одну пробу между 8:00 и 8:30 утра.Образцы немедленно центрифугировали при 2500 g в течение 10 минут, а надосадочные жидкости замораживали при -80 ° C перед анализом.
МЕТОДЫ АНАЛИЗА
Пролактин анализировали методом иммуноферментной флуоресценции с помощью прибора Stratus II (DADE®). Чувствительность составляла 0,4 нг / мл, а коэффициент вариации внутри анализа составлял 4%. Кортизол и GH анализировали методом хемилюминесценции с использованием прибора Immulite® (Behring). Чувствительность и коэффициент вариации внутри анализа составляли 4 пг / мл и 6% для GH и 2 нг / мл и 9% для кортизола.АКТГ и β-эндорфин-подобная иммунореактивность (называемая β-эндорфином в остальной части статьи) анализировали с помощью радиоиммуноанализа, как описано ранее.15-17 Предел обнаружения и коэффициент вариации внутри анализа составляли 2 пг / мл. и 7% для АКТГ, и 3 пг / мл и 9% для β-эндорфина. Перекрестные реакции для β-эндорфина составляли 50% с β-липотропином, <1% с лей-энкефалином и мет-энкефалином и <0,5% с динорфином 1-17. Другие опиоидные пептиды не мешали анализу.
СТАТИСТИЧЕСКИЙ АНАЛИЗ
Тест Манна-Уитни U использовался для сравнения базальных концентраций гормонов у пациентов и контрольной группы, дисперсионного анализа (ANOVA) для сравнения интраоперационных изменений концентраций гормонов и рангового коэффициента Спирмена для анализа корреляции между β-эндорфином, АКТГ, и концентрации кортизола.Коэффициент корреляции Спирмена рассчитывали на основе концентраций β-эндорфина, кортизола и АКТГ.
Результаты
Среди 36 пациентов, включенных в исследование, у 32 не было рецидива через 186 месяцев, у трех не было лечения. У одного пациента по техническим причинам разрез кожи был сделан через 30 минут после индукции.
БАЗАЛ КОНЦЕНТРАЦИИ
Не было различий в базальных концентрациях GH, ACTH, β-эндорфина и кортизола между пациентами и контрольной группой (таблица).У пациентов базальные концентрации пролактина были значительно выше (Mann-Whitney, p <0,0001).
КИНЕТИКА
У всех пациентов не наблюдалось увеличения концентрации пролактина после двух курсов лечения морфиноподобными препаратами (между временем 1 и 2 и моментом 3, рис. 1, 2 и 3).
фигура 1Средние значения (SD) предоперационных, периоперационных и послеоперационных концентраций некоторых гормонов, участвующих в реакции на стресс во время резекции микропролактином ринопалатиновым путем у 32 женщин.Образцы отбирали каждые 10 минут, начиная непосредственно перед премедикацией (за 30 минут до индукции) и до 80 минут после экстубации. Время 1 — индукция, время 2 — разрез кожи, время 3 — установка транспалатиновых ретракторов, время 4 — окончание резекции аденомы и время 5 — экстубация. Обратите внимание, что между временем 1 и 2 вводили феноперидин (20 мкг / кг) и в момент 3, альфентанил (20 мкг / кг).
фигура 2Средние значения (SD) предоперационных, периоперационных и послеоперационных концентраций GH и пролактина во время хирургической резекции микропролактином у трех женщин, у которых операция не была успешной.Образцы были взяты, как на рис. 1. Обратите внимание на отсутствие быстрого падения после окончания резекции.
Рисунок 3Предоперационные, периоперационные и послеоперационные изменения концентраций кортизола, АКТГ, β-эндорфина, GH и пролактина при хирургии микропролактиномы. У этого пациента по техническим причинам разрез кожи был сделан через 30 минут (а не через 10 минут) после индукции, в отличие от других пациентов. Обратите внимание, что перед хирургической процедурой наблюдается ранний пик GH.
У 32 потенциально излеченных женщин (рис. 1) наблюдалось резкое снижение концентрации пролактина, которое было значительным уже через 10 минут после окончания резекции (время 4 + 10 минут; p <0,001).
Гормон роста
Наблюдалось значительное увеличение концентрации GH, которое начиналось через 10 минут после момента индукции анестезии (время 2; p> 0,01), достигая максимума через 30 минут после индукции (рис. 1). Наблюдалось второе и значительное увеличение концентрации GH, начиная с экстубации (время 5; p <0.01), достигая максимума через 1 час после инкубации.
Β-эндорфин
Наблюдалось значительное снижение уровня β-эндорфина через 30 минут после индукции (время 3; p <0,01). И наоборот, увеличение стало значительным через 60 минут после индукции (p <0,001), достигнув кульминации через 15 минут после экстубации (рис. 1). Через 24 часа после экстубации концентрация в плазме крови вернулась к исходной.
Кортизол
Уровень кортизолабыл значительно ниже базального через 20 минут после индукции (время 1 + 20 минут, p <0,01), и снижение продолжалось до конца резекции.Напротив, через 30 минут после окончания резекции наблюдалась значительная высокая концентрация кортизола (время 4 + 30 минут; p <0,01), достигающая кульминации через 1 час после экстубации и достигая примерно 1,5-кратного базального уровня. Кортизол вернулся к исходной концентрации через 24 часа после экстубации.
ACTH
Через 20 и 30 минут после индукции наблюдалась достоверно низкая концентрация АКТГ в плазме (p <0,01). Напротив, через 20 минут после окончания резекции наблюдалось значительное увеличение концентрации АКТГ в плазме (p <0.001) с пиком во время экстубации (время 5).
У трех женщин, у которых операция не была успешной, не было обнаружено падения концентрации пролактина до времени 4+ 40 минут (рис. 2). За исключением пролактина, гормональная реакция на стресс была в том же диапазоне, что и у 32 потенциально излеченных пациентов.
Наконец, в случае пациента, у которого операция была отложена, была получена такая же гормональная реакция на хирургический стресс (рис. 3).
Корреляции
Было обнаружено две корреляции β-эндорфина, одна с АКТГ (R Спирмена = 0.95, p <0,001), другой - с кортизолом (R Спирмена = 0,88, p <0,001, рис. 4). Кортизол и АКТГ также коррелировали (R = 0,87; p <0,0001).
Рисунок 4Кривая регрессии β-эндорфина в зависимости от концентрации АКТГ и кортизола у 32 пациентов, оперированных по поводу микропролактиномы. Кривая строилась после учета средних концентраций АКТГ, кортизола и β-эндорфина в плазме, измеренных в девяти временных точках: за 30 минут до индукции, во время индукции, затем каждые 30 минут до 180 минут после индукции анестезии.Последний образец был взят через 24 часа после экстубации.
Обсуждение
Секреция пролактина находится под двойным контролем — ингибирующими факторами, наиболее важным из которых является дофамин18-20, и стимулирующими факторами. Среди вторых установлено, что морфиноподобные соединения14 21 например, эндогенные опиоиды, 18 22, в частности β-эндорфин, 13 стимулируют не только секрецию пролактина, но также секрецию GH.23 Тем не менее, β-эндорфин in vitro не имеет прямого действия на секрецию пролактина, но противодействует подавляющему контролю, осуществляемому дофамином.22 Это ингибирующее действие на дофаминергические нейроны 24 Считается, что 25 осуществляется через активацию μ- и k-рецепторов26.
Плазменный β-эндорфин секретируется стволом гипофиза, тогда как β-эндорфин спинномозговой жидкости возникает из ЦНС.27 В нашем исследовании мы измеряли концентрацию β-эндорфина в плазме только каждые 30 минут, потому что его период полураспада более длительный. чем другие гормоны передней доли гипофиза.27 В начале операции концентрация β-эндорфина оставалась низкой, несомненно, из-за введения экзогенных морфиноподобных препаратов, которые ингибировали его секрецию из гипофиза.9 28 С другой стороны, наблюдалось повышение концентраций АКТГ и β-эндорфина, значительное через 30 минут после установки транспалатиновых ретракторов и продолжающееся в период восстановления. Это предполагает, что либо интенсивность боли была достаточной для преодоления отрицательного эффекта морфина на секрецию CRF, либо клетки кортикотропина стимулировались рилизинг-фактором, отличным от CRF. Известно, что аргинин вазопрессин (АВП) стимулирует секрецию β-эндорфина и АКТГ. Интересно, что было показано, что в гипофизарной портальной крови овцы умеренный стресс вызывает равное высвобождение CRF и AVP, тогда как во время интенсивного стресса секреция AVP была намного более стимулированной, чем секреция CRF.29 Поскольку концентрация β-эндорфина в плазме увеличивалась примерно через 30 минут после болезненного раздражителя 30 31 боль, вызванная размещением ретрактора, несмотря на сопутствующее введение альфентанила, а также болевой стресс, сопровождающий пробуждение, могут объяснить кинетику, полученную в нашем исследовании. Сопоставимые кинетические результаты были опубликованы для операций на сердце9 и гипофиза12.
Периоперационное повышение уровня пролактина и гормона роста в ответ на стресс известно давно.7 Однако в случае наличия аденомы пролактина введение опиатов не вызывает высвобождения пролактина, как сообщалось в случае неаденомных клеток14. по-видимому, не влияет на кинетику других гормонов, участвующих в стрессе. Действительно, такие же кривые были получены у трех женщин, у которых операция не была успешной, о чем свидетельствует отсутствие быстрого падения концентрации пролактина в плазме.
Что касается GH, первый пик считался результатом индукции анестезии, которая вызывает интенсивный стресс 12, а не боли по следующим причинам: (1) в общем случае концентрация GH увеличивалась вдвое перед любой хирургической процедурой; (2) в случае пациента, операция которого была отложена после индукции, перед операцией наблюдался пик GH, амплитуда которого была сопоставима с таковой у других пациентов. Эти данные предполагают, что первый пик GH был связан только с индукционным стрессом.Второй пик GH произошел одновременно с возвращением сознания, примерно через 40 минут после пика β-эндорфина. Поскольку в это время невозможно отделить боль от стресса пробуждения, невозможно определить, был ли второй пик вызван болью, стрессом или обоими одновременно. Поскольку АКТГ и β-эндорфин секретируются, различное время секреции GH и β-эндорфина также обнаруживается между GH и ACTH. Это наблюдается не только во время хирургического стресса, но и во время динамических тестов функции гипофиза.Таким образом, нельзя сделать вывод, что основной стресс различен для двух групп гормонов. Однако, поскольку секреция GH не изменяется под действием экзогенных опиоидов во время анестезии, измерение GH может быть полезным маркером стресса во время операции по поводу микропролактиномы.
Реакция коры надпочечников на хирургический стресс ослабляется введением морфиноподобных препаратов, 8 9, возможно, через ингибирование высвобождения CRF32 33 и АКТГ.34 Напротив, антагонисты морфина стимулируют секрецию АКТГ у животных35. 36 и у людей 37 , что свидетельствует о существовании ингибирующего тонического контроля, оказываемого эндогенными опиоидами на переднюю долю гипофиза.32 37 38 Эти эффекты могут быть вторичными по отношению к центральным или периферическим механизмам, но также и к прямому действию опиоидов на эндокринные железы. 39 Увеличение концентрации циркулирующего кортизола во время пробуждения в настоящем исследовании, хотя и умеренное, было значительным и подтверждает предыдущие выводы. .11 40 Это послеоперационное увеличение может быть связано с растормаживанием кортикотрофической оси во время отмены препарата. Однако повышение уровня кортизола во время хирургического стресса, вероятно, является эпифеноменом, потому что это повышение слишком мало, чтобы иметь сильные биологические эффекты.41 Не удалось включить в это исследование адекватную контрольную группу. Поскольку мы не включили хирургическую контрольную группу, измеренные ответы могут быть или не быть специфичными для операции на гипофизе или для пациентов с гиперпролактинемией, но это не было целью нашего исследования.
Гормональные реакции на хирургический стресс изучались как при общей анестезии14, так и при эпидуральной или перидуральной анестезии.10 42 Недавнее появление эндоскопических хирургических методов породило надежды на снижение хирургического стресса по сравнению с традиционным хирургическим вмешательством, но эта надежда была разбита сравнительным исследованием основных маркеров стресса во время различных типов анестезии.42 43 год
Наконец, существование корреляции между концентрациями β-эндорфина и АКТГ известно уже почти 20 лет.44 Эта корреляция, по-видимому, не меняется при наличии пролактиновой опухоли.
Наши выводы резюмируются следующим образом:
(1) Во время операции по поводу пролактиномы наличие раннего пика GH во время индукции анестезии, независимо от какой-либо хирургической процедуры, убедительно свидетельствует о том, что GH является предпочтительным маркером хирургического стресса, тогда как β-эндорфин секретируется в ответ на боль.
Тот факт, что GH является маркером хирургического стресса, был установлен во многих хирургических состояниях, включая хирургию органов малого таза.45 Наши результаты убедительно показывают, что это также верно во время операции по поводу микропролактиномы. Поскольку у детей сообщалось, что повышение концентрации гормона стресса во время хирургических процедур связано с послеоперационными метаболическими осложнениями, 8 будет интересно изучить связь между высокими концентрациями GH и послеоперационными осложнениями.
(2) Быстрое падение концентрации пролактина не влияет на высвобождение других гормонов, вызывающих стресс.
(3) Введение опиатов не вызывает высвобождения пролактина, как ранее сообщалось in vitro, из неаденомных клеток.
Таблица 1Средние значения (SD) базальных концентраций гормонов гипофиза и кортизола, измеренных у 36 пациентов с микропролактиномами и у 10 здоровых женщин (у пациентов образцы были взяты до премедикации, в контрольной группе образцы были взяты между 8:00 и 8:30 утра)
| Как крупный международный издатель академических и исследовательских журналов Science Alert издает и разрабатывает названия в партнерстве с самыми престижные научные общества и издатели.Наша цель заключается в том, чтобы максимально широко использовать качественные исследования аудитория. | ||||||
| Мы прилагаем все усилия, чтобы поддержать исследователей которые публикуют в наших журналах. Есть масса информации здесь, чтобы помочь вам публиковаться вместе с нами, а также ценные услуги для авторов, которые уже публиковались у нас. | ||||||
| 2021 цены уже доступны. Ты может получить личную / институциональную подписку перечисленных журналы прямо из Science Alert. В качестве альтернативы вы возможно, пожелает связаться с выбранным вами агентством по подписке. Направляйте заказы, платежи и запросы в службу поддержки клиентов. в службу поддержки клиентов журнала Science Alert. | ||||||
| Science Alert гордится своей тесные и прозрачные отношения с обществом. В виде некоммерческий издатель, мы стремимся к самому широкому возможное распространение публикуемых нами материалов и на предоставление услуг высочайшего качества нашим издательские партнеры. | ||||||
| Здесь вы найдете ответы на наиболее часто задаваемые вопросы (FAQ), которые мы получили по электронной почте или через контактную форму в Интернете.В зависимости от характера вопросов мы разделили часто задаваемые вопросы на разные категории. | ||||||
| Азиатский индекс научного цитирования (ASCI) стремится предоставить авторитетный, надежный и значимая информация по освещению наиболее важных и влиятельные журналы для удовлетворения потребностей мировых научное сообщество.База данных ASCI также предоставляет ссылку к полнотекстовым статьям до более чем 25000 записей с ссылка на цитированные ссылки. | ||||||